Hydroxiprogesteron caproate - Hydroxyprogesterone caproate
 | |
 | |
| Kliniska data | |
|---|---|
| Handelsnamn | Delalutin, Proluton, Proluton Depot, Makena, andra |
| Andra namn | OHPC; Hydroxiprogesteron -kapronat; Hydroxiprogesteronhexanoat; 17a-hydroxiprogesteron-kaprat; 17a-OHPC; 17-hydroxiprogesteronkaprat; 17-OHPC; 17-HPC; 17a-HPC; HPC; LPCN-1107; 17α-Hydroxipregn-4-en-3,20-dion 17α-hexanoat |
| Vägar administrering |
• Intramuskulär injektion • Subkutan autoinjektion |
| Drogklass | Progestogen ; Progestin ; Progestogenester ; Antigonadotropin |
| ATC -kod | |
| Farmakokinetiska data | |
| Biotillgänglighet |
Oralt : Mycket lågt (~ 3% hos råttor) Intramuskulärt : 100% (hos råttor) |
| Proteinbindning | Omfattande (till albumin , inte till CBG eller (sannolikt) SHBG ) |
| Ämnesomsättning | Reduktion och hydroxylering (via CYP3A4 , CYP3A5 , CYP3A7 ) och konjugering ( glukuronidering , sulfation , acetylering ) |
| Eliminering halveringstid | Icke-gravid: 7,8 dagar Singlet: 16–17 dagar Tvillingar: 10 dagar |
| Exkretion |
Avföring : 50% Urin : 30% |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.010.127 |
| Kemiska och fysiska data | |
| Formel | C 27 H 40 O 4 |
| Molmassa | 428,613 g · mol −1 |
| 3D -modell ( JSmol ) | |
| |
| |
| (kontrollera) | |
Hydroxiprogesteron caproate ( OHPC ), som bland annat säljs under varumärkena Proluton och Makena , är en gestagenmedicin som används för att förhindra för tidig förlossning hos gravida kvinnor med en historia av tillståndet och för att behandla gynekologiska störningar . Det har också formulerats i kombination med östrogener för olika indikationer (varumärken Gravibinon och Primosiston ) och som en form av långvarig injicerbar preventivmedel (varumärke Chinese Injectable No. 1 ). Det används inte i munnen och ges istället genom injektion i muskler eller fett , vanligtvis en gång i veckan till en gång i månaden beroende på indikationen.
OHPC tolereras i allmänhet väl och ger få biverkningar . Reaktioner på injektionsstället som smärta och svullnad är den vanligaste biverkningen av OHPC. Medicinen kan öka risken för graviditetsdiabetes vid användning hos gravida kvinnor. OHPC är ett gestagen, eller ett syntetiskt gestagen , och är därför en agonist för progesteronreceptorn , det biologiska målet för gestagener som progesteron . Den har viss antimineralokortikoid aktivitet och ingen annan viktig hormonell aktivitet. Medicinen visar ett antal skillnader från naturligt progesteron .
OHPC upptäcktes 1953 och introducerades för medicinskt bruk 1954 eller 1955. Det marknadsfördes i USA under varumärket Delalutin och i hela Europa under varumärket Proluton. Medicineringen avbröts i USA 1999. Men OHPC därefter återinfördes i USA under varumärket Makena för behandling av tidig födsel 2011. På grund av en kraftigt ökad pris, en pris kontrovers inträffade i det här landet. OHPC var tidigare tillgängligt till låg kostnad från sammansatta apotek i USA, men detta blev förbjudet 2016.
Medicinsk användning
För tidig förlossning
Användningen av OHPC under graviditet för att förhindra för tidig förlossning hos kvinnor med en historia av för tidig förlossning mellan 20 veckor och 36 veckor och 6 dagar stöds av Society of Maternal Fetal Medicine Clinic Guidelines som publicerades i maj 2012 som nivå I och III bevis, Nivå A rekommendation. Nivå I -bevis refererar till en korrekt driven randomiserad kontrollerad prövning , och nivå III -bevis är stöd från expertutlåtanden, medan en rekommendation på nivå A ger att rekommendationen är gjord baserad på goda och konsekventa vetenskapliga bevis. OHPC 250 mg IM varje vecka, helst från 16–20 veckor tills 36 veckor rekommenderas. Hos dessa kvinnor, om den transvaginala ultraljuds livmoderhalslängden förkortas till <25 mm vid <24 veckor, kan cervikal cerclage erbjudas. I 2013 års studie som rekommendationen baseras på var det också en signifikant minskning av neonatal sjuklighet inklusive lägre frekvenser av nekrotiserande enterokolit (0 i behandlingsgruppen mot 4 i kontrollen), intraventrikulär blödning (4 i behandlingsgruppen jämfört med 8 i kontrollen för en relativ risk på 0,25) och behov av kompletterande syre (14% i behandlingsgruppen mot 24% i placebo för en relativ risk på 0,42). Dessutom innehöll denna studie 463 kvinnor, varav 310 fick injektion. Av dessa kvinnor hade 9 spädbarn med medfödda missbildningar (2%), men det fanns inget konsekvent mönster och inga involverade inre organ.
OHPC är för närvarande (i juni 2014) graviditetskategori B, vilket innebär att det inte finns några tecken på fosterrisk med användning av detta läkemedel under graviditeten. Även om detta nu är rekommendationen har detta inte alltid varit fallet. En granskning av Marc Keirse från Flinders University drog slutsatsen att information om de potentiella skadorna saknades. Tre kliniska studier med singletongraviditeter på 250 mg/vecka intramuskulärt OHPC har alla visat en trend för en ökning av graviditetsförlusten på grund av missfall jämfört med placebo. En av dem, en stor National Institutes of Health (NIH) -studie 2003, tittade på effekten av OHPC -injektioner hos kvinnor med risk för upprepad för tidig födelse och fann att den behandlade gruppen upplevde för tidig födsel hos 37% kontra 55% i kontrollerna . En uppföljningsstudie av avkomman visade inga bevis för att OHPC påverkade barnen under de första åren av livet. Baserat på dessa NIH -data godkändes OHPC av Food and Drug Administration (FDA) 2011 som ett läkemedel för att minska risken för för tidig födelse hos utvalda kvinnor i riskzonen. (vi)
FDA uttryckte oro över missfall vid rådgivande kommitténs möte 2006; utskottet röstade enhälligt att ytterligare studier var nödvändiga för att utvärdera den potentiella kopplingen av OHPC med ökad risk för missfall i andra trimestern och dödfödelse. En toxikologisk studie på rhesus apor resulterade i att alla rhesusfoster utsattes för 1 och 10 gånger den mänskliga dosekvivalenten för OHPC. Från och med 2008 var OHPC en kategori D -progestin enligt FDA (det vill säga det finns tecken på fosterskada). Det finns spekulationer om att ricinoljan i OHPC -formuleringen kanske inte är fördelaktig för graviditet. Observera att ovannämnda NEJM-studie av Meirs et al. jämför effekten av OHPC (med ricinoljekomponenten) med ricinoljeinjektion som placebo.
En studie som publicerades i februari 2016 i The Lancet uppgav bland annat följande:
OPPTIMUM tyder starkt på att effekten av progesteron för att förbättra resultat är antingen obefintlig eller svag. Med tanke på heterogeniteten hos förtidigt arbetskraftssyndrom kan vi inte utesluta fördelar i specifika fenotypiska eller genotypiska undergrupper av kvinnor i riskzonen. Undergrupperna av kvinnor som kan dra nytta verkar dock inte vara lätta att identifiera med nuvarande urvalsstrategier, inklusive mätning av livmoderhalslängd och fibronektintestning. Bekräftande tyder vår studie på att progesteron är säkert för dem som vill ta det för tidig profylax. Den totala frekvensen av biverkningar hos mödrar eller barn var liknande i progesteron- och placebogrupperna. Det fanns få skillnader i förekomsten av negativa sekundära utfall i de två grupperna, med undantag för en högre frekvens av njur-, gastrointestinala och respiratoriska komplikationer i barndomen i progesterongrupperna. Viktigare är att de absoluta frekvenserna av dessa komplikationer var låga. Uppföljning av andra spädbarn exponerade i livmodern för vaginalt progesteron skulle vara till hjälp för att avgöra om den ökade frekvensen av vissa njur-, gastrointestinala och andningskomplikationer är en verklig effekt eller ett typ I-fel.
Tidskriftsgranskaren Richard Lehman, senior forskare vid Institutionen för primärhälsovård vid University of Oxford, gjorde följande anmärkningsvärda kommentarer till OPPTIMUM -studien: "Det är det. Den här historien är slut, och ingen behöver någonsin använda vaginalt progesteron igen för att förhindra för tidig förlossning. "
En Cochrane -översyn av gestagen för att förhindra för tidig förlossning drog slutsatsen att det fanns få bevis för att antingen vaginal eller intramuskulär progesteron hjälpte till att minska risken för för tidig födsel hos kvinnor med multipel graviditet.
Gynekologiska störningar
OHPC används för behandling av hotade missfall , gynekologiska störningar som dysmenorré , premenstruellt syndrom , fibrocystisk bröstsjukdom , adenos och bröstsmärta . Dessutom används OHPC vid behandling av endometriecancer och har visat sig vara avsevärt effektiv för att förlänga liv hos både premenopausala och postmenopausala kvinnor med sjukdomen. Läkemedlet användes i stor utsträckning på 1950 -talet till 1970 -talet för sådana indikationer, men OHPC har nyligen fått mest uppmärksamhet vid förebyggande av för tidig födsel .
Preventivmedel
OHPC är tillgängligt i kombination med östradiolvalerat som ett kombinerat injicerbart preventivmedel en gång i månaden i några få länder.
Andra användningsområden
OHPC har använts som en del av menopausal hormonbehandling hos kvinnor.
OHPC har använts för att behandla godartad prostatahyperplasi hos män, även om bevis på effektivitet är marginella och osäkra. Det har också använts för att behandla prostatacancer , i en dos av 1500 mg två gånger per vecka. Verkningsmekanismen för OHPC vid dessa användningsområden är undertryckande av testikulär androgenproduktion via undertryckande av luteiniserande hormonsekretion, som är resultatet av den progestogena och antigonadotropa aktiviteten hos OHPC. Symtom på hypogonadism kan dock utvecklas när OHPC används för denna indikation, där två tredjedelar av männen uppges ha impotens .
OHPC har använts som en komponent i feminiserande hormonbehandling för transpersoner . På grund av mikronisering används mer bioidentiska gestagener.
Tillgängliga blanketter
OHPC finns ensamt i form av ampuller och injektionsflaskor med 125 och 250 mg/ml oljelösningar för intramuskulär injektion (varumärken Proluton, Makena). Det är också tillgängligt ensamt i form av en 250 mg/ml autoinjektor för subkutan injektion (varumärke Makena).
OHPC finns eller var tillgängligt i kombination med östradiolvalerat i form av ampuller och injektionsflaskor med 250 mg/ml OHPC och 5 mg/ml östradiolvalerat oljelösningar för intramuskulär injektion (varumärken Gravibinon, Chinese Injectable No. 1). Läkemedlet finns eller var tillgängligt i kombination med östradiolbensoat i form av ampuller med 125–250 mg OHPC och 10 mg östradiolbensoat i oljelösning för intramuskulär injektion (varumärke Primosiston) också. Dessutom har OHPC marknadsförts i kombination med östradiol dipropionat i form av 50 mg/ml OHPC och 1 mg/ml östradiol dipropionat (varumärke EP Hormone Depot) i Japan .
Kontraindikationer
Kontraindikationer för OHPC inkluderar tidigare eller nuvarande trombos eller tromboembolisk sjukdom , känd eller misstänkt bröstcancer , tidigare eller nuvarande historia av annan hormonkänslig cancer , odiagnostiserad onormal vaginal blödning som inte är relaterad till graviditet , kolestatisk gulsot av graviditet , levertumörer eller aktiv leversjukdom , och okontrollerad hypertoni . Några relativa kontraindikationer finns också för OHPC.
Bieffekter
OHPC tolereras i allmänhet väl och ger relativt få biverkningar . Reaktioner på injektionsstället som smärta , ömhet , svullnad , klåda , blåmärken och klumpar är den vanligaste biverkningen av OHPC. I motsats till stora doser av progesteron, som ger måttliga till svåra sådana reaktioner, är OHPC dock relativt fritt från reaktioner vid injektionsstället. Biverkningar av OHPC som förekommer hos mer än eller lika med 2%av användarna inkluderar smärta vid injektionsstället (34,8%), svullnad på injektionsstället (17,1%), urtikaria (12,3%), klåda (7,7%), klåda på injektionsstället (5,8) %), illamående (5,8%), knutor på injektionsstället (4,5%) och diarré (2,3%). Numeriskt ökade frekvenser i förhållande till kontroller av missfall (2,4% mot 0%), dödfödsel (2,0% mot 1,3%), intag för för tidigt arbete (16,0% mot 13,8%), preeklampsi eller graviditetshypertension (8,8% mot 4,6 %), graviditetsdiabetes (5,6%mot 4,6%) och oligohydramnios (3,6%mot 1,3%) har observerats med OHPC i kliniska prövningar där det gavs till gravida kvinnor för att förhindra för tidig födsel.
Överdos
Det har inte rapporterats om överdosering av OHPC. Vid överdosering bör behandlingen baseras på symptom . OHPC har studerats hos människor vid höga doser på 2 000 till 5 000 mg per vecka genom intramuskulär injektion, utan säkerhetsproblem .
Interaktioner
OHPC påverkar sannolikt inte de flesta cytokrom P450 -enzymer vid terapeutiska koncentrationer. Läkemedelsinteraktionsstudier har inte utförts med OHPC.
Farmakologi
Farmakodynamik
OHPC har gestagenaktivitet , viss antimineralokortikoidaktivitet och ingen annan viktig hormonell aktivitet.
| Förening | hPR-A | hPR-B | rbPR | rbGR | rbER | |||
|---|---|---|---|---|---|---|---|---|
| Progesteron | 100 | 100 | 100 | <1 | <1 | |||
| 17α-hydroxiprogesteron | 1 | 1 | 3 | 1 | <1 | |||
| Hydroxiprogesteron caproate | 26 | 30 | 28 | 4 | <1 | |||
| Hydroxiprogesteronacetat | 38 | 46 | 115 | 3 | ? | |||
| Anmärkningar: Värdena är procentsatser (%). Referensligander (100%) var progesteron för PR , dexametason för GR , och östradiol för ER . Källor: Se mall. | ||||||||
| Förening | Form | Dos för specifik användning (mg) | DOA | |||
|---|---|---|---|---|---|---|
| TFD | POICD | CICD | ||||
| Algestonacetofenid | Oljesol. | - | - | 75–150 | 14–32 d | |
| Gestonorone caproate | Oljesol. | 25–50 | - | - | 8–13 d | |
| Hydroxyprogest. acetat | Aq. misst. | 350 | - | - | 9–16 d | |
| Hydroxyprogest. caproate | Oljesol. | 250–500 | - | 250–500 | 5–21 d | |
| Medroxyprog. acetat | Aq. misst. | 50–100 | 150 | 25 | 14–50+ d | |
| Megestrolacetat | Aq. misst. | - | - | 25 | > 14 d | |
| Noretisteron enanthate | Oljesol. | 100–200 | 200 | 50 | 11–52 d | |
| Progesteron | Oljesol. | 200 | - | - | 2–6 d | |
| Aq. soln. | ? | - | - | 1–2 d | ||
| Aq. misst. | 50–200 | - | - | 7–14 d | ||
|
Anteckningar och källor:
|
||||||
Progestogen aktivitet
OHPC, även känt som 17α-hydroxiprogesteronkaprat, ligger närmare progesteron när det gäller struktur och farmakologi än de flesta andra gestagener och är i huvudsak ett rent progestogen- det vill säga en selektiv agonist för progesteronreceptorn (PR) med minimal eller ingen annan hormonell aktivitet. OHPC har dock förbättrat farmakokinetiken jämfört med progesteron, nämligen en mycket längre varaktighet med intramuskulär injektion i oljelösning .
Administrerad genom intramuskulär injektion är endometrieomvandlingsdosen för OHPC per cykel 250 till 500 mg och den veckovisa substitutionsdosen för OHPC är 250 mg, medan den effektiva dosen av OHPC i menstruationsfördröjningstestet (Greenblatt) är 25 mg per vecka. En effektiv ägglossningshämmande dos av OHPC är 500 mg en gång per månad genom intramuskulär injektion. Dosen av OHPC som används i kombinerade injicerbara preventivmedel en gång i månaden är emellertid 250 mg, och denna kombination är effektiv för att hämma ägglossning på samma sätt. För jämförelse är dosen medroxiprogesteronacetat (MPA; 6α-metyl-17α-hydroxiprogesteronacetat), en nära analog av OHPC, som används genom intramuskulär injektion i mikrokristallint vattenhaltig suspension i kombinerade injicerbara preventivmedel en gång i månaden, 25 mg. Det har också sagts att 250 mg OHPC i oljelösning med intramuskulär injektion är ekvivalent i progestogen effekt med 50 mg medroxiprogesteronacetat i mikrokristallin vattenhaltig suspension. Även om halveringstiden för intramuskulär OHPC i oljelösning hos icke-gravida kvinnor är cirka 8 dagar, är halveringstiden för intramuskulär medroxiprogesteronacetat i mikrokristallin vattenhaltig suspension hos kvinnor cirka 50 dagar. OHPC är också i viss mån mindre potent än den mer nära besläktade ester hydroxiprogesteron-acetat (OHPA; 17α-hydroxiprogesteron-acetat).
17α-Hydroxyprogesteron (OHP) har svag progestogen aktivitet, men C17α- förestring resulterar i högre gestagenaktivitet. Av en mängd olika estrar , den kaproat ades (hexanoat) -ester befanns ha den starkaste progestogen aktivitet, och detta tjänade som grund för utvecklingen av OHPC, liksom andra kaproat progestogen estrar såsom gestonorone kaproat . OHPC är ett mycket mer potent gestagen än 17a-hydroxiprogesteron, men har inte lika hög affinitet för PR som progesteron. OHPC har cirka 26% och 30% av progesterons affinitet för humant PR-A respektive PR-B . Läkemedlet var inte mer effektivt än progesteron för att aktivera dessa receptorer och framkalla associerat genuttryck in vitro .
Antigonadotropa effekter
På grund av aktivering av PR, har OHPC antigonadotropic effekter, eller producerar hämning av hypotalamus-hypofys-gonad-axeln , och kan avsevärt undertrycka gonadotropin sekretion och gonadal könshormonproduktion vid tillräckligt höga doser. En studie visade att OHPC genom intramuskulär injektion i en dos av 200 mg två gånger i veckan under de första två veckorna och sedan 200 mg en gång i veckan i 12 veckor inte signifikant påverkade urinutsöndring av östrogener , luteiniserande hormon eller follikelstimulerande hormon hos män med godartad prostatahyperplasi. I en annan studie som använde en ospecificerad dos av intramuskulär OHPC, utvärderades testosteronsekretion hos en enda man och befanns minska från 4,2 mg/dag till 2,0 mg/dag (eller med cirka 52%) med 6 veckors behandling, medan utsöndring av luteiniserande hormon förblev oförändrat hos mannen. Ännu en studie visade att 3000 mg/vecka OHPC genom intramuskulär injektion dämpade testosteronnivåerna från 640 ng/dL till 320–370 ng/dL (med 42–50%) hos en enda man med prostatacancer, vilket liknade testosteronundertryckningen med cyproteronacetat eller klormadinonacetat . Gestonoron caproate , ett närbesläktat gestagen till OHPC med cirka 5 till 10 gånger större styrka hos människor, visade sig undertrycka testosteronnivåer med 75% vid en dos av 400 mg/vecka hos män med prostatacancer. Som jämförelse minskade orchiektomi testosteronnivåerna med 91%. I allmänhet kan progestiner maximalt undertrycka testosteronnivåer med cirka 70 till 80%. De antigonadotropa effekterna av OHPC och därmed dess testosteronsuppression är grunden för användningen av OHPC vid behandling av godartad prostatahyperplasi och prostatacancer hos män. Undertryck av luteiniserande hormonnivåer av OHPC har också observerats hos kvinnor.
Glukokortikoidaktivitet
OHPC sägs inte ha någon glukokortikoid aktivitet. I enlighet med detta har OHPC visat sig inte förändra kortisolnivåer hos människor även med mycket höga doser genom intramuskulär injektion. Detta är av relevans eftersom läkemedel med betydande glukokortikoidaktivitet undertrycker kortisolnivåer på grund av ökad negativ feedback på hypotalamus -hypofysen -binjuraxeln . OHPC har studerats hos människor i doser så höga som 5000 mg per vecka genom intramuskulär injektion, med säkerhet och utan glukokortikoideffekter observerade. Läkemedlet interagerar dock med glukokortikoidreceptorn ; den har cirka 4% av dexametasonens affinitet för kaninens glukokortikoidreceptor. Men den fungerar som en partiell agonist för receptorn och har ingen större effekt än progesteron för att aktivera receptorn och framkalla associerat genuttryck in vitro .
Andra aktiviteter
Som ett rent gestagen har OHPC ingen androgen , antiandrogen , östrogen eller glukokortikoid aktivitet. Frånvaron av androgen och antiandrogen aktivitet med OHPC står i kontrast till de flesta andra 17α -hydroxiprogesteron -derivativa progestiner. På grund av dess brist på androgena egenskaper, på samma sätt som progesteron, har OHPC inga teratogena effekter på fostret , vilket gör det säkert att använda under graviditeten . Även om OHPC har beskrivits som ett rent gestagen, finns det bevis för att det har viss antimineralokortikoid aktivitet, på samma sätt som progesteron och 17a-hydroxiprogesteron. Detta inkluderar kliniskt viktiga diuretiska effekter och reversering av östrogeninducerad vätskeretention och ödem . Till skillnad från progesteron förväntas OHPC och dess metaboliter inte interagera med icke-genomiska receptorer, såsom membranprogesteronreceptorer eller GABA A- receptorn . I enlighet med detta anses OHPC inte ha neurosteroidaktiviteter av progesteron eller dess associerade lugnande effekter.
I samband med cytokrom P450 -enzymer har OHPC ingen effekt på CYP1A , CYP2D6 , CYP2C9 eller CYP3A4 , men är en blygsam inducerare av CYP2C19 .
Skillnader från progesteron
Det finns farmakodynamiska skillnader mellan progesteron och OHPC, vilket kan ha konsekvenser för obstetrisk användning. Dessa inkluderar:
- Minskad myometrial aktivitet med progesteron in vitro men ingen effekt eller ökad myometrial aktivitet med OHPC
- Förebyggande av livmoderhalsmognad med progesteron men okänd effekt med OHPC
- En icke-signifikant ökad dödfödelse och missfall med OHPC (i en studie)
- En möjligen ökad förekomst av graviditetsdiabetes med OHPC (ökad i två studier, ingen skillnad i en studie) men ingen sådan effekt med progesteron
- En signifikant ökad risk för perinatala biverkningar som fosterskada och för tidig förlossning vid flera graviditeter med OHPC (i två studier)
Skillnader i metabolismen av progesteron och OHPC och skillnader i bildning och aktivitet av metaboliter kan vara ansvariga för eller involverade i dessa observerade biologiska och farmakologiska skillnader. Progesteron metaboliseras av 5α- och 5β-reduktaser , 3α- och 3β-hydroxysteroiddehydrogenaser och 20α- och 20β-hydroxysteroiddehydrogenas i olika vävnader . I målvävnader, särskilt livmoderhalsen och myometrium, reglerar dessa enzymer lokala progesteronkoncentrationer och kan aktivera eller inaktivera progesteronsignalering. Dessutom katalyserar dessa enzymer bildandet av metaboliter av progesteron såsom 5β-dihydroprogesteron och allopregnanolon , som signalerar genom sina egna icke-genomiska receptorer som membranprogesteronreceptorer och GABA A- receptorn och har sina egna viktiga effekter under graviditeten. Som exempel har 5β-dihydroprogesteron visat sig spela en viktig roll för att undertrycka myometriaktivitet medan allopregnanolon har kraftiga lugnande och bedövande effekter hos modern och särskilt fostret och är involverad i fostrets nervsystems utveckling . I motsats till progesteron metaboliseras inte OHPC av traditionella steroidtransformerande enzymer och metaboliseras istället uteslutande via oxidation vid caproates sidokedja av cytokrom P450- enzymer. Som sådan tros det inte ha samma vävnadsspecifika aktiverings- och inaktiveringsmönster som progesteron gör eller samma icke-genomiska åtgärder som progesteron och dess metaboliter besitter.
Ytterligare klinisk forskning förväntas ge ytterligare data för att klargöra frågan om säkerhet med OHPC. Det har i alla fall rekommenderats av American College of Obstetricians and Gynecologists att gravida kvinnor som behandlas med OHPC får råd om dess risker och fördelar.
Farmakokinetik
| Parameter | Singleton | Tvilling |
|---|---|---|
| C max (ng/ml) | 22,6 (15,8–27,4) | 17,3 (12–27) |
| C medelvärde (0 – t) (ng/ml) | 16,8 (12,8–22,7) | 12,3 (8,4–18,7) |
| C -tråg (ng/ml) | 14.1 (10–18.1) | 11,2 (4,8–16,3) |
| AUC 0 – t (ng/ml/dag) | 117,3 (89,9–159,1) | 86,1 (59–131) |
| t 1/2 (dagar) | 16,2 (10,6–21,0) | 10 (6–16) |
| T max (dagar) | 1,0 (1–3) | 1.2 (1–2) |
| V d / F (x 10 3 ) (L) | 56 (25,2–69,6) | 16,9 (9,1–24,5) |
| CL / F (x 10 3 ) (L) | 2.1 (1.5–2.7) | 1,2 (0,9–1,7) |
| Fotnoter: a = OHPC 250 mg en gång i veckan genom intramuskulär injektion. Källor: | ||
Absorption
Hos djur är biotillgängligheten för OHPC med intramuskulär injektion nästan 100%, men dess orala biotillgänglighet är mycket låg med mindre än 3%. Hos kvinnor har 70 mg/dag oralt OHPC liknande endometrial potens som 70 mg/dag oralt OHPA och 2,5 mg/dag oralt medroxiprogesteronacetat , vilket indikerar att oral OHPC och OHPA har nästan 30 gånger lägre styrka än medroxiprogesteronacetat via oral administrering. Studier av progestogena endometrialförändringar med oral OHPC hos kvinnor blandas emellertid, varav en fann svaga effekter med 100 mg/dag medan en annan fann att doser på 250 till 1000 mg inte gav några effekter. Som ett resultat av dess låga orala styrka har OHPC inte använts oralt och har istället administrerats genom intramuskulär injektion. En ny oral formulering av OHPC (utvecklingskodnamn LPCN-1107) är dock under utveckling och har visat sig vara effektiv, även om den krävde administrering två gånger om dagen i en klinisk studie.
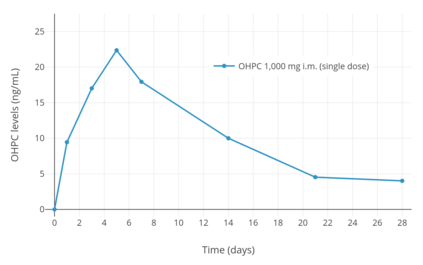
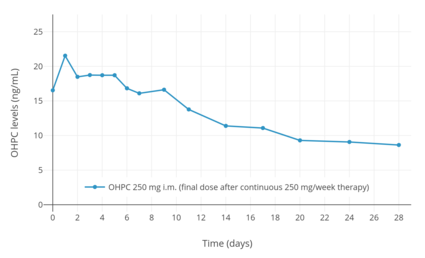
En depåeffekt uppstår när OHPC injiceras intramuskulärt eller subkutant , så att medicinen har en förlängd varaktighet av verkan . Efter en enda intramuskulär injektion av 1 000 mg OHPC hos fem kvinnor med endometriecancer var toppnivåerna för OHPC 27,8 ± 5,3 ng/ml och tiden till maximal koncentration var 4,6 ± 1,7 (3–7) dagar. Efter 13 veckors kontinuerlig administrering av 1 000 mg OHPC per vecka var lägsta nivåer av OHPC 60,0 ± 14 ng/ml. De farmakokinetiska parametrarna för 250 mg OHPC en gång i veckan genom intramuskulär injektion har också studerats hos gravida kvinnor med singleton och multipel (tvilling och triplett) graviditet. Steady state -nivåer av medicinen uppnås inom 4 till 12 veckor efter administrering hos gravida kvinnor. Varaktigheten av den kliniska biologiska effekten av OHPC genom intramuskulär injektion har också studerats hos kvinnor. En enda intramuskulär injektion av 65 till 500 mg OHPC i oljelösning har visat sig ha en verkningstid på 5 till 21 dagar när det gäller effekt i livmodern och kroppstemperaturen hos kvinnor.
OHPC har befunnits ha liknande farmakokinetik, inklusive toppnivåer , tid till toppnivåer , area-under-kurvan-nivåer (dvs total exponering) och elimineringshalveringstiden , med administrering via intramuskulär injektion eller subkutan autoinjection . Det fanns emellertid en högre incidens av smärta vid injektionsstället med subkutan autoinjection än med intramuskulär injektion (37,3% mot 8,2%).
Distribution
OHPC är i stor utsträckning bunden till plasmaproteiner , av vilka albumin ingår . Till skillnad från progesteron och 17α-hydroxiprogesteron har OHPC mycket låg affinitet för kortikosteroidbindande globulin (mindre än 0,01% av det för kortisol ). Progesteron och 17α-hydroxiprogesteron har låg affinitet för könshormonbindande globulin , och av detta skäl, är endast en mycket liten del av dem (mindre än 0,5%) bundet till detta protein i cirkulationen.
Ämnesomsättning
OHPC verkar metaboliseras främst av cytokrom P450 -enzymerna CYP3A4 och CYP3A5 . Det kan också metaboliseras av CYP3A7 i fostrets lever och moderkakan . Till skillnad från progesteron metaboliseras inte OHPC av traditionella steroidtransformerande enzymer och bildar inte liknande metaboliter . Metabolismen av OHPC sker genom reduktion , hydroxylering och konjugering , inklusive glukuronidering , sulfatering och acetylering . Den kaproat estern av OHPC klyvs inte under metabolism , så 17α-hydroxiprogesteron inte bildas från OHPC. Som sådan är OHPC inte ett prodrug av 17a-hydroxiprogesteron eller progesteron .
OHPC har visat sig ha en eliminationshalveringstid på 7,8 dagar när den ges genom intramuskulär injektion i en oljebaserad formulering till icke-gravida kvinnor. Dess totala varaktighet sägs vara 10 till 14 dagar, vilket är mycket längre än intramuskulärt administrerat progesteron i en oljeformulering (2 till 3 dagar). Hos gravida verkar halveringstiden för OHPC vara längre, cirka 16 eller 17 dagar. Hos kvinnor som är gravida med tvillingar snarare än en singel befanns emellertid halveringstiden för OHPC vara kortare än detta, vid 10 dagar. OHPC har upptäckts hos gravida kvinnor upp till 44 dagar efter den sista dosen.
Eliminering
OHPC är eliminerad 50% i feces och 30% i urinen då de ges genom intramuskulär injektion till gravida kvinnor. Både den fria steroiden och konjugaten utsöndras genom dessa vägar, med konjugaten mer framträdande i avföring.
Veterinär
Farmakokinetiken för OHPC hos olika hovdjur inklusive boskap, buffel, får och get har studerats.
Tid -koncentrationskurvor
Kemi
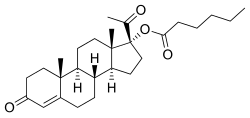
OHPC, även känd som 17α-hydroxiprogesteronkaproat eller som 17α-hydroxipregn-4-en-3,20-dion 17α-hexanoat, är en syntetisk pregnan steroid och ett derivat av progesteron . Det är specifikt ett derivat av 17a-hydroxiprogesteron med en hexanoat (kaproat) ester vid C17a-positionen. Analoger av OHPC innefatta andra 17α-hydroxiprogesteron derivat såsom algeston acetophenide (dihydroxyprogesterone acetophenide), klormadinonacetat , cyproteronacetat , hydroxiprogesteron-acetat , hydroxiprogesteron heptanoat , medroxiprogesteronacetat och megestrolacetat , liksom kaproat estrar klormadinon kaproat , gestonorone kaproat (norhydroxyprogesterone caproate), medroxiprogesteron caproate , megestrol caproate och methenmadinone caproate .
Syntes
Kemiska synteser av OHPC har beskrivits.
Historia
Tillsammans med hydroxiprogesteronacetat utvecklades OHPC av Karl Junkmann från Schering AG 1953 och rapporterades först av honom i medicinsk litteratur 1954. Det marknadsfördes enligt uppgift först i Japan 1954 eller 1955 och introducerades därefter som Delalutin i USA Stater 1956. På grund av sin mycket längre varaktighet än parenteralt progesteron hade OHPC i stort sett ersatt progesteron i klinisk praxis 1975. Efter decenniers användning tog Squibb , tillverkaren, frivilligt tillbaka Delalutin -produkten i USA 1999. Förnyat intresse för OHPC i USA tändes med en stor NIH-sponsrad studie 2003 som visade att OHPC minskade risken för för tidig födelse hos utvalda gravida kvinnor i riskzonen. Med uppföljningsdata visar inga tecken på skadliga effekter på avkomman, godkände FDA medicinen, som sponsras av KV Pharmaceutical som Makena , som särläkemedel i februari 2011 för att minska risken för tidig födsel hos kvinnor före 37 veckors graviditet med ett enda foster som hade minst en tidigare för tidig förlossning.
Samhälle och kultur
Generiska namn
Hydroxiprogesteron caproate är det generiska namnet på OHPC och dess INN , USAN , BANM och JAN , medan hydroxiprogesteronhexanoat var dess tidigare BANM .
OHPC är ofta felmärkt som och förväxlas med progesteron och 17a-hydroxiprogesteron . Det bör inte heller förväxlas med hydroxiprogesteronacetat , hydroxiprogesteronheptanoat eller medroxiprogesteronacetat .
Märkesnamn
OHPC marknadsförs över hela världen under en mängd olika varumärken, inklusive Proluton , Proluton Depot och Makena ( USA ), bland många andra. Det var också tidigare marknadsförs under varumärkena inklusive Delalutin , Prodrox och Hylutin bland andra, men dessa formuleringar har sedan dess upphört. Det har marknadsförs under varumärkena Gravibinon och injicerbara nr 1 (eller kinesiska Injicerbara nr 1) i kombination med estradiolvalerat och under varumärket Primosiston i kombination med östradiolbensoat .
Tillgänglighet
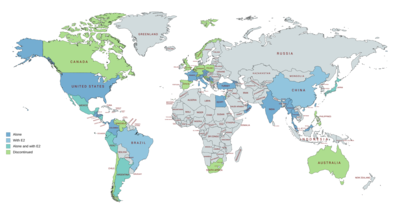
OHPC marknadsförs i USA och i hela Europa , Asien och Central- och Sydamerika . Det är särskilt tillgängligt inte i Kanada , Storbritannien , Nya Zeeland eller Sydafrika , och endast veterinärmedicinska preparat är tillgängliga i Australien . OHPC marknadsförs också i kombination med östradiolvalerat som ett kombinerat injicerbart preventivmedel i ett antal länder, inklusive i Sydamerika , Mexiko , Japan och Kina . Det har marknadsförts som ett injicerbart preparat i kombination med östradiolbensoat i vissa länder också.
Prisstrid
Med utnämningen av OHPC som särläkemedel av FDA och godkännande av Makena 2011 var priset på OHPC i USA kommer att öka från US $ 15 till US $ 1500 för en enda dos, eller från ca US $ 300 till mellan USA 25 000 dollar och 30 000 dollar för en typisk behandlingsmånad. Detta var ungefär en 100-faldig kostnadsökning, med "minimal extra klinisk nytta", och var en starkt kritiserad prisstrategi . FDA meddelade senare att compounding apotek skulle kunna fortsätta att sälja OHPC på sin vanliga kostnad på cirka US $ 10 till US $ 20 per dos utan rädsla för rättsliga repressalier. KV Pharmaceutical valde också att sänka sitt pris på Makena till 690 dollar per dos. OHPC fortsatte att vara tillgängligt till låg kostnad från sammansatta apotek till slutet av 2016, varefter FDA publicerade nya vägledningsdokument som förbjöd sammansatta apotek att sälja produkter som "i huvudsak är kopior" av kommersiellt tillgängliga läkemedelsprodukter.
Forskning
Cyklisk terapi med 150 mg OHPC genom intramuskulär injektion befanns vara effektiva vid behandling av 76 kvinnor med ihållande, behandlingsresistent akne i en preliminär studie, med 84% som svarar på terapi och upplever en "bra-att-utmärkt" förbättring i symptom.
OHPC studerades genom Schering för användning som ett progestogen-bara injicerbara preventivmedel i en dos av 250 till 500 mg en gång i månaden genom intramuskulär injektion men produceras dålig cykelkontroll vid dessa doser och var aldrig marknadsföras.
OHPC i sig har visat sig ha liten eller ingen effektivitet vid behandling av bröstcancer hos kvinnor. Omvänt, kombinationen av estradiolvalerat har och OHPC visat sig vara effektiva vid behandling av bröstcancer hos kvinnor. Initial forskning baserad på begränsade kliniska data rapporterade att svarsfrekvensen för bröstcancer med en kombination av östradiolvalerat och OHPC verkade vara större än med enbart östrogen (35% mot 50%). Men senare forskning med tillhörande men mer potent progestin gestonorone caproate fann att kombinationen av estradiolvalerat och gestonorone kaproat hade effektivitet som inte var signifikant skiljer sig från en enbart östrogen vid behandling av bröstcancer hos kvinnor.
En ny oral formulering av OHPC (utvecklings kodnamnet LPCN-1107) är under utveckling för att förebygga tidig förlossning . Från och med september 2017 är det i fas II eller fas III kliniska prövningar för denna indikation.
Se även
- Estradiolvalerat/hydroxiprogesteronkaprat
- Estradiolbensoat/hydroxiprogesteronkaprat
- Estradiol dipropionat/hydroxiprogesteron caproate
Referenser
Vidare läsning
- Meis PJ (maj 2005). "17 hydroxiprogesteron för förebyggande av för tidig leverans". Obstetrik och gynekologi . 105 (5 punkter 1): 1128–35. doi : 10.1097/01.AOG.0000160432.95395.8f . PMID 15863556 .
- Facchinetti F, Vaccaro V (oktober 2009). "Farmakologisk användning av progesteron och 17-alfa-hydroxiprogesteron kaproat för att förhindra för tidig leverans". Minerva Ginecologica . 61 (5): 401–9. PMID 19749671 .
- Deeks ED (oktober 2011). "17 α-Hydroxyprogesteron caproate (Makena ™): för att förebygga för tidig födsel". Barnläkemedel . 13 (5): 337-45. doi : 10.2165/11208140-000000000-00000 . PMID 21888448 . S2CID 207297651 .
- Merlob P, Stahl B, Klinger G (januari 2012). "17α Hydroxiprogesteron caproate för förebyggande av återkommande spontan för tidig förlossning". Reproduktionstoxikologi . 33 (1): 15–9. doi : 10.1016/j.reprotox.2011.10.017 . PMID 22120850 .
- O'Brien JM (oktober 2012). "Säkerheten för progesteron och 17-hydroxiprogesteron kaproat administrering för att förebygga för tidig födsel: en evidensbaserad bedömning". American Journal of Perinatology . 29 (9): 665–72. doi : 10.1055/s-0032-1316444 . PMID 22773279 .
- Romero R, Stanczyk FZ (juni 2013). "Progesteron är inte samma sak som 17α-hydroxiprogesteron caproate: konsekvenser för obstetrisk praxis" . American Journal of Obstetrics and Gynecology . 208 (6): 421–6. doi : 10.1016/j.ajog.2013.04.027 . PMC 4120746 . PMID 23643669 .
- Feghali M, Venkataramanan R, Caritis S (december 2014). "Förebyggande av för tidig leverans med 17-hydroxiprogesteronkaprat: farmakologiska överväganden" . Seminarier i perinatologi . 38 (8): 516–22. doi : 10.1053/j.semperi.2014.08.013 . PMC 4253874 . PMID 25256193 .
- Saccone G, Suhag A, Berghella V (juli 2015). "17-alfa-hydroxiprogesteron kaproat för underhållstokolys: en systematisk granskning och metaanalys av randomiserade försök". American Journal of Obstetrics and Gynecology . 213 (1): 16–22. doi : 10.1016/j.ajog.2015.01.054 . PMID 25659469 .
- O'Brien JM, Lewis DF (januari 2016). "Förebyggande av för tidig födsel med vaginalt progesteron eller 17-alfa-hydroxiprogesteronkaproat: en kritisk undersökning av effekt och säkerhet". American Journal of Obstetrics and Gynecology . 214 (1): 45–56. doi : 10.1016/j.ajog.2015.10.934 . PMID 26558340 .
- Caritis SN, Feghali MN, Grobman WA, Rouse DJ (augusti 2016). "Vad vi har lärt oss om rollen som 17-alfa-hydroxiprogesteron kaproat i förebyggande av för tidig förlossning" . Seminarier i perinatologi . 40 (5): 273–80. doi : 10.1053/j.semperi.2016.03.002 . PMC 4983195 . PMID 27105940 .
- Saccone G, Khalifeh A, Elimian A, Bahrami E, Chaman-Ara K, Bahrami MA, Berghella V (mars 2017). "Vaginal progesteron vs intramuskulär 17α-hydroxiprogesteron kaproat för förebyggande av återkommande spontan för tidig födsel i singleton-graviditeter: systematisk granskning och metaanalys av randomiserade kontrollerade studier" . Ultraljud i obstetrik och gynekologi . 49 (3): 315–321. doi : 10.1002/uog.17245 . PMID 27546354 . S2CID 11.445.977 .
- Oler E, Eke AC, Hesson A (juli 2017). "Metaanalys av randomiserade kontrollerade studier som jämför 17a-hydroxiprogesteronkaprat och vaginal progesteron för att förebygga återkommande spontan för tidig leverans". International Journal of Gynecology and Obstetrics . 138 (1): 12–16. doi : 10.1002/ijgo.12166 . HDL : 2027,42 / 137.297 . PMID 28369874 . S2CID 24480427 .
- Manuck TA (december 2017). "17-alfa hydroxiprogesteron caproate för förebyggande förebyggande av förlossning: Var har vi varit, hur kom vi hit och vart tar vi vägen?". Seminarier i perinatologi . 41 (8): 461–467. doi : 10,1053 / j.semperi.2017.08.004 . PMID 28.947.068 .