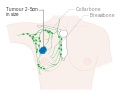
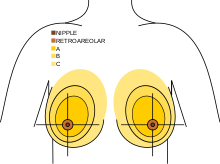
Bröstcancer -Breast cancer
| Bröstcancer | |
|---|---|
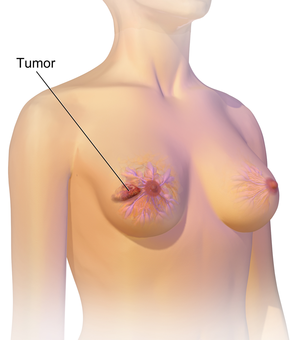 | |
| En illustration av bröstcancer | |
| Specialitet | Onkologi |
| Symtom | En knöl i ett bröst, en förändring i bröstform, gropar i huden, vätska från bröstvårtan, en nyligen vänt bröstvårtan, en röd fjällande hudfläck på bröstet |
| Riskfaktorer | Att vara kvinna, fetma , brist på motion, alkohol, hormonersättningsterapi under klimakteriet , joniserande strålning , tidig ålder vid första menstruationen , få barn sent i livet eller inte alls, högre ålder, tidigare bröstcancer, familjehistoria av bröstcancer, Klinefelter syndrom |
| Diagnostisk metod | Vävnadsbiopsi Mammografi |
| Behandling | Kirurgi, strålbehandling , kemoterapi , hormonbehandling , riktad terapi |
| Prognos | Femårsöverlevnad ≈85 % (USA, Storbritannien) |
| Frekvens | 2,2 miljoner drabbade (globalt, 2020) |
| Dödsfall | 685 000 (globalt, 2020) |
Bröstcancer är cancer som utvecklas från bröstvävnad . Tecken på bröstcancer kan vara en knöl i bröstet, en förändring i bröstform, gropar i huden, mjölkavstötning , vätska som kommer från bröstvårtan , en nyligen vänd bröstvårta eller en röd eller fjällande hudfläck. Hos personer med avlägsen spridning av sjukdomen kan det finnas skelettsmärta , svullna lymfkörtlar , andnöd eller gul hud .
Riskfaktorer för att utveckla bröstcancer inkluderar fetma , brist på fysisk träning , alkoholism , hormonersättningsterapi under klimakteriet , joniserande strålning , tidig ålder vid första menstruationen , att få barn sent i livet eller inte alls, högre ålder, ha en tidigare historia av bröstcancer och en familjehistoria av bröstcancer. Cirka 5–10 % av fallen är resultatet av en ärftlig genetisk predisposition, inklusive BRCA-mutationer bland annat. Bröstcancer utvecklas oftast i celler från slemhinnan i mjölkkanalerna och lobulerna som förser dessa kanaler med mjölk. Cancer som utvecklas från kanalerna är kända som duktala karcinom , medan de som utvecklas från lobuli är kända som lobulära karcinom . Det finns mer än 18 andra undertyper av bröstcancer. Vissa, såsom duktalt karcinom in situ , utvecklas från pre-invasiva lesioner . Diagnosen bröstcancer bekräftas genom att ta en biopsi av den berörda vävnaden. När diagnosen har ställts görs ytterligare tester för att avgöra om cancern har spridit sig utanför bröstet och vilka behandlingar som är mest sannolikt att vara effektiva.
Balansen mellan fördelar och skador av bröstcancerscreening är kontroversiell. En Cochrane-granskning från 2013 fann att det var oklart om mammografisk screening gör mer skada än nytta, eftersom en stor andel kvinnor som testar positivt visar sig inte ha sjukdomen. En granskning från 2009 för US Preventive Services Task Force fann bevis på nytta hos dessa 40 till 70 år, och organisationen rekommenderar screening vartannat år hos kvinnor i åldern 50 till 74 år. Läkemedlen tamoxifen eller raloxifen kan användas i ett försök att förebygga bröstcancer hos dem som löper hög risk att utveckla den. Kirurgiskt avlägsnande av båda brösten är en annan förebyggande åtgärd hos vissa högriskkvinnor. Hos dem som har diagnostiserats med cancer kan ett antal behandlingar användas, inklusive kirurgi, strålbehandling , kemoterapi , hormonell terapi och riktad terapi . Typer av operationer varierar från bröstbevarande operation till mastektomi . Bröstrekonstruktion kan ske vid operationstillfället eller vid ett senare tillfälle. Hos dem där cancern har spridit sig till andra delar av kroppen syftar behandlingar mestadels till att förbättra livskvalitet och komfort.
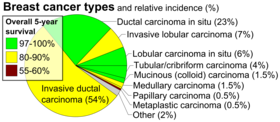
Utfall för bröstcancer varierar beroende på cancertyp, sjukdomens omfattning och personens ålder. Femårsöverlevnaden i England och USA är mellan 80 och 90% . I utvecklingsländer är femårsöverlevnaden lägre. Över hela världen är bröstcancer den ledande cancerformen hos kvinnor och står för 25 % av alla fall. Under 2018 resulterade det i 2 miljoner nya fall och 627 000 dödsfall. Det är vanligare i utvecklade länder och är mer än 100 gånger vanligare hos kvinnor än hos män .
tecken och symtom
Bröstcancer uppträder oftast som en knöl som känns annorlunda än resten av bröstvävnaden. Mer än 80% av fallen upptäcks när en person upptäcker en sådan knöl med fingertopparna. De tidigaste bröstcancerfallen upptäcks dock med mammografi . Klumpar som finns i lymfkörtlar i armhålorna kan också indikera bröstcancer.
Andra indikationer på bröstcancer än en knöl kan vara förtjockning som skiljer sig från den andra bröstvävnaden, ett bröst som blir större eller lägre, en bröstvårta som ändrar position eller form eller blir inverterad, hud som rynkar sig eller gropar, utslag på eller runt bröstvårtan, flytningar från bröstvårtor, konstant smärta i delar av bröstet eller armhålan och svullnad under armhålan eller runt nyckelbenet. Smärta (" mastodyni ") är ett opålitligt verktyg för att fastställa förekomsten eller frånvaron av bröstcancer, men kan vara ett tecken på andra brösthälsoproblem .
Ett annat symptomkomplex av bröstcancer är Pagets bröstsjukdom . Detta syndrom uppträder som hudförändringar som liknar eksem; såsom rodnad, missfärgning eller mild flagning av bröstvårtans hud. När Pagets sjukdom i bröstet utvecklas kan symtom innefatta stickningar, klåda, ökad känslighet, sveda och smärta. Det kan också finnas flytningar från bröstvårtan. Ungefär hälften av kvinnorna som diagnostiserats med Pagets bröstsjukdom har också en knöl i bröstet.
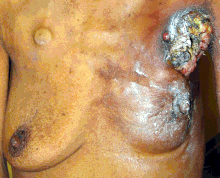
Inflammatorisk bröstcancer är en sällsynt (visas bara i mindre än 5 % av bröstcancerdiagnoserna) men ändå aggressiv form av bröstcancer som kännetecknas av de svullna, röda områdena som bildas på toppen av bröstet. De visuella effekterna av inflammatorisk bröstcancer är ett resultat av en blockering av lymfkärl av cancerceller. Denna typ av bröstcancer ses i vanligare diagnosen i yngre åldrar, överviktiga kvinnor och afroamerikanska kvinnor. Eftersom inflammatorisk bröstcancer inte uppträder som en knöl kan det ibland bli en fördröjning av diagnosen.
Bröstsekretorisk karcinom (MSC) är en sällsynt form av sekretorisk karcinom som uteslutande förekommer i bröstet. Det utvecklas vanligtvis hos vuxna men drabbar i en betydande andel av fallen även barn: MSC står för 80 % av all bröstcancer hos barn. MSC-lesioner är vanligtvis långsamt växande, smärtfria, små ductala brösttumörer som har invaderat vävnaden runt deras ursprungskanaler , ofta spridit sig till sentinellymfkörtlar och/eller axillära lymfkörtlar , men sällan metastaserat till avlägsna vävnader. Dessa tumörer har typiskt distinkta mikroskopiska egenskaper och tumörceller som bär en balanserad genetisk translokation där en del av NTRK3 -genen smälts samman med en del av ETV6 -genen för att bilda en fusionsgen , ETV6-NTRK3 . Denna fusionsgen kodar för ett chimärt protein som kallas ETV6-NTRK3. NTRK3-delen av ETV6-NTRK3-proteinet har uppreglerad tyrosinkinasaktivitet som stimulerar två signalvägar , PI3K/AKT/mTOR- och MAPK/ERK-vägarna , som främjar cellproliferation och överlevnad och därigenom kan bidra till utvecklingen av MSC. Konservativ kirurgi, modifierad radikal mastektomi och radikal mastektomi har varit de vanligaste ingreppen som används för att behandla vuxna, medan enkel mastektomi, lokal excision med sentinel lymfkörtelbiopsi och fullständig axillär dissektion har rekommenderats för att behandla barn med MSC. I samtliga fall, långvariga, t ex >20 år, rekommenderas uppföljningsundersökningar. De relativt sällsynta fallen av MSC som har metastaserat till avlägsna vävnader har visat få eller inga svar på kemoterapi och strålbehandling. Tre patienter med metastaserande sjukdom hade goda partiella svar på Entrectinib , ett läkemedel som hämmar tyrosinkinasaktiviteten hos fusionsproteinet ETV6-NTRK3. På grund av dess långsamma tillväxt och låga metastaser till avlägsna vävnader har individer med MSC haft 20 års överlevnadsfrekvens på 93,16 %.
I sällsynta fall kan det som initialt ser ut som ett fibroadenom (hård, rörlig icke-cancerös knöl) i själva verket vara en phyllodestumör . Phyllodes tumörer bildas i stroma (bindväv) i bröstet och innehåller körtelvävnad såväl som stromal vävnad. Phyllodes-tumörer är inte iscensatta i vanlig mening; de klassificeras på grundval av deras utseende under mikroskopet som godartade, borderline eller maligna.
Maligna tumörer kan resultera i metastaserande tumörer – sekundära tumörer (som härrör från den primära tumören) som sprider sig utanför ursprungsplatsen. Symtomen som orsakas av metastaserad bröstcancer beror på platsen för metastasen. Vanliga metastaser inkluderar ben, lever, lunga och hjärna. När cancer har nått ett sådant invasivt tillstånd, kategoriseras den som en cancer i stadium 4, cancer i detta tillstånd är ofta dödlig. Vanliga symtom på cancer i stadium 4 inkluderar oförklarlig viktminskning, ben- och ledvärk, gulsot och neurologiska symtom. Dessa symtom kallas ospecifika symtom eftersom de kan vara manifestationer av många andra sjukdomar. I sällsynta fall kan bröstcancer spridas till ytterst ovanliga platser såsom lymfkörtlar i bukspottkörteln, vilket orsakar gallvägsobstruktion, vilket leder till diagnostiska svårigheter.
De flesta symtom på bröstsjukdomar, inklusive de flesta knölar, visar sig inte representera underliggande bröstcancer. Mindre än 20 % av knölarna är till exempel cancer, och godartade bröstsjukdomar som mastit och fibroadenom i bröstet är vanligare orsaker till symtom på bröstsjukdomar.
Riskfaktorer
Riskfaktorer kan delas in i två kategorier:
- modifierbara riskfaktorer (saker som människor kan förändra själva, såsom konsumtion av alkoholhaltiga drycker), och
- fasta riskfaktorer (saker som inte går att ändra, såsom ålder och fysiologiskt kön).
De primära riskfaktorerna för bröstcancer är kvinnlig och äldre ålder. Andra potentiella riskfaktorer inkluderar genetik, brist på barnafödande eller brist på amning, högre nivåer av vissa hormoner, vissa kostmönster och fetma. En studie indikerar att exponering för ljusföroreningar är en riskfaktor för utveckling av bröstcancer.
Om alla vuxna bibehöll den hälsosammaste möjliga livsstilen, inklusive att inte dricka alkoholhaltiga drycker , bibehålla en hälsosam kroppssammansättning , aldrig röka , äta hälsosam mat och andra åtgärder, skulle nästan en fjärdedel av fallen av bröstcancer i världen kunna förhindras. De återstående tre fjärdedelarna av fallen av bröstcancer kan inte förebyggas genom livsstilsförändringar.
Livsstil

Att dricka alkoholhaltiga drycker ökar risken för bröstcancer, även bland mycket lätta alkoholkonsumenter (kvinnor som dricker mindre än hälften av en alkoholdryck per dag). Risken är högst bland storkonsumenter. Globalt sett orsakas ungefär ett av tio fall av bröstcancer av kvinnor som dricker alkoholhaltiga drycker. Att dricka alkoholhaltiga drycker är bland de vanligaste modifierbara riskfaktorerna.
Korrelationen mellan fetma och bröstcancer är allt annat än linjär. Studier visar att de som snabbt går upp i vikt i vuxen ålder löper högre risk än de som varit överviktiga sedan barndomen. Likaså verkar överflödigt fett i mittsektionen inducera en högre risk än övervikt som bärs i underkroppen. Detta innebär att maten man äter är viktigare än ens BMI . Kostfaktorer som kan öka risken inkluderar en fettrik kost och fetmarelaterade höga kolesterolnivåer . Jodbrist i kosten kan också spela en roll. Bevis för fiber är oklara. En granskning från 2015 visade att studier som försökte koppla fiberintag med bröstcancer gav blandade resultat. Under 2016 observerades ett preliminärt samband mellan lågt fiberintag under tonåren och bröstcancer.
Att röka tobak tycks öka risken för bröstcancer, med ju större mängd rökt och ju tidigare i livet som rökningen började, desto högre risk. Hos dem som är långtidsrökare ökar den relativa risken med 35 % till 50 %.
Brist på fysisk aktivitet har kopplats till cirka 10 % av fallen. Att sitta regelbundet under längre perioder är förknippat med högre dödlighet i bröstcancer. Risken förnekas inte av regelbunden träning, även om den sänks.
Hormonbehandling för att behandla klimakteriet är också associerad med en ökad risk för bröstcancer. Användningen av hormonell preventivmedel orsakar inte bröstcancer för de flesta kvinnor; om den har en effekt är den liten (i storleksordningen 0,01 % per användare-år; jämförbar med mödradödligheten i USA), tillfällig och uppvägd av användarnas signifikant minskade risk för äggstockscancer och endometriecancer . Bland dem med en familjehistoria av bröstcancer verkar användningen av moderna p-piller inte påverka risken för bröstcancer. Det är mindre säkert om hormonella preventivmedel kan öka den redan höga andelen bröstcancer hos kvinnor med mutationer i bröstcancermottaglighetsgenerna BRCA1 eller BRCA2 .
Amning minskar risken för flera typer av cancer, inklusive bröstcancer. På 1980-talet ansåg abort-bröstcancerhypotesen att inducerad abort ökade risken för att utveckla bröstcancer. Denna hypotes var föremål för omfattande vetenskaplig undersökning, som drog slutsatsen att varken missfall eller aborter är förknippade med en ökad risk för bröstcancer.
Andra riskfaktorer inkluderar strålning och dygnsstörningar relaterade till skiftarbete och rutinätande sent på kvällen. Ett antal kemikalier har också kopplats samman, inklusive polyklorerade bifenyler , polycykliska aromatiska kolväten och organiska lösningsmedel Även om strålningen från mammografi är en låg dos, uppskattas det att årlig screening från 40 till 80 års ålder kommer att orsaka cirka 225 dödsfall bröstcancer per miljon screenade kvinnor.
Genetik
Genetik tros vara den primära orsaken till 5–10 % av alla fall. Kvinnor vars mamma fick diagnosen före 50 har en ökad risk på 1,7 och de vars mamma fick diagnosen vid 50 års ålder eller senare har en ökad risk på 1,4. Hos de med noll, en eller två drabbade släktingar är risken för bröstcancer före 80 års ålder 7,8 %, 13,3 % och 21,1 % med en efterföljande dödlighet i sjukdomen på 2,3 %, 4,2 % respektive 7,6 %. Hos dem med en första gradens släkting med sjukdomen är risken för bröstcancer mellan 40 och 50 år dubbelt så stor som för den allmänna befolkningen.
I mindre än 5 % av fallen spelar genetik en mer betydande roll genom att orsaka ett ärftligt bröst-äggstockscancersyndrom . Detta inkluderar de som bär på genmutationen BRCA1 och BRCA2 . Dessa mutationer står för upp till 90 % av den totala genetiska påverkan med en risk för bröstcancer på 60–80 % hos de drabbade. Andra betydande mutationer inkluderar p53 ( Li-Fraumeni syndrom ), PTEN ( Cowden syndrom ) och STK11 ( Peutz-Jeghers syndrom ), CHEK2 , ATM , BRIP1 och PALB2 . År 2012 sa forskare att det finns fyra genetiskt distinkta typer av bröstcancer och att i varje typ leder genetiska förändringar till många cancerformer.
Andra genetiska anlag inkluderar bröstvävnadens täthet och hormonella nivåer. Kvinnor med tät bröstvävnad är mer benägna att få tumörer och är mindre benägna att få diagnosen bröstcancer – eftersom den täta vävnaden gör tumörer mindre synliga på mammografi. Dessutom löper kvinnor med naturligt höga östrogen- och progesteronnivåer också högre risk för tumörutveckling.
Medicinska tillstånd
Bröstförändringar som atypisk duktal hyperplasi och lobulärt karcinom in situ , som finns vid benigna brösttillstånd som fibrocystiska bröstförändringar , är korrelerade med en ökad risk för bröstcancer.
Diabetes mellitus kan också öka risken för bröstcancer. Autoimmuna sjukdomar som lupus erythematosus verkar också öka risken för att få bröstcancer.
De främsta orsakerna till sporadisk bröstcancer är förknippade med hormonnivåer. Bröstcancer främjas av östrogen. Detta hormon aktiverar utvecklingen av bröst under puberteten, menstruationscyklerna och graviditeten. Obalansen mellan östrogen och progesteron under menstruationsfaserna orsakar cellproliferation. Dessutom kan oxidativa metaboliter av östrogen öka DNA-skador och mutationer. Upprepad cykling och försämring av reparationsprocessen kan omvandla en normal cell till premaligna och så småningom maligna celler genom mutation. Under det premaligna stadiet kan hög proliferation av stromaceller aktiveras av östrogen för att stödja utvecklingen av bröstcancer. Under ligandbindningsaktiveringen kan ER reglera genuttryck genom att interagera med östrogensvarselement inom promotorn av specifika gener. Uttrycket och aktiveringen av ER på grund av brist på östrogen kan stimuleras av extracellulära signaler. Intressant nog kan ER som direkt binder till flera proteiner, inklusive tillväxtfaktorreceptorer, främja uttrycket av gener relaterade till celltillväxt och överlevnad.
Förhöjda prolaktinnivåer i blodet är associerade med ökad risk för bröstcancer. En metaanalys av observationsforskning med över två miljoner individer har föreslagit ett måttligt samband mellan antipsykotisk användning och bröstcancer, möjligen förmedlad av prolaktininducerande egenskaper hos specifika medel.
Patofysiologi
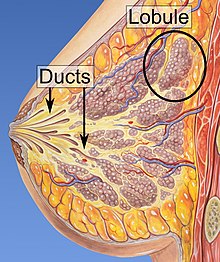

Bröstcancer, liksom andra cancerformer , uppstår på grund av en interaktion mellan en miljöfaktor (extern) och en genetiskt mottaglig värd. Normala celler delar sig så många gånger som behövs och stannar. De fäster vid andra celler och stannar på plats i vävnader. Celler blir cancerösa när de förlorar sin förmåga att sluta dela sig, att fästa sig vid andra celler, att stanna där de hör hemma och att dö vid rätt tidpunkt.
Normala celler kommer att självförstöra ( programmerad celldöd ) när de inte längre behövs. Fram till dess är celler skyddade från programmerad död av flera proteinkluster och vägar. En av de skyddande vägarna är PI3K / AKT -vägen; en annan är RAS / MEK / ERK -vägen. Ibland muteras generna längs dessa skyddsvägar på ett sätt som gör dem permanent "på", vilket gör cellen oförmögen att självförstöra när den inte längre behövs. Detta är ett av stegen som orsakar cancer i kombination med andra mutationer. Normalt stänger PTEN -proteinet av PI3K/AKT-vägen när cellen är redo för programmerad celldöd. I vissa bröstcancer är genen för PTEN-proteinet muterad, så PI3K/AKT-vägen sitter fast i "på"-läget och cancercellen förstör inte själv.
Mutationer som kan leda till bröstcancer har experimentellt kopplats till östrogenexponering. Dessutom har G-proteinkopplade östrogenreceptorer associerats med olika cancerformer i det kvinnliga reproduktionssystemet inklusive bröstcancer.
Onormal tillväxtfaktorsignalering i interaktionen mellan stromaceller och epitelceller kan underlätta maligna celltillväxt. I bröstfettvävnad leder överuttryck av leptin till ökad cellproliferation och cancer.
I USA har 10 till 20 procent av kvinnorna med bröstcancer eller äggstockscancer en släkting i första eller andra graden med en av dessa sjukdomar. Män med bröstcancer har en ännu högre sannolikhet. Den familjära tendensen att utveckla dessa cancerformer kallas ärftligt bröst–äggstockscancersyndrom . Den mest kända av dessa, BRCA- mutationerna , ger en livstidsrisk för bröstcancer på mellan 60 och 85 procent och en livstidsrisk för äggstockscancer på mellan 15 och 40 procent. Vissa mutationer associerade med cancer, såsom p53 , BRCA1 och BRCA2 , förekommer i mekanismer för att korrigera fel i DNA . Dessa mutationer är antingen ärvda eller förvärvade efter födseln. Förmodligen tillåter de ytterligare mutationer, vilket möjliggör okontrollerad delning, brist på fäste och metastasering till avlägsna organ. Det finns dock starka bevis för kvarvarande riskvariation som går långt utöver ärftliga BRCA- genmutationer mellan bärarfamiljer. Detta orsakas av oobserverade riskfaktorer. Detta implicerar miljömässiga och andra orsaker som triggers för bröstcancer. Den ärvda mutationen i BRCA1- eller BRCA2 -gener kan störa reparation av DNA-tvärlänkar och DNA-dubbelsträngsbrott (kända funktioner hos det kodade proteinet). Dessa cancerframkallande ämnen orsakar DNA-skador som DNA-tvärbindningar och dubbelsträngsbrott som ofta kräver reparationer via vägar som innehåller BRCA1 och BRCA2. Men mutationer i BRCA- gener står för endast 2 till 3 procent av alla bröstcancerfall. Levin et al. säga att cancer kanske inte är oundviklig för alla bärare av BRCA1- och BRCA2 -mutationer. Ungefär hälften av ärftliga bröst-äggstockscancersyndrom involverar okända gener. Dessutom kan vissa latenta virus minska uttrycket av BRCAl -genen och öka risken för brösttumörer.
GATA-3 styr direkt uttrycket av östrogenreceptorn (ER) och andra gener associerade med epitelial differentiering, och förlusten av GATA-3 leder till förlust av differentiering och dålig prognos på grund av cancercellsinvasion och metastaser.
Diagnos
De flesta typer av bröstcancer är lätta att diagnostisera genom mikroskopisk analys av ett prov – eller biopsi – av det drabbade området av bröstet. Det finns också typer av bröstcancer som kräver specialiserade labbundersökningar.
De två vanligaste screeningmetoderna, fysisk undersökning av brösten av en vårdgivare och mammografi, kan erbjuda en ungefärlig sannolikhet för att en knöl är cancer, och kan även upptäcka några andra lesioner, såsom en enkel cysta . När dessa undersökningar inte är avgörande kan en vårdgivare ta bort ett prov av vätskan i klumpen för mikroskopisk analys (ett förfarande som kallas finnålsaspiration eller finnålsaspiration och cytologi, FNAC) för att fastställa diagnosen. En nålspiration kan utföras på en vårdgivares kontor eller klinik. En lokalbedövning kan användas för att bedöva bröstvävnaden för att förhindra smärta under ingreppet, men kanske inte nödvändigt om klumpen inte är under huden. Ett fynd av klar vätska gör att klumpen är högst osannolik att vara cancer, men blodig vätska kan skickas iväg för inspektion under ett mikroskop för cancerceller. Tillsammans kan fysisk undersökning av brösten, mammografi och FNAC användas för att diagnostisera bröstcancer med en god grad av noggrannhet.
Andra alternativ för biopsi inkluderar en kärnbiopsi eller vakuumassisterad bröstbiopsi, som är procedurer där en del av bröstklumpen tas bort; eller en excisionsbiopsi , där hela klumpen avlägsnas. Mycket ofta är resultaten av fysisk undersökning av en vårdgivare, mammografi och ytterligare tester som kan utföras under speciella omständigheter (såsom ultraljudsundersökning eller MRI ) tillräckliga för att motivera excisionsbiopsi som den definitiva diagnostiska och primära behandlingsmetoden.
Utskuren mänsklig bröstvävnad , som visar ett oregelbundet, tätt, vitt stjärnområde av cancer 2 cm i diameter, inom gul fettvävnad
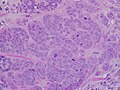
Höggradigt invasivt duktalt karcinom, med minimal tubulibildning, markerad pleomorfism och framträdande mitoser , 40x fält
Mammografi som visar ett normalt bröst (vänster) och ett bröst med cancer (höger)
Klassificering
Bröstcancer klassificeras av flera betygssystem. Var och en av dessa påverkar prognosen och kan påverka behandlingssvaret. Beskrivning av en bröstcancer inkluderar optimalt alla dessa faktorer.
- Histopatologi . Bröstcancer klassificeras vanligtvis främst efter dess histologiska utseende. De flesta bröstcancer härrör från epitelet som täcker kanalerna eller lobulierna, och dessa cancerformer klassificeras som duktalt eller lobulärt karcinom. Carcinom in situ är tillväxt av låggradiga cancerceller eller precancerösa celler i ett speciellt vävnadsutrymme såsom bröstkanalen utan invasion av den omgivande vävnaden. Däremot begränsar sig inte invasivt karcinom till det initiala vävnadsutrymmet.
- Betyg . Gradering jämför utseendet på bröstcancercellerna med utseendet på normal bröstvävnad. Normala celler i ett organ som bröstet blir differentierade, vilket innebär att de antar specifika former och former som återspeglar deras funktion som en del av det organet. Cancerceller förlorar den differentieringen. Vid cancer blir de celler som normalt skulle radas upp på ett ordnat sätt för att utgöra mjölkkanalerna oorganiserade. Celldelningen blir okontrollerad. Cellkärnor blir mindre enhetliga. Patologer beskriver celler lika väl differentierade (låg grad), måttligt differentierade (mellanklass) och dåligt differentierade (hög grad) eftersom cellerna progressivt förlorar de egenskaper som ses i normala bröstceller. Dåligt differentierade cancerformer (de vars vävnad är minst lik normal bröstvävnad) har en sämre prognos.
-
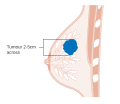
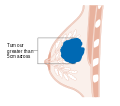
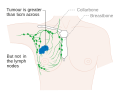
Scen . Bröstcancerstadieindelning med TNM-systemet baseras på tumörens storlek ( T ), om tumören har spridit sig till lymfkörtlarna ( N ) i armhålorna eller inte och om tumören har m etastaserats ( M ) (dvs. sprids till en mer avlägsen del av kroppen). Större storlek, nodal spridning och metastaser har ett större stadiumnummer och en sämre prognos. Huvudstadierna är:
- Steg 0 är ett pre-canceröst eller markörtillstånd, antingen duktalt karcinom in situ (DCIS) eller lobulärt karcinom in situ (LCIS).
- Stadier 1–3 är inom bröstet eller regionala lymfkörtlar.
- Steg 4 är "metastaserande" cancer som har en mindre gynnsam prognos eftersom den har spridit sig utanför bröstet och regionala lymfkörtlar.
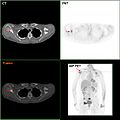
- Där det är tillgängligt kan avbildningsstudier användas som en del av iscensättningsprocessen i vissa fall för att leta efter tecken på metastaserande cancer. Men i fall av bröstcancer med låg risk för metastaser uppväger riskerna förknippade med PET-skanningar , CT-skanningar eller benskanningar de möjliga fördelarna, eftersom dessa procedurer utsätter personen för en betydande mängd potentiellt farlig joniserande strålning.
-
Receptorstatus . Bröstcancerceller har receptorer på sin yta och i sin cytoplasma och kärna . Kemiska budbärare som hormoner binder till receptorer och detta orsakar förändringar i cellen. Bröstcancerceller kan ha eller inte ha tre viktiga receptorer: östrogenreceptor (ER), progesteronreceptor (PR) och HER2 .
ER+ cancerceller (det vill säga cancerceller som har östrogenreceptorer) är beroende av östrogen för sin tillväxt, så de kan behandlas med läkemedel för att blockera östrogeneffekter (t.ex. tamoxifen ), och har generellt en bättre prognos. Obehandlad är HER2+ bröstcancer generellt sett mer aggressiv än HER2+ bröstcancer, men HER2+ cancerceller svarar på läkemedel som den monoklonala antikroppen trastuzumab (i kombination med konventionell kemoterapi), och detta har förbättrat prognosen avsevärt. Celler som inte har någon av dessa tre receptortyper (östrogenreceptorer, progesteronreceptorer eller HER2) kallas trippelnegativa , även om de ofta uttrycker receptorer för andra hormoner, såsom androgenreceptorer och prolaktinreceptorer . - DNA-analyser . DNA-tester av olika typer inklusive DNA-mikroarrayer har jämfört normala celler med bröstcancerceller. De specifika förändringarna i en viss bröstcancer kan användas för att klassificera cancern på flera sätt och kan hjälpa till att välja den mest effektiva behandlingen för den DNA-typen.
Undersökning
Bröstcancerscreening hänvisar till att testa annars friska kvinnor för bröstcancer i ett försök att uppnå en tidigare diagnos under antagandet att tidig upptäckt kommer att förbättra resultaten. Ett antal screeningtester har använts inklusive kliniska och självbröstundersökningar, mammografi , genetisk screening, ultraljud och magnetisk resonanstomografi.
En klinisk eller självbröstundersökning innebär att känna bröstet efter knölar eller andra avvikelser. Kliniska bröstundersökningar utförs av vårdgivare, medan självbröstundersökningar utförs av personen själv. Bevis stödjer inte effektiviteten av någon av de olika typerna av bröstundersökningar, eftersom när en knöl är tillräckligt stor för att hittas kommer den sannolikt att ha växt i flera år och därmed snart vara tillräckligt stor för att hittas utan undersökning. Mammografisk screening för bröstcancer använder röntgenstrålar för att undersöka bröstet för okarakteristiska massor eller klumpar. Under en screening komprimeras bröstet och en tekniker tar bilder från flera vinklar. Ett allmänt mammografi tar bilder av hela bröstet, medan ett diagnostiskt mammografi fokuserar på en specifik knöl eller ett område av oro.
Ett antal nationella organ rekommenderar bröstcancerscreening. För den genomsnittliga kvinnan rekommenderar US Preventive Services Task Force och American College of Physicians mammografi vartannat år hos kvinnor mellan 50 och 74 år, Europarådet rekommenderar mammografi mellan 50 och 69 med de flesta program som använder en 2-års frekvens , medan Europeiska kommissionen rekommenderar mammografi från 45 till 75 vartannat till vart tredje år, och i Kanada rekommenderas screening mellan 50 och 74 år med en frekvens av 2 till 3 år. American Cancer Society stöder också att kvinnor i åldern 40 år och äldre får mammografi årligen. Dessa arbetsgruppsrapporter påpekar att förutom onödiga operationer och ångest inkluderar riskerna med mer frekventa mammografi en liten men signifikant ökning av bröstcancer orsakad av strålning.
Cochrane -samarbetet (2013) anger att bevis av bästa kvalitet varken visar en minskning av cancerspecifika eller en minskning av alla orsaksdödlighet från screening av mammografi. När mindre rigorösa studier läggs till analysen sker en minskning av dödligheten i bröstcancer med 0,05 % (en minskning med 1 av 2000 dödsfall i bröstcancer under 10 år eller en relativ minskning på 15 % i bröstcancer). Screening över 10 år resulterar i en ökning med 30 % av frekvensen av överdiagnostik och överbehandling (3 till 14 per 1000) och mer än hälften kommer att ha minst ett falskt positivt test. Detta har resulterat i uppfattningen att det inte är klart om mammografiscreening gör mer nytta eller skada. Cochrane konstaterar att, på grund av de senaste förbättringarna av bröstcancerbehandling och riskerna för falska positiva resultat från bröstcancerscreening som leder till onödig behandling, "det verkar därför inte längre fördelaktigt att gå till bröstcancerscreening" i alla åldrar. Det är inte känt om MRT som screeningmetod har större skador eller fördelar jämfört med standard mammografi.
Förebyggande
Livsstil
Kvinnor kan minska risken för bröstcancer genom att hålla en hälsosam vikt, minska alkoholanvändningen , öka fysisk aktivitet och amma . Dessa ändringar kan förhindra 38 % av bröstcancerfallen i USA, 42 % i Storbritannien, 28 % i Brasilien och 20 % i Kina. Fördelarna med måttlig träning som snabba promenader ses i alla åldersgrupper inklusive postmenopausala kvinnor. Hög fysisk aktivitet minskar risken för bröstcancer med cirka 14 %. Strategier som uppmuntrar regelbunden fysisk aktivitet och minskar fetma kan också ha andra fördelar, såsom minskade risker för hjärt- och kärlsjukdomar och diabetes. En studie som inkluderade data från 130 957 kvinnor av europeisk härkomst fann "starka bevis för att högre nivåer av fysisk aktivitet och mindre stillasittande tid sannolikt minskar risken för bröstcancer, med resultat som generellt är konsekventa över bröstcancersubtyper".
American Cancer Society och American Society of Clinical Oncology rådde 2016 att människor borde äta en diet rik på grönsaker, frukt, fullkorn och baljväxter. Högt intag av citrusfrukter har associerats med en 10% minskning av risken för bröstcancer. Marina omega-3 fleromättade fettsyror verkar minska risken. Hög konsumtion av sojabaserade livsmedel kan minska risken.
Förebyggande operation
Borttagning av båda brösten innan någon cancer har diagnostiserats eller någon misstänkt knöl eller annan lesion har uppstått (ett förfarande som kallas "profylaktisk bilateral mastektomi " eller "riskreducerande mastektomi") kan övervägas hos kvinnor med BRCA1- och BRCA2-mutationer, som är associerade med en avsevärt förhöjd risk för en eventuell diagnos av bröstcancer. Bevis är inte tillräckligt starkt för att stödja denna procedur hos någon annan än kvinnor med den högsta risken. BRCA-testning rekommenderas för personer med hög familjerisk efter genetisk rådgivning. Det rekommenderas inte rutinmässigt. Detta beror på att det finns många former av förändringar i BRCA-gener, allt från ofarliga polymorfismer till uppenbart farliga frameshift-mutationer . Effekten av de flesta identifierbara förändringar i generna är osäker. Att testa på en person med genomsnittlig risk är särskilt sannolikt att ge ett av dessa obestämda, värdelösa resultat. Att ta bort det andra bröstet hos en person som har bröstcancer (kontralateral riskreducerande mastektomi eller CRRM) kan minska risken för cancer i det andra bröstet, men det är oklart om att ta bort det andra bröstet hos dem som har bröstcancer förbättrar överlevnaden. Allt fler kvinnor som testar positivt för felaktiga BRCA1- eller BRCA2-gener väljer att genomgå en riskreducerande operation . Samtidigt är den genomsnittliga väntetiden för att genomgå ingreppet två år, vilket är mycket längre än rekommenderat.
Mediciner
De selektiva östrogenreceptormodulatorerna minskar risken för bröstcancer men ökar risken för tromboembolism och endometriecancer . Det finns ingen övergripande förändring i risken för dödsfall. De rekommenderas därför inte för att förebygga bröstcancer hos kvinnor med genomsnittlig risk, men det rekommenderas att de erbjuds till personer med hög risk och över 35 år. behandlingsförlopp med dessa mediciner. Aromatashämmare (som exemestan och anastrozol ) kan vara effektivare än selektiva östrogenreceptormodulatorer (som tamoxifen) för att minska risken för bröstcancer och de är inte förknippade med en ökad risk för endometriecancer och tromboembolism.
Förvaltning
Hanteringen av bröstcancer beror på olika faktorer, inklusive cancerstadiet och personens ålder. Behandlingar är mer aggressiva när cancern är mer avancerad eller det finns en högre risk för återfall av cancern efter behandling.
Bröstcancer behandlas vanligtvis med kirurgi, som kan följas av kemoterapi eller strålbehandling, eller båda. Ett multidisciplinärt arbetssätt är att föredra. Hormonreceptorpositiva cancerformer behandlas ofta med hormonblockerande terapi under flera år. Monoklonala antikroppar, eller andra immunmodulerande behandlingar, kan administreras i vissa fall av metastaserande och andra avancerade stadier av bröstcancer, även om detta behandlingsområde fortfarande studeras.
Kirurgi

Kirurgi involverar fysiskt avlägsnande av tumören, vanligtvis tillsammans med en del av den omgivande vävnaden. En eller flera lymfkörtlar kan biopsieras under operationen; Lymfkörtelprovtagningen utförs i allt högre grad genom en vaktpostlymfkörtelbiopsi .
Standardoperationer inkluderar:
- Mastektomi : Borttagning av hela bröstet.
- Kvadrantektomi : Borttagning av en fjärdedel av bröstet.
- Lumpektomi : Borttagning av en liten del av bröstet.
När tumören har tagits bort, om personen så önskar, kan bröstrekonstruktionskirurgi , en typ av plastikkirurgi , utföras för att förbättra det estetiska utseendet på den behandlade platsen. Alternativt använder kvinnor bröstproteser för att simulera ett bröst under kläderna, eller väljer en platt bröstkorg. Bröstvårtans protes kan användas när som helst efter mastektomi.
Medicin
Läkemedel som används efter och utöver operation kallas för adjuvant terapi . Kemoterapi eller andra typer av terapi före operation kallas neoadjuvant terapi . Aspirin kan minska dödligheten i bröstcancer när det används tillsammans med andra behandlingar.
Det finns för närvarande tre huvudgrupper av läkemedel som används för adjuvant bröstcancerbehandling: hormonblockerande medel, kemoterapi och monoklonala antikroppar.
Hormonell terapi
Vissa bröstcancer kräver östrogen för att fortsätta växa. De kan identifieras genom närvaron av östrogenreceptorer (ER+) och progesteronreceptorer (PR+) på deras yta (ibland kallade tillsammans för hormonreceptorer). Dessa ER+ cancerformer kan behandlas med läkemedel som antingen blockerar receptorerna, t.ex. tamoxifen , eller alternativt blockerar produktionen av östrogen med en aromatashämmare , t.ex. anastrozol eller letrozol . Användning av tamoxifen rekommenderas i 10 år. Tamoxifen ökar risken för postmenopausala blödningar , endometriepolyper , hyperplasi och endometriecancer ; Användning av tamoxifen med ett intrauterint system som frisätter levonorgestrel kan öka vaginal blödning efter ett till två år, men minskar något endometriepolyper och hyperplasi, men inte nödvändigtvis endometriecancer. Letrozol rekommenderas i fem år.
Aromatashämmare är endast lämpliga för kvinnor efter klimakteriet; men i denna grupp verkar de bättre än tamoxifen. Detta beror på att det aktiva aromataset hos postmenopausala kvinnor skiljer sig från den vanliga formen hos premenopausala kvinnor, och därför är dessa medel ineffektiva för att hämma det dominerande aromataset hos premenopausala kvinnor. Aromatashämmare ska inte ges till premenopausala kvinnor med intakt äggstocksfunktion (såvida de inte också är på behandling för att stoppa deras äggstockar från att fungera). CDK-hämmare kan användas i kombination med endokrin eller aromatasterapi.
Kemoterapi
Kemoterapi används främst för fall av bröstcancer i steg 2–4, och är särskilt fördelaktigt vid östrogenreceptornegativ (ER-) sjukdom. Cytostatikamedicinerna administreras i kombinationer, vanligtvis under 3–6 månaders perioder. En av de vanligaste regimerna, känd som "AC", kombinerar cyklofosfamid med doxorubicin . Ibland tillsätts ett taxanläkemedel , såsom docetaxel , och regimen är då känd som "CAT". En annan vanlig behandling är cyklofosfamid, metotrexat och fluorouracil (eller "CMF"). De flesta kemoterapimediciner fungerar genom att förstöra snabbväxande och/eller snabbt replikerande cancerceller, antingen genom att orsaka DNA-skada vid replikering eller genom andra mekanismer. Men medicinerna skadar också snabbväxande normala celler, vilket kan orsaka allvarliga biverkningar. Skador på hjärtmuskeln är den farligaste komplikationen av till exempel doxorubicin.
Monoklonala antikroppar
Trastuzumab , en monoklonal antikropp mot HER2, har förbättrat den femåriga sjukdomsfria överlevnaden av HER2-positiva bröstcancer i stadium 1–3 till cirka 87 % (total överlevnad 95 %). Mellan 25 % och 30 % av bröstcancerfallen överuttrycker HER2-genen eller dess proteinprodukt, och överuttryck av HER2 i bröstcancer är associerat med ökat återfall av sjukdomen och sämre prognos. Trastuzumab är dock mycket dyrt och dess användning kan orsaka allvarliga biverkningar (ungefär 2 % av personer som får det utvecklar betydande hjärtskador). En annan antikropp pertuzumab förhindrar HER2-dimerisering och rekommenderas tillsammans med trastuzumab och kemoterapi vid svår sjukdom.
Riktad terapi
Elacestrant (Orserdu) godkändes för medicinsk användning i USA i januari 2023.
Strålning
Strålbehandling ges efter operation till regionen av tumörbädden och regionala lymfkörtlar, för att förstöra mikroskopiska tumörceller som kan ha undgått operation. När den ges intraoperativt som riktad intraoperativ strålbehandling kan den också ha en gynnsam effekt på tumörens mikromiljö. Strålbehandling kan ges som extern strålbehandling eller som brachyterapi (intern strålbehandling). Konventionellt ges strålbehandling efter operationen för bröstcancer. Strålning kan också ges vid operationstillfället av bröstcancern. Strålning kan minska risken för återfall med 50–66 % (1/2 – 2/3 minskning av risken) när den tillförs i rätt dos och anses nödvändig när bröstcancer behandlas genom att endast ta bort klumpen (Lumpectomy eller Wide Local excision). ). Vid tidig bröstcancer ger partiell bröstbestrålning inte samma cancerkontroll i bröstet som vid behandling av hela bröstet och kan orsaka värre biverkningar.
Eftervård
Vård efter primär bröstcancerbehandling, annars kallad ”uppföljningsvård”, kan vara intensiv med regelbundna laboratorietester på asymtomatiska personer för att försöka uppnå tidigare upptäckt av eventuella metastaser. En granskning har visat att uppföljningsprogram med regelbundna fysiska undersökningar och enbart årlig mammografi är lika effektiva som mer intensiva program bestående av laboratorietester när det gäller tidig upptäckt av återfall, total överlevnad och livskvalitet.
Multidisciplinära rehabiliteringsprogram, ofta inklusive träning, utbildning och psykologisk hjälp, kan ge kortsiktiga förbättringar av funktionsförmåga, psykosocial anpassning och socialt deltagande hos personer med bröstcancer.
Besvär i övre extremiteterna som axel- och armsmärtor, svaghet och begränsad rörelse är en vanlig biverkning efter strålbehandling eller bröstcanceroperation. Enligt forskning i Storbritannien kan ett träningsprogram som startas 7–10 dagar efter operationen minska problem i övre extremiteterna.
Prognos
Prognostiska faktorer
| Skede | 5-års överlevnad |
|---|---|
| Steg I | 100 % |
| Steg II | 90 % |
| Steg III | 70 % |
| Steg IV | 30 % |
Stadiet av bröstcancer är den viktigaste komponenten i traditionella klassificeringsmetoder för bröstcancer, eftersom det har en större effekt på prognosen än andra överväganden . Stadieindelningen tar hänsyn till storlek, lokalt engagemang, lymfkörtelstatus och om metastaserande sjukdom föreligger. Ju högre stadium vid diagnos, desto sämre prognos. Stadiet höjs av sjukdomens invasivitet till lymfkörtlar, bröstvägg, hud eller utanför, och cancercellernas aggressivitet. Stadiet sänks av förekomsten av cancerfria zoner och nära-normalt cellbeteende (gradering). Storleken är inte en faktor i iscensättningen om inte cancern är invasiv. Till exempel kommer duktalt karcinom in situ (DCIS) som involverar hela bröstet fortfarande att vara stadium noll och följaktligen en utmärkt prognos.
- Cancer i steg 1 (och DCIS, LCIS) har en utmärkt prognos och behandlas i allmänhet med lumpektomi och ibland strålning.
- Cancer i steg 2 och 3 med en successivt sämre prognos och större risk för återfall behandlas vanligtvis med kirurgi (lumpektomi eller mastektomi med eller utan avlägsnande av lymfkörtel ), kemoterapi (plus trastuzumab för HER2+-cancer) och ibland strålning (särskilt efter stora cancerformer, multipla cancerformer). positiva noder eller lumpektomi).
- Steg 4, metastaserande cancer, (dvs spridning till avlägsna platser) har en dålig prognos och hanteras av olika kombinationer av alla behandlingar från kirurgi, strålning, kemoterapi och riktade terapier.
Bröstcancergraden bedöms genom att jämföra bröstcancercellerna med normala bröstceller. Ju närmare normala cancercellerna är, desto långsammare tillväxt och desto bättre prognos. Om celler inte är väl differentierade kommer de att verka omogna, dela sig snabbare och tenderar att spridas. Väl differentierad får betyget 1, måttlig är betyget 2, medan dålig eller odifferentierad får ett högre betyg på 3 eller 4 (beroende på vilken skala som används). Det mest använda betygssystemet är Nottingham-schemat.
Yngre kvinnor med en ålder under 40 år eller kvinnor över 80 år tenderar att ha en sämre prognos än postmenopausala kvinnor på grund av flera faktorer. Deras bröst kan förändras med deras menstruationscykler, de kan vara ammande spädbarn och de kan vara omedvetna om förändringar i deras bröst. Därför är yngre kvinnor vanligtvis i ett mer framskridet stadium när de får diagnosen. Det kan också finnas biologiska faktorer som bidrar till en högre risk för återfall av sjukdomen för yngre kvinnor med bröstcancer.
Psykologiska aspekter
Inte alla människor med bröstcancer upplever sin sjukdom på samma sätt. Faktorer som ålder kan ha en betydande inverkan på hur en person hanterar en bröstcancerdiagnos. Premenopausala kvinnor med östrogenreceptorpositiv bröstcancer måste konfrontera problemen med tidig klimakteriet som induceras av många av de kemoterapiregimer som används för att behandla sin bröstcancer, särskilt de som använder hormoner för att motverka äggstocksfunktion.
Hos kvinnor med icke-metastaserande bröstcancer kan psykologiska interventioner som kognitiv beteendeterapi ha positiva effekter på utfall som ångest, depression och humörstörningar. Fysisk aktivitetsinterventioner kan också ha positiva effekter på hälsorelaterad livskvalitet, ångest, kondition och fysisk aktivitet hos kvinnor med bröstcancer efter adjuvant behandling.
Epidemiologi
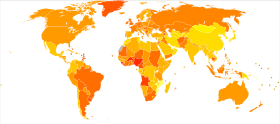
|
inga data
<2
2–4
4–6
6–8
8–10
10–12 |
12–14
14–16
16–18
18–20
20–22
>22 |
Över hela världen är bröstcancer den vanligaste invasiva cancerformen hos kvinnor. Tillsammans med lungcancer är bröstcancer den vanligaste diagnosen cancer, med 2,09 miljoner fall vardera 2018. Bröstcancer drabbar 1 av 7 (14 %) av kvinnorna i världen. (Den vanligaste formen av cancer är icke-invasiv icke-melanom hudcancer ; icke-invasiva cancerformer är i allmänhet lätta att bota, orsakar mycket få dödsfall och utesluts rutinmässigt från cancerstatistiken.) Bröstcancer utgör 22,9 % av alla invasiva cancerformer hos kvinnor och 16 % av all cancer hos kvinnor. År 2012 utgjorde den 25,2 % av cancersjukdomarna som diagnostiserades hos kvinnor, vilket gör den till den vanligaste kvinnliga cancern.
Under 2008 orsakade bröstcancer 458 503 dödsfall över hela världen (13,7 % av cancerdödsfallen hos kvinnor och 6,0 % av alla cancerdödsfall för män och kvinnor tillsammans). Lungcancer, den näst vanligaste orsaken till cancerrelaterade dödsfall hos kvinnor, orsakade 12,8 % av cancerdödsfallen hos kvinnor (18,2 % av alla dödsfall i cancer för män och kvinnor tillsammans).
Förekomsten av bröstcancer varierar kraftigt runt om i världen: den är lägst i mindre utvecklade länder och störst i de mer utvecklade länderna. I de tolv världsregionerna är de årliga åldersstandardiserade incidenstalen per 100 000 kvinnor följande: 18 i östra Asien, 22 i södra Centralasien och Afrika söder om Sahara, 26 i sydöstra Asien, 26, 28 i Nordafrika och Västasien, 42 i Syd- och Centralamerika, 42, 49 i Östeuropa, 56 i Sydeuropa, 73 i Nordeuropa, 74 i Oceanien, 78 i Västeuropa och 90 i Nordamerika. Metastaserad bröstcancer drabbar mellan 19 % (USA) och 50 % (delar av Afrika) av kvinnor med bröstcancer.
Antalet fall över hela världen har ökat avsevärt sedan 1970-talet, ett fenomen som delvis tillskrivs den moderna livsstilen. Bröstcancer är starkt relaterad till ålder med endast 5 % av all bröstcancer som förekommer hos kvinnor under 40 år. Det fanns mer än 41 000 nydiagnostiserade fall av bröstcancer registrerade i England 2011, cirka 80 % av dessa fall var hos kvinnor som var 50 år eller äldre. Baserat på amerikansk statistik 2015 fanns det 2,8 miljoner kvinnor som drabbades av bröstcancer. I USA ökade den åldersjusterade incidensen av bröstcancer per 100 000 kvinnor från cirka 102 fall per år på 1970-talet till cirka 141 i slutet av 1990-talet, och har sedan dess sjunkit och hållit sig konstant kring 125 sedan 2003. Men åldern -justerade dödsfall i bröstcancer per 100 000 kvinnor ökade endast något från 31,4 år 1975 till 33,2 år 1989 och har sedan dess minskat stadigt till 20,5 år 2014.
Flera primära tumörer
Flera primära tumörer kan uppstå på olika platser (i motsats till att en enda tumör sprids). Dessa tumörer kan förekomma i båda brösten (bilaterala tumörer), i olika kvadranter av ett enda bröst (multicentrisk cancer), eller separata tumörer inom en enda bröstkvadrant (multifokal cancer).
Incidensen av multicentriska och multifokala bröstcancer (MMBC) ökar, delvis på grund av förbättrad mammografiteknik. Incidensen av MMBC rapporteras mellan 9 och 75 % i höginkomstländer, beroende på kriterier som används. Till exempel rapporterade Kina att endast 2% av patienterna definieras som MMBC. Anledningen till denna skillnad beror på bristande enhetlighet i diagnosen. Därför bör standardiserade metoder och kriterier göras för att definiera förekomsten av MMBC korrekt.
Mutationer i tumörsuppressorgener såsom BRCA1 och BRCA2 , PI3K /AKT/mTOR-vägen och PTEN kan relateras till bildandet av flera primära bröstcancer. Diagnos sker på samma sätt som andra bröstcancerformer.
Mastektomi är den vanliga kirurgiska behandlingen för multicentriska bröstcancerpatienter. Dubbel lumpektomi , även märkt som bröstkonservativ terapi (BCT), är en alternativ och föredragen kirurgisk behandling till mastektomi för patienter med multicentrisk bröstcancer i tidigt stadium. Förfarandet med dubbla lumpektomier involverar kirurgisk ablation av cancertumörhärdarna och de omgivande bröstvävnaderna i olika kvadranter av samma bröst. Fördelarna med dubbla lumpektomier är undvikandet av bröstrekonstruktionskirurgi och minimal bröst ärrbildning. Det är dock inte att föredra för patienter med fler än två tumörer i samma bröst på grund av svårigheter att ta bort alla cancerceller. Patienter med flera primära brösttumörer kan få behandlingar som kemoterapi, strålbehandling och bröstrekonstruktionskirurgi för samma indikationer som andra bröstcancerpatienter.
Historia
På grund av dess synlighet var bröstcancer den cancerform som oftast beskrivs i gamla dokument. Eftersom obduktioner var sällsynta var cancer i de inre organen i princip osynliga för antikens medicin. Bröstcancer kunde dock kännas genom huden och i sitt avancerade tillstånd utvecklades ofta till svampskador : tumören skulle bli nekrotisk (dö från insidan, vilket gör att tumören ser ut att gå sönder) och sår upp sig genom huden och gråter stinkande, mörk vätska.
Det äldsta upptäckta beviset på bröstcancer är från Egypten och går tillbaka 4200 år, till den sjätte dynastin . Studien av en kvinnas kvarlevor från nekropolen Qubbet el-Hawa visade den typiska destruktiva skadan på grund av metastatisk spridning. Edwin Smith Papyrus beskriver åtta fall av tumörer eller sår i bröstet som behandlades genom kauterisering . Skriften säger om sjukdomen, "Det finns ingen behandling." I århundraden har läkare beskrivit liknande fall i sina metoder, med samma slutsats. Forntida medicin, från grekernas tid till 1600-talet, var baserad på humoralism och trodde därför att bröstcancer i allmänhet orsakades av obalanser i de grundläggande vätskorna som kontrollerade kroppen, särskilt ett överskott av svart galla . Alternativt sågs det som gudomligt straff .
Mastektomi för bröstcancer utfördes åtminstone så tidigt som 548 e.Kr., då det föreslogs av hovläkaren Aetios av Amida till Theodora . Det var inte förrän läkarna fick större förståelse för cirkulationssystemet på 1600-talet som de kunde koppla bröstcancers spridning till lymfkörtlarna i armhålan. I början av 1700-talet utförde den franske kirurgen Jean Louis Petit totala mastektomier som inkluderade borttagning av axillära lymfkörtlar , eftersom han insåg att detta minskade återfall. Petits arbete byggde på metoderna från kirurgen Bernard Peyrilhe , som på 1600-talet dessutom tog bort bröstmuskeln under bröstet, eftersom han bedömde att detta förbättrade prognosen avsevärt. Men dåliga resultat och den avsevärda risken för patienten gjorde att läkare inte delade åsikten från kirurger som Nicolaes Tulp , som på 1600-talet utropade "det enda botemedlet är en operation i tid". Den framstående kirurgen Richard Wiseman dokumenterade i mitten av 1600-talet att efter 12 mastektomier dog två patienter under operationen, åtta patienter dog kort efter operationen av progressiv cancer och endast två av de 12 patienterna blev botade. Läkare var konservativa i behandlingen de ordinerade i de tidiga stadierna av bröstcancer. Patienterna behandlades med en blandning av detox-utrensningar , blodutsläpp och traditionella läkemedel som var tänkta att sänka surheten, såsom alkalisk arsenik .
När Anne av Österrike 1664 fick diagnosen bröstcancer, involverade den första behandlingen kompresser mättade med hemlockjuice . När klumparna ökade inledde kungens läkare en behandling med arseniksalvor . Den kungliga patienten dog 1666 i fruktansvärd smärta. Varje misslyckad behandling för bröstcancer ledde till sökandet efter nya behandlingar, vilket stimulerade en marknad för läkemedel som annonserades och såldes av kvacksalvare , örtläkare , kemister och apotekare . Bristen på anestesi och antiseptika gjorde mastektomi till en smärtsam och farlig prövning. På 1700-talet åtföljdes en mängd olika anatomiska upptäckter av nya teorier om orsaken till och tillväxten av bröstcancer. Den undersökande kirurgen John Hunter hävdade att neural vätska genererade bröstcancer. Andra kirurger föreslog att mjölk i bröstvägarna ledde till cancertillväxt. Teorier om trauma mot bröstet som orsak till maligna förändringar i bröstvävnad var avancerade. Upptäckten av bröstklumpar och svullnader underblåste kontroverser om hårda tumörer och om knölar var godartade stadier av cancer. Medicinska åsikter om nödvändig omedelbar behandling varierade. Kirurgen Benjamin Bell förespråkade borttagning av hela bröstet, även när bara en del var påverkad.
Bröstcancer var ovanligt fram till 1800-talet, då förbättringar av sanitet och kontroll av dödliga infektionssjukdomar resulterade i dramatiska ökningar av livslängden. Tidigare hade de flesta kvinnor dött för unga för att ha utvecklat bröstcancer. År 1878 beskrev en artikel i Scientific American historisk behandling med tryck avsett att framkalla lokal ischemi i de fall då kirurgiskt avlägsnande inte var möjligt. William Stewart Halsted började utföra radikala mastektomier 1882, mycket hjälpt av framsteg inom allmän kirurgisk teknik, såsom aseptisk teknik och anestesi. Halsted radikal mastektomi involverade ofta att ta bort båda brösten, associerade lymfkörtlar och de underliggande bröstmusklerna. Detta ledde ofta till långvarig smärta och funktionsnedsättning, men ansågs nödvändigt för att förhindra att cancern skulle återkomma. Före tillkomsten av Halsted radikala mastektomi var 20-årsöverlevnaden endast 10%; Halsteds operation höjde den siffran till 50%.
Bröstcancerstadiesystem utvecklades på 1920- och 1930-talen för att bestämma i vilken utsträckning en cancer har utvecklats genom att växa och sprida sig. Den första fallkontrollerade studien om bröstcancerepidemiologi gjordes av Janet Lane-Claypon , som publicerade en jämförande studie 1926 av 500 bröstcancerfall och 500 kontroller med samma bakgrund och livsstil för det brittiska hälsoministeriet. Radikala mastektomier förblev standarden för vård i USA fram till 1970-talet, men i Europa antogs i allmänhet bröstbesparande procedurer, ofta följt av strålbehandling , på 1950-talet. År 1955 publicerade George Crile Jr. Cancer and Common Sense och hävdade att cancerpatienter behövde förstå tillgängliga behandlingsalternativ. Crile blev en nära vän till miljöaktivisten Rachel Carson , som hade genomgått en radikal mastektomi i Halsted 1960 för att behandla sin malign bröstcancer. Den amerikanske onkologen Jerome Urban främjade superradikala mastektomier, och tog ännu mer vävnad, fram till 1963, då de tioåriga överlevnaden visade sig vara lika med den mindre skadliga radikala mastektomien. Carson dog 1964 och Crile fortsatte med att publicera ett brett utbud av artiklar, både i den populära pressen och i medicinska tidskrifter, som utmanade den utbredda användningen av Halsteds radikala mastektomi. 1973 publicerade Crile What Women Should Know About the Breast Cancer Controversy . När Betty Ford 1974 diagnostiserades med bröstcancer diskuterades alternativen för att behandla bröstcancer öppet i pressen. Under 1970-talet ledde en ny förståelse av metastaser till att man uppfattade cancer som en systemisk sjukdom såväl som en lokaliserad, och mer sparsamma procedurer utvecklades som visade sig vara lika effektiva.
På 1980- och 1990-talen krävde och fick sedan tusentals kvinnor som framgångsrikt slutfört standardbehandling höga doser benmärgstransplantationer, och trodde att detta skulle leda till bättre långsiktig överlevnad. Det visade sig dock vara helt ineffektivt och 15–20 % av kvinnorna dog på grund av den brutala behandlingen. 1995 års rapporter från Nurses' Health Study och 2002 års slutsatser från Women's Health Initiative- studien bevisade definitivt att hormonbehandling avsevärt ökade förekomsten av bröstcancer.
Samhälle och kultur
Före 1900-talet fruktades och diskuterades bröstcancer i tysta toner, som om det vore skamligt. Eftersom lite säkert kunde göras med primitiva kirurgiska tekniker, tenderade kvinnor att lida tyst snarare än att söka vård. När operationen utvecklades och överlevnaden på lång sikt förbättrades, började kvinnor att öka medvetenheten om sjukdomen och möjligheten till framgångsrik behandling. "Women's Field Army", som drevs av American Society for the Control of Cancer (senare American Cancer Society ) under 1930- och 1940-talen var en av de första organiserade kampanjerna. 1952 började den första peer-to-peer- stödgruppen , kallad "Reach to Recovery", tillhandahålla besök på sjukhus efter mastektomi från kvinnor som överlevt bröstcancer.
Bröstcancerrörelsen på 1980- och 1990-talen utvecklades ur de större feministiska rörelserna och kvinnohälsorörelsen på 1900-talet . Denna serie av politiska och utbildningskampanjer, delvis inspirerade av de politiskt och socialt effektiva kampanjerna för AIDS-medvetenhet, resulterade i en utbredd acceptans av andra åsikter före operation, mindre invasiva kirurgiska ingrepp, stödgrupper och andra framsteg inom vården.
Rosa band

Ett rosa band är den mest framträdande symbolen för bröstcancermedvetenhet. Rosa band, som kan göras billigt, säljs ibland som insamlingar, ungefär som vallmo på minnesdagen . De kan bäras för att hedra dem som har diagnostiserats med bröstcancer, eller för att identifiera produkter som tillverkaren skulle vilja sälja till konsumenter som är intresserade av bröstcancer. På 1990-talet lanserades kampanjer för medvetenhet om bröstcancer av amerikanska företag. Som en del av dessa orsaksrelaterade marknadsföringskampanjer donerade företag till en mängd olika bröstcancerinitiativ för varje rosa band-produkt som köptes.> The Wall Street Journal noterade "att de starka känslor som framkallats av bröstcancer översätts till ett företags resultat " . Medan många amerikanska företag donerade till befintliga bröstcancerinitiativ, etablerade andra som Avon sina egna bröstcancerstiftelser på baksidan av rosa bandprodukter.
Att bära eller visa upp ett rosa band har kritiserats av motståndarna till denna praxis som ett slags slacktivism , eftersom det inte har någon praktisk positiv effekt. Det har också kritiserats som hyckleri , eftersom vissa människor bär det rosa bandet för att visa god vilja mot kvinnor med bröstcancer, men sedan motsätter sig dessa kvinnors praktiska mål, som patienträttigheter och lagstiftning mot föroreningar . Kritiker säger att de rosa bandens må-bra natur och rosa konsumtion distraherar samhället från bristen på framsteg när det gäller att förebygga och bota bröstcancer. Det kritiseras också för att förstärka könsstereotyper och objektifiera kvinnor och deras bröst.< 2002 lanserade Breast Cancer Action kampanjen "Think Before You Pink" mot pinkwashing för att rikta sig mot företag som har valt den rosa kampanjen för att marknadsföra produkter som orsakar bröstcancer , såsom alkoholhaltiga drycker.
Bröstcancerkultur
I sin bok från 2006 Pink Ribbons, Inc.: Breast Cancer and the Politics of Philanthropy hävdade Samantha King att bröstcancer har förvandlats från en allvarlig sjukdom och individuell tragedi till en marknadsdriven bransch med överlevnad och företagsförsäljning. 2010 hävdade Gayle Sulik att de primära syftena eller målen med bröstcancerkulturen är att bibehålla bröstcancers dominans som den framträdande kvinnohälsofrågan, att främja intrycket att samhället gör något effektivt mot bröstcancer, och att upprätthålla och utöka bröstcanceraktivisters sociala, politiska och ekonomiska makt. Samma år publicerade Barbara Ehrenreich en åsiktsartikel i Harper's Magazine , där hon beklagade att i bröstcancerkulturen ses bröstcancerterapi som en övergångsrit snarare än en sjukdom. För att passa in i denna form måste kvinnan med bröstcancer normalisera och feminisera sitt utseende och minimera störningarna som hennes hälsoproblem orsakar någon annan. Ilska, sorg och negativitet måste tystas. Som med de flesta kulturella modeller ges människor som följer modellen social status, i det här fallet som canceröverlevande . Kvinnor som förkastar modellen skys, straffas och skäms. Kulturen kritiseras för att behandla vuxna kvinnor som små flickor, vilket framgår av "baby" leksaker som rosa nallar som ges till vuxna kvinnor.
Betoning
2009 kritiserade den amerikanska vetenskapsjournalisten Christie Aschwanden att tonvikten på bröstcancerscreening kan skada kvinnor genom att utsätta dem för onödig strålning, biopsier och kirurgi. En tredjedel av de diagnostiserade bröstcancerfallen kan avta av sig själv. Screening av mammografi upptäcker effektivt icke-livshotande, asymtomatiska bröstcancer och precancerformer, även om man förbiser allvarliga cancerformer. Enligt cancerforskaren H. Gilbert Welch har screening av mammografi tagit den "hjärndöda metoden som säger att det bästa testet är det som hittar flest cancerformer" snarare än det som hittar farliga cancerformer.
År 2002 noterades att som ett resultat av bröstcancers höga synlighet kan de statistiska resultaten misstolkas, såsom påståendet att en av åtta kvinnor kommer att få diagnosen bröstcancer under sitt liv – ett påstående som beror på det orealistiska antagandet att ingen kvinna kommer att dö av någon annan sjukdom före 95 års ålder. År 2010 var överlevnaden för bröstcancer i Europa 91 % efter ett år och 65 % efter fem år. I USA var femårsöverlevnaden för lokaliserad bröstcancer 96,8 %, medan den i fall av metastaser endast var 20,6 %. Eftersom prognosen för bröstcancer i detta skede var relativt gynnsam, jämfört med prognosen för andra cancerformer, var bröstcancer som dödsorsak bland kvinnor 13,9 % av alla dödsfall i cancer. Den näst vanligaste dödsorsaken i cancer hos kvinnor var lungcancer, den vanligaste cancerformen i världen för män och kvinnor. Den förbättrade överlevnaden gjorde bröstcancer till den vanligaste cancerformen i världen. År 2010 uppskattningsvis 3,6 miljoner kvinnor världen över har haft en bröstcancerdiagnos under de senaste fem åren, medan endast 1,4 miljoner manliga eller kvinnliga överlevande från lungcancer levde.
Skillnader i hälsa i bröstcancer
Det finns etniska skillnader i dödligheten för bröstcancer såväl som vid behandling av bröstcancer. Bröstcancer är den vanligaste cancerformen som drabbar kvinnor i alla etniska grupper i USA. Incidensen av bröstcancer bland svarta kvinnor i åldern 45 år och äldre är högre än för vita kvinnor i samma åldersgrupp. Vita kvinnor i åldern 60–84 har högre incidens av bröstcancer än svarta kvinnor. Trots detta är svarta kvinnor i alla åldrar mer benägna att ge efter för bröstcancer.
Bröstcancerbehandlingen har förbättrats avsevärt de senaste åren, men svarta kvinnor är fortfarande mindre benägna att få behandling jämfört med vita kvinnor. Riskfaktorer som socioekonomisk status, sent stadium eller bröstcancer vid diagnos, genetiska skillnader i tumörsubtyper, skillnader i tillgång till hälsovård bidrar alla till dessa skillnader. Socioekonomiska bestämningsfaktorer som påverkar skillnaden i bröstcancersjukdom inkluderar fattigdom, kultur och social orättvisa. Hos latinamerikanska kvinnor är förekomsten av bröstcancer lägre än hos icke-spansktalande kvinnor men diagnostiseras ofta i ett senare skede än vita kvinnor med större tumörer.
Svarta kvinnor diagnostiseras vanligtvis med bröstcancer i yngre ålder än vita kvinnor. Medianåldern för diagnos för svarta kvinnor är 59, jämfört med 62 för vita kvinnor. Förekomsten av bröstcancer hos svarta kvinnor har ökat med 0,4 % per år sedan 1975 och 1,5 % per år bland kvinnor från Asien/Stillahavsöarna sedan 1992. Incidensen var stabil för icke-spansktalande vita, latinamerikaner och infödda kvinnor. Femårsöverlevnaden noteras vara 81 % hos svarta kvinnor och 92 % hos vita kvinnor. Kinesiska och japanska kvinnor har den högsta överlevnaden.
Fattigdom är en viktig drivkraft för skillnader i samband med bröstcancer. Kvinnor med låga inkomster är mindre benägna att genomgå bröstcancerscreening och är därför mer benägna att få en diagnos i sent skede. Att se till att kvinnor från alla etniska grupper får rättvis hälsovård inklusive bröstscreening kan påverka dessa skillnader positivt.
Graviditet
Graviditet i tidig ålder minskar risken att utveckla bröstcancer senare i livet. Risken för bröstcancer minskar också med antalet barn en kvinna får. Bröstcancer blir sedan vanligare under 5 eller 10 år efter graviditeten men blir sedan mindre vanlig än bland befolkningen i allmänhet. Dessa cancerformer kallas postpartum bröstcancer och har sämre resultat inklusive en ökad risk för fjärrspridning av sjukdomar och dödlighet. Andra cancerformer som upptäcks under eller strax efter graviditeten uppträder i ungefär samma takt som andra cancerformer hos kvinnor i liknande ålder.
Att diagnostisera ny cancer hos en gravid kvinna är svårt, delvis på grund av att eventuella symtom vanligtvis antas vara ett normalt obehag i samband med graviditet. Som ett resultat av detta upptäcks cancer vanligtvis i ett något senare skede än genomsnittet hos många gravida eller nyligen gravida kvinnor. Vissa avbildningsprocedurer, såsom MRI (magnetisk resonanstomografi), datortomografi , ultraljud och mammografi med fosterskydd anses vara säkra under graviditeten; vissa andra, såsom PET-skanningar är det inte.
Behandlingen är i allmänhet densamma som för icke-gravida kvinnor. Strålning undviks dock normalt under graviditeten, särskilt om fosterdosen kan överstiga 100 cGy. I vissa fall skjuts vissa eller alla behandlingar upp till efter födseln om cancern upptäcks sent i graviditeten. Tidiga förlossningar för att påskynda behandlingens start är inte ovanligt. Kirurgi anses generellt vara säker under graviditet, men vissa andra behandlingar, särskilt vissa cytostatika som ges under den första trimestern , ökar risken för fosterskador och graviditetsförlust (spontana aborter och dödfödslar). Elektiva aborter krävs inte och förbättrar inte sannolikheten för att modern överlever eller blir botad.
Strålningsbehandlingar kan störa moderns förmåga att amma sitt barn eftersom det minskar bröstets förmåga att producera mjölk och ökar risken för mastit . Dessutom, när kemoterapi ges efter födseln, passerar många av läkemedlen genom bröstmjölken till barnet, vilket kan skada barnet.
När det gäller framtida graviditet bland överlevande bröstcancer finns det ofta rädsla för att cancer ska återkomma. Å andra sidan anser många fortfarande att graviditet och föräldraskap representerar normalitet, lycka och livsuppfyllelse.
Hormoner
Preventivmedel
Hos överlevande bröstcancer bör icke-hormonella preventivmetoder såsom kopparintrauterinapparaten (IUD) användas som förstahandsalternativ. Gestagenbaserade metoder som depå medroxiprogesteronacetat , spiral med gestagen eller enbart gestagenpiller har en dåligt utredd men möjligen ökad risk för cancerrecidiv, men kan användas om positiva effekter överväger denna eventuella risk.
Menopausal hormonersättning
Hos överlevande bröstcancer rekommenderas det att först överväga icke-hormonella alternativ för klimakteriets effekter, såsom bisfosfonater eller selektiva östrogenreceptormodulatorer (SERM) för osteoporos, och vaginalt östrogen för lokala symtom. Observationsstudier av systemisk hormonersättningsterapi efter bröstcancer är generellt betryggande. Om hormonersättning är nödvändig efter bröstcancer kan behandling med enbart östrogen eller östrogenbehandling med en intrauterin enhet med gestagen vara säkrare alternativ än kombinerad systemisk behandling.
Forskning
Behandlingar utvärderas i kliniska prövningar. Detta inkluderar individuella läkemedel, kombinationer av läkemedel och kirurgiska och strålningstekniker. Undersökningar inkluderar nya typer av riktad terapi , cancervacciner , onkolytisk viroterapi , genterapi och immunterapi .
Den senaste forskningen rapporteras årligen vid vetenskapliga möten som American Society of Clinical Oncology , San Antonio Breast Cancer Symposium och St. Gallen Oncology Conference i St. Gallen, Schweiz. Dessa studier granskas av professionella föreningar och andra organisationer och formuleras till riktlinjer för specifika behandlingsgrupper och riskkategorier.
Fenretinid , en retinoid , studeras också som ett sätt att minska risken för bröstcancer. I synnerhet har kombinationer av ribociclib plus endokrin terapi varit föremål för kliniska prövningar.
En granskning från 2019 fann måttliga säkra bevis för att ge människor antibiotika före bröstcanceroperation hjälpte till att förhindra infektion på operationsstället (SSI) . Ytterligare studier krävs för att fastställa det mest effektiva antibiotikaprotokollet och användningen hos kvinnor som genomgår omedelbar bröstrekonstruktion.
Kryoablation
Från och med 2014 studeras kryoablation för att se om det kan vara ett substitut för en lumpektomi vid små cancerformer. Det finns preliminära bevis hos de med tumörer mindre än 2 centimeter. Det kan också användas av personer där operation inte är möjlig. En annan recension säger att kryoablation ser lovande ut för tidig bröstcancer av liten storlek.
Bröstcancercellinjer
En del av den nuvarande kunskapen om bröstcancer baseras på in vivo och in vitro studier utförda med cellinjer från bröstcancer. Dessa ger en obegränsad källa till homogent självreplikerande material, fritt från kontaminerande stromaceller och ofta lätt att odla i enkla standardmedier . Den första beskrivna bröstcancercellinjen, BT-20 , etablerades 1958. Sedan dess, och trots ihållande arbete inom detta område, har antalet erhållna permanenta linjer varit slående lågt (cirka 100). Försök att odla bröstcancercellinjer från primära tumörer har faktiskt i stort sett varit misslyckade. Denna dåliga effektivitet berodde ofta på tekniska svårigheter förknippade med extraktion av livsdugliga tumörceller från deras omgivande stroma. De flesta av de tillgängliga bröstcancercellinjerna kommer från metastaserande tumörer, främst från pleurautgjutning . Effusioner gav i allmänhet ett stort antal dissocierade, livsdugliga tumörceller med liten eller ingen kontaminering av fibroblaster och andra tumörstromaceller. Många av de för närvarande använda BCC-linjerna etablerades i slutet av 1970-talet. Ett mycket fåtal av dem, nämligen MCF-7 , T-47D , MDA-MB-231 och SK-BR-3 , står för mer än två tredjedelar av alla sammanfattningar som rapporterar studier på nämnda bröstcancercellinjer, enligt slutsatsen från en Medline -baserad undersökning.
Molekylära markörer
Metaboliska markörer
Kliniskt är de mest användbara metabola markörerna vid bröstcancer östrogen- och progesteronreceptorerna som används för att förutsäga svar på hormonbehandling. Nya eller potentiellt nya markörer för bröstcancer inkluderar BRCA1 och BRCA2 för att identifiera personer med hög risk att utveckla bröstcancer, HER-2 och SCD1 , för att förutsäga svar på terapeutiska regimer, och urokinasplasminogenaktivator , PA1-1 och SCD1 för att bedöma prognos .
Andra djur
- Brösttumör för bröstcancer hos andra djur
- Musmodeller av bröstcancermetastaser
Referenser
externa länkar
|
Bibliotekets resurser om bröstcancer |