Melioidos - Melioidosis
| Melioidos | |
|---|---|
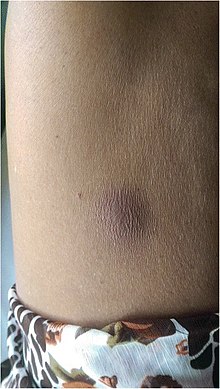 | |
| Melioidosabscess på buken | |
| Specialitet |
Smittsam sjukdom |
| Symtom | Ingen, feber, lunginflammation , flera bölder |
| Komplikationer | Encefalomyelit , septisk chock , akut pyelonefrit , septisk artrit , osteomyelit |
| Vanlig start | 1-21 dagar efter exponering |
| Orsaker | Burkholderia pseudomallei sprids genom kontakt med jord eller vatten |
| Riskfaktorer | Diabetes mellitus , talassemi , alkoholism , kronisk njursjukdom |
| Diagnostisk metod | Växer bakterierna i odlingsmedier |
| Differentialdiagnos | Tuberkulos |
| Förebyggande | Förebyggande från exponering för förorenat vatten, antibiotikaprofylax |
| Behandling | Ceftazidim , meropenem , co-trimoxazol |
| Frekvens | 165 000 personer per år |
| Dödsfall | 89 000 personer per år |
Melioidos är en infektionssjukdom som orsakas av en gramnegativ bakterie som kallas Burkholderia pseudomallei . De flesta smittade med B. pseudomallei upplever inga symptom, men de som upplever symtom har tecken och symtom som sträcker sig från mild, såsom feber , hudförändringar, lunginflammation och bölder , till svår med inflammation i hjärnan , inflammation i lederna och farligt lågt blodtryck som orsakar döden. Cirka 10% av personer med melioidos utvecklar symtom som varar längre än två månader, kallade "kronisk melioidos".
Människor infekteras med B. pseudomallei genom kontakt med förorenat vatten. Bakterierna kommer in i kroppen genom sår, inandning eller intag. Överföring från person till person eller från djur till människa är extremt sällsynt. Infektionen förekommer ständigt i Sydostasien, särskilt i nordöstra Thailand och norra Australien. I utvecklade länder, som i Europa och USA, importeras i allmänhet fall av melioidos från länder där melioidos är vanligare. Tecken och symtom på melioidos liknar tuberkulos och feldiagnos är vanligt. Diagnos bekräftas vanligtvis av tillväxten av B. pseudomallei från en infekterad persons blod eller annan kroppsvätska. De med melioidos behandlas först med en "intensiv fas" -kurs av intravenösa antibiotika (oftast ceftazidim ) följt av en flera månaders behandling av co-trimoxazol . Även om de behandlas ordentligt dör cirka 10% av personer med melioidos av det. Om den behandlas felaktigt kan dödsfallet uppgå till 40%.
Insatser för att förhindra melioidos inkluderar att bära skyddsutrustning vid hantering av förorenat vatten, öva handhygien, dricka kokt vatten och undvika direkt kontakt med jord, vatten eller kraftigt regn. Den antibiotika trimsulfa används som en förebyggande endast för personer med hög risk för att få melioidos efter att ha utsatts för bakterierna. Inget vaccin mot melioidos har godkänts.
Ungefär 165 000 människor smittas av melioidos per år, vilket resulterar i cirka 89 000 dödsfall. Diabetes är en stor riskfaktor för melioidos; över hälften av melioidosfallet är hos personer med diabetes. Ökad nederbörd är associerad med ökat antal melioidosfall i endemiska områden. Det beskrevs först av Alfred Whitmore 1912 i dagens Myanmar .
tecken och symtom
Akut
Exponering för Burkholderia pseudomallei kan vanligtvis orsaka att antikroppar produceras mot det utan några symptom. Av de patienter som utvecklar klinisk infektion upplever 85% akuta symptom från ett nyligen förvärvat bakterie. Den genomsnittliga inkubationstiden för akut melioidos är 9 dagar (intervall 1–21 dagar). Ändå kan symtom på melioidos dyka upp på 24 timmar för dem som är smittade under en nästan drunkning i förorenat vatten. De drabbade uppvisar symptom på sepsis (övervägande feber) med eller utan lunginflammation , eller lokal abscess eller annat infektionsfokus. Förekomsten av ospecifika tecken och symtom har fått melioidos att ha smeknamnet "den stora efterliknaren".
Personer med diabetes eller regelbunden exponering för bakterierna löper ökad risk att utveckla melioidos. Sjukdomen bör övervägas hos dem som vistas i endemiska områden som utvecklar feber, lunginflammation eller bölder i lever, mjälte, prostata eller parotidkörtlar. Den kliniska manifestationen av sjukdomen kan sträcka sig från enkla hudförändringar till allvarliga organproblem. Hudförändringar kan vara ospecifika abscesser eller sår. I norra Australien fick 60% av de infekterade barnen endast hudskador medan 20% fick lunginflammation. De vanligaste organen som drabbas är lever, mjälte, lungor, prostata och njurar. Bland de vanligaste kliniska tecknen är närvaron av bakterier i blodet (i 40 till 60%av fallen), lunginflammation (50%) och septisk chock (20%). Personer med endast lunginflammation kan ha en framträdande hosta med sputum och andfåddhet. Men de med septisk chock tillsammans med lunginflammation kan ha minimal hosta. Resultaten av en röntgenstråle kan variera från diffusa nodulära infiltrat hos personer med septisk chock till progressiv stelning av lungorna i de övre loberna endast för personer med lunginflammation. Överskott av vätska i pleurahålan och uppsamling av pus i ett hålrum är vanligare för melioidos som påverkar nedre loberna i lungorna. I 10% av fallen utvecklar människor sekundär lunginflammation orsakad av andra bakterier efter den primära infektionen.
Beroende på infektionsförloppet utvecklas andra allvarliga manifestationer. Ungefär 1 till 5% av de infekterade utvecklar inflammation i hjärnan och hjärnan som täcker eller samlar in pus i hjärnan ; 14 till 28% utvecklar bakteriell inflammation i njurarna , njure abscess eller prostatabscesser; 0 till 30% utvecklar abscesser i nacken eller spottkörteln ; 10 till 33% utvecklar lever-, mjälte- eller parestestinala bölder; 4 till 14% utvecklar septisk artrit och osteomyelit . Sällsynta manifestationer inkluderar lymfkörtelsjukdom som liknar tuberkulos, mediastinala massor, vätskeuppsamling i hjärtat som täcker , onormal dilatation av blodkärl på grund av infektion och inflammation i bukspottkörteln . I Australien utvecklar upp till 20% av de infekterade hanarna prostatabscess som kännetecknas av smärta under urinering , svårigheter att urinera och urinretention som kräver kateterisering . Rektal undersökning visar inflammation i prostata . I Thailand utvecklar 30% av de infekterade barnen parotidabcesser. Encefalomyelit kan förekomma hos friska människor utan riskfaktorer. De med melioidos -encefomyelit tenderar att ha normala datortomografiska skanningar, men ökad T2 -signal genom magnetisk resonansavbildning , som sträcker sig till hjärnstammen och ryggmärgen . Kliniska tecken inkluderar: ensidig övre motoriska neuron lem svaghet, cerebellära tecken och kranial nerv pares ( VI , VII nerv pares och bulbar pares ). Vissa fall uppvisade enbart slapp förlamning . I norra Australien hade alla melioidos med fall av encefalomyelit förhöjda vita blodkroppar i cerebrospinalvätskan (CSF), mestadels mononukleära celler med förhöjt CSF -protein.
Kronisk
Kronisk melioidos definieras vanligtvis av symptom som varar längre än två månader och förekommer hos cirka 10% av patienterna. Kliniska presentationer inkluderar feber, viktminskning och produktiv hosta med eller utan blodig sputum, vilket kan efterlikna tuberkulos . Dessutom kan långvariga bölder på flera kroppsställen också förekomma. Tuberkulos bör övervägas om lymfkörtlar förstoras vid lungroten . Kronisk melioidos kan uppstå med kaviterande lunginflammation som liknar kronisk lungtuberkulos. Lunginflammation orsakad av melioidos orsakar sällan ärrbildning och förkalkning av lungorna, till skillnad från tuberkulos.
Latent
Vid latent infektion kan immunkompetenta personer rensa infektionen utan att visa några symptom, men mindre än 5% av alla melioidosfall har aktivering efter en tids latens. Patienter med latent melioidos kan vara symptomfria i årtionden. Inledningsvis var den längsta perioden mellan förmodad exponering och klinisk presentation tros vara 62 år i andra världskriget krigsfånge i Burma-Thailand-Malaysia. Efterföljande genotypning av bakterieisolatet från en veteran från Vietnamkriget visade dock att isolatet kanske inte kom från Sydostasien , utan från Sydamerika. Detta återinför en annan rapport som satte den längsta latensperioden för melioidos till 29 år. Potentialen för långvarig inkubation erkändes hos amerikanska soldater som var inblandade i Vietnamkriget och kallades "Vietnam-tidsbomben". I Australien är den längsta registrerade latensperioden 24 år. Olika komorbiditeter som diabetes, njursvikt och alkoholism kan predisponera för återaktivering av melioidos.
Orsak
Bakterie
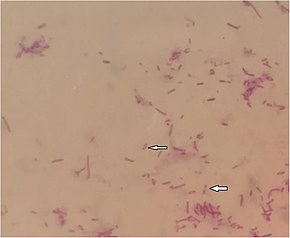
Melioidos orsakas av en gramnegativ, rörlig, saprofytisk bakterie som heter Burkholderia pseudomallei . Bakterien kan också vara en opportunistisk , fakultativ intracellulär patogen. Det är också aerobt och oxidastest positivt. En vakuol i mitten av bakterien får den att likna en "säkerhetsnål" när Gram färgas. Bakterierna avger en stark jordlukt efter 24 till 48 timmars tillväxt i kulturen. B. pseudomallei producerar en glycocalyx polysackarid kapsel som gör den resistent mot många typer av antibiotika. Det är generellt resistent mot gentamicin och kolistin , men känsligt för amoxicillin/klavulansyra (co-amoxiclav). B. pseudomallei är en biosäkerhetsnivå 3 -patogen, som kräver specialiserad laboratoriehantering. I djur, en annan liknande organism namnges Burkholderia mallei är det kausativa medlet av de sjukdoms rots . B. pseudomallei kan särskiljas från en annan närbesläktad, men mindre patogen art, B. thailandensis , genom dess förmåga att assimilera arabinos . B. pseudomallei är mycket anpassningsbar till olika värdmiljöer, allt från mykorrhizala svampsporer till amöbor . Dess anpassningsförmåga kan ge den en överlevnadsfördel i människokroppen.
Genom för B. pseudomallei består av två replikoner : kromosom 1 kodar för bakteriernas hushållsfunktioner såsom cellväggssyntes, rörlighet och metabolism; kromosom 2 kodar funktioner som gör att bakterierna kan anpassa sig till olika miljöer. Horisontell genöverföring bland bakterier har resulterat i mycket varierande genom i B. pseudomallei . Australien har föreslagits som den tidiga reservoaren för B. pseudomallei på grund av den höga genetiska variationen hos bakterierna som finns i denna region. Bakterier isolerade från Afrika och Central- och Sydamerika verkar ha en gemensam förfader som levde på 1600- till 1800 -talen. B. mallei är en klon av B. pseudomallei som har förlorat betydande delar av sitt arvsmassa genom att den anpassats för att leva uteslutande hos däggdjur.
Överföring
B. pseudomallei finns normalt i mark och ytvatten och är vanligast på jorddjup på 10 cm till 90 cm. Det har hittats i jordar, dammar, vattendrag, pooler, stillastående vatten och risfält. Den kan överleva i näringsfattiga förhållanden som destillerat vatten, ökenjord och näringsfattig jord i mer än 16 år. Det kan också överleva i antiseptiska och tvättmedel, sura miljöer ( pH 4,5 i 70 dagar) och miljöer vid temperaturer från 24 till 32 ° C (72 till 89,6 ° F). Bakterierna överlever inte i närvaro av ultraviolett ljus.
Bakterier kan komma in i kroppen genom sår, inandning och intag av förorenat vatten. Överföring från person till person är extremt sällsynt. Melioidos är en erkänd sjukdom hos djur inklusive katter, hundar, getter, får och hästar. Nötkreatur, vattenbufflar och krokodiler anses vara relativt resistenta mot melioidos trots deras ständiga exponering för infekterat vatten och mark. Fåglar är också resistenta mot melioidos. Överföring från djur till människor är sällsynt.
Otillräcklig klorering av vattenförsörjningen hade förknippats med B. pseudomallei -utbrott i norra och västra Australien. Bakterierna har också hittats i en oklorerad vattenförsörjning på landsbygden i Thailand. Bevattningsvätska förorenad med B -pseudomallei är associerad med nosokomiell sårinfektion på sjukhus. Baserat på hela genomens sekvensering av bakterierna kan människor spela en roll för att flytta B. pseudomallei från plats till plats.
Patogenes
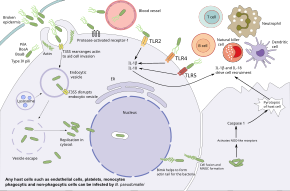
B. pseudomallei har förmågan att infektera olika typer av celler och undvika mänskliga immunsvar. Bakterier kommer först in vid en paus i huden eller slemhinnan och replikerar i epitelcellerna. Därifrån använder de flagellär motilitet för att sprida och infektera olika celltyper. I blodomloppet kan bakterierna infektera både fagocyter och icke -fagocyter. B. pseudomallei använder flagellor för att röra sig nära värdceller och fäster sedan till cellerna med hjälp av olika vidhäftningsproteiner, inklusive pilusprotein av typ IV PilA och vidhäftningsproteiner BoaA och BoaB. Vidare beror vidhäftningen av bakterierna delvis på närvaron av värdproteinet proteasaktiverad receptor-1 , som är närvarande på ytan av endotelceller , trombocyter och monocyter . När de är bundna kommer bakterierna in i värdceller genom endocytos och hamnar inuti en endocytisk vesikel . När blåsan försurar använder B. pseudomallei sitt typ 3 -utsöndringssystem (T3SS) för att injicera effektorproteiner i värdcellen, vilket stör vesikeln och låter bakterierna fly in i värdcytoplasman . Inom värdcytoplasman undviker bakterierna att dödas av värdens autofagi med användning av olika T3SS -effektorproteiner. Bakterierna replikerar i värdcytoplasman.
Inuti värdcellen rör sig bakterierna genom att inducera polymerisationen av värdaktinet bakom dem, vilket driver bakterierna framåt. Denna aktinförmedlade motilitet åstadkommes med autotransportören BimA, som interagerar med aktin vid bakänden av bakterien. Drivs av aktin, bakterierna skjuter mot värdmembranet, vilket skapar utsprång som sträcker sig in i angränsande celler. Dessa utskjutningar får angränsande celler att smälta samman, vilket leder till bildandet av multikärniga jätteceller (MNGC). När MNGC lyser bildar de plack (ett centralt klart område med en ring av sammansmältade celler) som ger skydd för bakterierna för ytterligare replikering eller latent infektion . Samma process i infekterade neuroner kan tillåta bakterier att resa genom nervrötter i ryggmärgen och hjärnan, vilket leder till inflammation i hjärnan och ryggmärgen . Förutom att de sprids från cell till cell kan bakterierna också spridas genom blodomloppet och orsaka sepsis. Bakterierna kan överleva i antigenpresenterande celler och dendritiska celler . Således fungerar dessa celler som bärare som transporterar bakterierna in i lymfsystemet, vilket orsakar utbredd spridning av bakterierna i människokroppen.
Medan B. pseudomallei kan överleva i fagocytiska celler, kan dessa celler döda B. pseudomallei med flera mekanismer. Makrofager aktiverade av interferon gamma har förbättrat dödandet av B. pseudomallei via produktion av inducerbart kväveoxidsyntas . Försurning av endosomen och nedbrytning av bakterierna är också möjlig, dock gör bakteriekapseln och LPS B. pseudomallei resistent mot lysosomal nedbrytning. När B. pseudomallei rymmer in i värdcytosolen kan den igenkännas genom mönsterigenkänningsreceptorer som NOD-liknande receptorer , vilket utlöser bildandet av inflammasomen och aktivering av caspas 1 , vilket inducerar värdcellens död genom pyroptos och ytterligare aktivering av immunsystemet. Flera systemiska värdförsvar bidrar också till immunsvaret. B. pseudomallei utlöser både komplementsystemet och koagulationskaskaden , men den tjocka bakteriekapseln förhindrar verkan av komplementmembranattackkomplexet .
Ytterligare element i immunsystemet aktiveras av värdavgiftsliknande receptorer som TLR2, TLR4 och TLR5 som känner igen de bevarade bitarna av bakterierna som LPS och flagella. Denna aktivering resulterar i produktion av cytokiner såsom interleukin 1 beta (IL-1β) och interleukin 18 (IL-18). IL-18 ökar IFN-produktionen genom naturliga mördarceller , medan IL-1beta minskar IFN-produktionen. Dessa immunmolekyler driver rekryteringen av andra immunceller, såsom neutrofiler , dendritiska celler , B -celler och T -celler till infektionsstället. T -celler verkar vara särskilt viktiga för att kontrollera B. pseudomallei ; T -cellstal ökar hos överlevande och låga T -celltal är förknippade med hög risk för dödsfall av melioidos. Trots detta är HIV -infektion inte en riskfaktor för melioidos. Även om makrofager visar avreglerade cytokinsvar hos personer med HIV -infektion, är bakteriell internalisering och intracellulärt dödande fortfarande effektiva. Personer som är infekterade med B. pseudomallei utvecklar antikroppar mot bakterierna, och människor som bor i endemiska områden tenderar att ha antikroppar i blodet som känner igen B. pseudomallei , men effektiviteten av dessa antikroppar för att förebygga melioidos är oklar.
B. pseudomallei kan förbli latent i människokroppen från 19 till 29 år tills den återaktiveras under immunsuppression eller stressrespons. Bakteriernas plats under latent infektion och den mekanism genom vilken de undviker immunigenkänning i flera år är båda oklara. Bland de föreslagna mekanismerna finns bosättning i cellens kärna för att förhindra att smälta, komma in i ett stadium av långsammare tillväxt, antibiotikaresistens och genetisk anpassning till värdmiljön. Granulom (innehållande neutrofiler, makrofager, lymfocyter och flerkärniga jätteceller) bildade vid infektionsstället vid melioidos har associerats med latent infektion hos människor.
Diagnos
Bakteriekultur är den definitiva diagnosen melioidos. B. pseudomallei är aldrig en del av människans flora. Därför är varje tillväxt av bakterier diagnostiska för melioidos. Blodkulturer är de vanligaste proverna för diagnos, eftersom bakterier kan detekteras i blodet i 50 till 60% av fallen av melioidos. Andra prover, såsom hals, rektala pinnar, pus från bölder och sputum, kan också användas för odling. När bakterier inte växer från personer som starkt misstänks ha melioidos, bör upprepade kulturer tas, eftersom efterföljande kulturer kan bli positiva. B. pseudomallei kan odlas på fårblodagar , MacConkey -agar , Ashdowns medium (innehållande gentamicin ) eller Ashdowns buljong (innehållande kolistin ). Agarplattor för melioidos ska inkuberas vid 37 ° C (98,6 ° F) i luft och inspekteras dagligen i fyra dagar. På agarplattorna bildar B. pseudomallei krämiga, icke -hemolytiska kolonier efter 2 dagars inkubation. Efter 4 dagars inkubation verkar kolonierna torra och skrynkliga. Kolonier av B. pseudomallei som odlas på Francis -medium (en modifiering av Ashdown -medium med gentamicinkoncentration ökad till 8 mg/l) är gula. För laboratorier utanför endemiska områden kan Burkholderia cepacia selektiv agar eller Pseudomonas selektiv agar användas om Ashdowns medium inte är tillgängligt. Det är viktigt att inte tolka bakterietillväxten som Pseudomonas eller Bacillus spp. Andra biokemiska screeningverktyg kan också användas för att detektera B. pseudomallei , inklusive API 20NE eller 20E biokemiskt kit kombinerat med Gram -färgning, oxidastest , typiska tillväxtegenskaper och resistens mot vissa antibiotika hos bakterierna. Molekylära metoder som 16S rDNA -sonder och polymeraskedjereaktion kan också användas för att detektera B. pseudomallei i kultur, men de är endast tillgängliga i forsknings- och referenslaboratorier.
Allmänna blodprov hos personer med melioidos visar låga antal vita blodkroppar (indikerar infektion), förhöjda leverenzymer, ökade bilirubinnivåer (indikerar leversvikt) och förhöjda urea- och kreatininnivåer (indikerar njurfunktion). Lågt blodsocker och acidos förutsäger en sämre prognos hos dem med melioidos. Andra tester såsom C-reaktivt protein och procalcitoninnivåer är emellertid inte tillförlitliga för att förutsäga svårighetsgraden av melioidosinfektion.
Genom mikroskopi ses B. pseudomallei som gramnegativ och stavformad, med en bipolär färgning som liknar en säkerhetsnål. Bakterier kan ibland ses direkt i kliniska prover från infekterade personer, men identifiering med ljusmikroskopi är varken specifik eller känslig . Immunfluorescensmikroskopi är mycket specifik för att detektera bakterier direkt från kliniska prover, men har mindre än 50% känslighet. En lateral flödesimmunanalys har utvecklats men inte utvärderats utförligt. Allt fler laboratorier använder matrisassisterad laserdesorption/joniseringsmasspektrometri för att identifiera bakterierna exakt.
Serologiska tester såsom indirekt hemagglutination har använts för att detektera förekomsten av antikroppar mot B. pseudomallei . Olika grupper av människor har dock mycket olika nivåer av antikroppar, så tolkningen av dessa test beror på plats. I Australien har mindre än 5% av människor B. pseudomallei -antikroppar, så förekomsten av till och med relativt låga mängder antikroppar är ovanlig och kan tyda på melioidos. I Thailand har många människor antikroppar mot B. pseudomallei , så bara en relativt hög mängd antikroppar i blodet tyder på melioidos. Thailand använder också direkt immunofluorescerande antikroppstest (IFAT) och latexagglutination. I IFAT kan både B. pseudomallei -antigen och B. thailandensis användas för att kvantifiera mängden antikroppar som produceras mot bakterierna. Därför måste resultaten tolkas med försiktighet eftersom en falskt positiv reaktion kan hittas om någon tidigare utsatts för icke-patogen B. thailandensis . Latexagglutination är användbar vid screening för misstänkta B. pseudomallei -kolonier. Kommersiella ELISA -kit för melioidos är inte längre tillgängliga på marknaden på grund av låg känslighet för detektering av humana antikroppar.
Olika avbildningsmetoder kan också hjälpa till med diagnosen melioidos. Vid akut melioidos med spridning av bakterierna genom blodomloppet visar röntgen på bröstet multifokala nodulära lesioner. Det kan också visa sammanslagna knölar eller kavitationer . För dem med akut melioidos utan spridning till blodomloppet visar röntgen på bröstet konsolidering av övre lob eller kavitationer. Vid kronisk melioidos liknar den långsamma utvecklingen av övre lobkonsolidering av lungorna tuberkulos. För bölder som finns i andra delar av kroppen förutom lungorna, särskilt i levern och mjälten, har CT -skanning högre känslighet jämfört med en ultraljudsskanning. Vid lever- och mjältabcesser visar en ultraljudsskanning "målliknande" lesioner, medan CT-skanning visar "bikaketecken" i leverabcesser. För melioidos som involverar hjärnan har MR högre känslighet än en CT -skanning vid diagnos av lesionen. MR visar ringförstärkande lesioner för hjärnmelioidos.
Förebyggande
Melioidos är en anmälningspliktig sjukdom i Australien. Detta gör att landet kan övervaka sjukdomsbördan och begränsa utbrott. Melioidos har bara varit ett anmälningspliktigt tillstånd i Thailand sedan juni 2016. Ändå inledde Australien också medvetenhetskampanjer för att öka samhällets förståelse av sjukdomen. I USA kan laboratoriearbetare hantera kliniska prover av B. pseudomallei under BSL-2- förhållanden, medan massproduktion av sådana organismer kräver BSL-3- försiktighetsåtgärder. Dessutom har flera fall av sjukhusförvärvad infektion av melioidos rapporterats, så vårdgivare rekommenderas att utöva handhygien och universella försiktighetsåtgärder .
Storskalig vattenklorering har varit framgångsrik för att minska B. pseudomallei i vattnet i Australien. I medel- till låginkomstländer bör vatten kokas före konsumtion. I höginkomstländer kan vatten behandlas med ultraviolett ljus för dem som riskerar att drabbas av melioidos. De som löper stor risk för kontakt med bakterierna bör bära skyddsutrustning (t.ex. stövlar och handskar) under arbetet. De som bor i endemiska områden bör undvika direktkontakt med jord och utomhusexponering för kraftigt regn eller dammmoln. Flaskvatten eller kokt vatten föredras för att dricka.
Efterexponering förebyggande
Efter exponering för B. pseudomallei (särskilt efter en laboratorieolycka) rekommenderas behandling med co-trimoxazol. Alternativt kan co-amoxiclav och doxycyklin användas för dem som är intoleranta mot co-trimoxazol. Eftersom co-trimoxazol kan orsaka allvarliga biverkningar tenderar endast högriskindivider att få sådana behandlingar. Lågriskindivider skulle i stället få frekvent övervakning.
Vaccination
Flera vaccinkandidater har testats i djurmodeller. Ändå har inga vaccinkandidater prövats hos människor. Större hinder för vaccinerna är begränsad effekt i djurmodeller, fastställande av den bästa metoden för vaccinadministration hos människor och logistiska och ekonomiska frågor vid etablering av mänskliga försök i endemiska områden.
Behandling
Behandlingen av melioidos är uppdelad i två steg, en intravenös intensiv fas och en utrotningsfas för att förhindra återfall. Valet av antibiotika beror på bakteriens känslighet för olika antibiotika. B. pesudomallei är i allmänhet mottaglig för ceftazidim, meropenem, imipenem och co-amoxiclav. Dessa läkemedel är utformade för att döda bakterierna. Det är också mottagligt för doxycyklin, kloramfenikol och co-trimoxazol. Dessa läkemedel är utformade för att hämma tillväxten av bakterierna. Bakterierna är resistenta mot penicillin, ampicillin, första och andra generationens cefalosporin , gentamicin, streptomycin, tobramycin, makrolider och polymyxiner. B. pseudomallei isolat från regionen av Sarawak , Malaysia är känsliga för gentamicin, men.
Intensiv fas
Intravenös ceftazidim är det nuvarande valda läkemedlet för behandling av akut melioidos och bör administreras i minst 10 dagar. Meropenem , imipenem och cefoperazon - sulbactam -kombinationen (Sulperazon) är också effektiva. Intravenöst amoxicillin-klavulanat (co-amoxiclav) får användas om inget av ovanstående fyra läkemedel finns tillgängligt; co-amoxiclav förhindrar döden av melioidos, liksom ceftazidim. Intravenös antibiotika ges i minst 10 dagar. Median feber clearance tid vid melioidos är 9 dagar.
Meropenem är den föredragna antibiotikabehandlingen för neurologisk melioidos och de med septisk chock som läggs in på intensivvårdsavdelningar . Co-trimoxazol rekommenderas vid neurologisk melioidos, osteomyelit, septisk artrit, hud- och gastrointestinal infektion och djupt sittande abscess. För djupgående infektioner som abscesser i inre organ, osteomyelit, septisk artrit och neurologisk melioidos bör antibiotikatiden vara längre (upp till 4 till 8 veckor). Tiden det tar för feber att bli av kan vara mer än 10 dagar hos personer med djup infektion. Resistens mot ceftazidim, karbapenem och co-amoxiclav är sällsynta i intensivfasen, men är mer framträdande under utrotningsterapi. Inga skillnader ses mellan att använda cefoperazon/sulbaktam eller ceftazidim för att behandla melioidos, eftersom båda visar liknande dödsfall och sjukdomsprogression efter behandling. För personer med nedsatt njurfunktion bör dosen ceftazidim, meropenem och co-trimoxazol sänkas. När det kliniska tillståndet förbättrats kan meropenem bytas tillbaka till ceftazidim. Om kombinationsterapin ceftazidim eller meropenem minskar återfallshastigheten i tidig fas av behandlingen är oklart.
Utrotningsfas
Efter behandlingen av den akuta sjukdomen är utrotning (eller underhålls) behandling med co-trimoxazol det valda läkemedlet och ska användas i minst 3 månader. För dem med neurologisk melioidos och osteomyelit bör läkemedel ges i mer än 6 månader. Co-amoxiclav och doxycyklin är andra läkemedel. Co-trimoxazol ska inte användas till personer med glukos-6-fosfatdehydrogenasbrist , eftersom det kan orsaka hemolytisk anemi . Andra biverkningar, såsom utslag, hyperkalemi , nedsatt njurfunktion och gastrointestinala symptom, bör leda till minskning av doserna co-trimoxazol. Kloramfenikol rekommenderas inte längre rutinmässigt för detta ändamål. Co-amoxiclav är ett alternativ för patienter som inte kan ta co-trimoxazol och doxycyklin (t.ex. gravida kvinnor och barn under 12 år), men är inte lika effektiva och har högre återfallshastighet. Enbehandlingsbehandling med fluorokinolon (t.ex. ciprofloxacin ) eller doxycyklin för den orala underhållsfasen är ineffektiv.
I Australien används co-trimoxazol till barn och gravida mödrar efter de första 12 veckorna av graviditeten. Samtidigt, i Thailand, är co-amoxiclav det valda läkemedlet för barn och gravida kvinnor. Emellertid, B. pseudomallei förvärvar ofta motstånd vid samtidig amoxiclav används. Fall har också rapporterats där melioidos framgångsrikt behandlas med co-trimoxazol i 3 månader utan att genomgå intensiv terapi förutsatt att endast hudmanifestationer ses utan inblandning av inre organ eller sepsis. Resistens mot cotrimoxazol är sällsynt i Australien.
Kirurgi
Kirurgisk dränering är indicerad för enstaka, stora abscesser i levern, muskeln och prostata. För flera abscesser i levern, mjälten och njuren är det dock inte möjligt att kirurgisk dränering är nödvändig eller nödvändig. För septisk artrit krävs artrotomitvätt och dränering. Kirurgisk debridering kan vara nödvändig. För dem med mykotisk aneurysm krävs brådskande kirurgi för protetiska kärltransplantat. Livslång terapi med co-trimoxazol kan behövas för personer med protetiska kärltransplantat. Andra bölder behöver sällan dräneras eftersom majoriteten av dem kan lösa sig med antibiotikabehandling. I Australien kan prostataabscess kräva rutinmässig avbildning och dränering.
Andra
Immunmodulerande behandlingar som granulocytkolonistimulerande faktor , Interleukin 7 och anti-PDI ( programmerad celldöd ) kan vara användbara vid behandling av melioidos, särskilt för dem med septisk chock. Detta beror på att dessa läkemedel kan bidra till att öka kroppens immunförsvar mot bakterierna.
Prognos
I väl resurser där sjukdomen kan upptäckas och behandlas tidigt är risken för död 10%. I resursfattiga miljöer är risken att dö av sjukdomen mer än 40%.
För dem med ofullständig behandling, återkomsten av symtom efter en period av sjukdom remission ( " utbrott ") kan förekomma. Därefter krävs sjukhusintag för intravenös antibiotika. För dem som har avslutat behandlingen framgångsrikt kan återfall också uppstå på grund av rekrudens eller ny melioidosinfektion. Med bättre terapier har rekrudensfrekvensen minskat från 10 till 5%. Den nya infektionen är nu vanligare än rekrudens. Riskfaktorer för recrudencens inkluderar sjukdomens svårighetsgrad (patienter med positiva blodkulturer eller multifokal sjukdom har högre risk för återfall), val av antibiotika för utrotningsterapi (doxycyklinmonoterapi och fluorokinolonbehandling är inte lika effektiva), dålig efterlevnad av utrotningsterapi och utrotningsterapiens varaktighet mindre än 8 veckor.
Underliggande medicinska tillstånd som diabetes mellitus, kronisk njursjukdom och cancer kan förvärra den långsiktiga överlevnaden och funktionsnedsättningen för dem som återhämtar sig från infektion. Den allvarligaste komplikationen av melioidos är encefalomyelit . Det kan orsaka quadriparesis (muskelsvaghet i alla lemmar), delvis slapp parapares (muskelsvaghet i båda benen) eller fotfall. För dem med tidigare melioidosassocierade ben- och ledinfektioner kan komplikationer såsom sinusinfektion , ben- och leddeformiteter uppstå med begränsat rörelseomfång.
Epidemiologi
Melioidos är en undersökt sjukdom som förblir endemisk i utvecklingsländer. År 2015 bildades International Melioidosis Society för att öka medvetenheten om sjukdomen. 2016 utvecklades en statistisk modell som visade att antalet är 165 000 fall per år med 138 000 av dem som förekommer i östra och södra Asien och Stilla havet. I ungefär hälften av dessa fall (54% eller 89 000) kommer människor att dö. Underrapportering är ett vanligt problem eftersom endast 1300 fall rapporterades över hela världen sedan 2010, vilket är mindre än 1% av den beräknade incidensen baserat på modelleringen. Brist på laboratoriediagnostik och bristande medvetenhet om sjukdomen hos vårdgivare orsakar också underdiagnostik. Även om bakteriekulturer blir positiva för B. pesudomallei kan de kasseras som föroreningar, särskilt i laboratorier i icke-endemiska områden. Från och med 2018 ingår inte melioidos i WHO: s lista över försummade tropiska sjukdomar .
Melioidos är endemisk i delar av Sydostasien (inklusive Thailand, Laos, Singapore, Brunei, Malaysia, Myanmar och Vietnam), södra Kina, Taiwan och norra Australien. Kraftiga nederbörd kan öka sin omfattning i centrala Australien. Indien och sporadiska fall i Sydamerika. Den verkliga bördan av melioidos i Afrika och Mellanöstern är fortfarande okänd på grund av låg mängd data. Det fanns 24 afrikanska länder och tre länder i Mellanöstern som förutspås vara endemiska med melioidos, men inte ett enda fall rapporterades från dem. Totalt 51 fall av melioidos rapporterades i Bangladesh från 1961–2017. Men brist på medvetenhet och resurser ger upphov till underdiagnostik av sjukdomen i landet. I USA har två historiska fall (1950 och 1971) och tre senaste fall (2010, 2011, 2013) rapporterats bland personer som inte rest utomlands. Trots omfattande undersökningar bekräftades aldrig källan till melioidos. En möjlig förklaring är att import av medicinska växtprodukter eller exotiska reptiler kunde ha resulterat i införandet av melioidos i USA. I Europa importeras mer än hälften av melioidosfall från Thailand.
Melioidos finns i alla åldersgrupper. För Australien och Thailand är medianåldern av infektionen 50 år; 5 till 10% av patienterna är mindre än 15 år. Den enskilt viktigaste riskfaktorn för att utveckla melioidos är diabetes mellitus, följt av farligt alkoholbruk, kronisk njursjukdom och kronisk lungsjukdom. Mer än 50% av personer med melioidos har diabetes; diabetiker har en 12-faldig ökad risk att drabbas av melioidos. Diabetes minskar makrofagernas förmåga att bekämpa bakterierna och minskar produktionen av T -hjälpceller . Överdriven frisättning av tumörnekrosfaktor alfa och interleukin 12 av mononukleära celler ökar risken för septisk chock. Diabetesläkemedlet glibenklamid kan också störa monocytens inflammatoriska svar. Andra riskfaktorer inkluderar talassemi , yrkesmässig exponering (t.ex. risodlare ), rekreationsexponering för mark, vatten, hane, ålder över 45 år och långvarig steroidanvändning/immunsuppression, men 8% av barnen och 20% av vuxna med melioidos har inga riskfaktorer. HIV -infektion disponerar inte för melioidos. Spädbarnsfall har rapporterats möjligen på grund av överföring från mor till barn, infektion i samhället eller sjukvårdsrelaterad infektion. De som mår bra kan också smittas av B. pseudomallei . Till exempel började 25% av barn som vistas i endemiska områden producera antikroppar mot B. pseudomallei mellan 6 månader och 4 år, vilket tyder på att de utsattes för det under denna tid. Detta innebär att många människor utan symptom kommer att testa positivt i serologitester i endemiska områden. I Thailand överstiger seropositiviteten 50%, medan i Australien är seropositiviteten bara 5%. Sjukdomen är tydligt förknippad med ökad nederbörd, med antalet fall som ökar efter ökad nederbörd. Kraftigt nederbörd ökar koncentrationen av bakterierna i matjorden, vilket ökar risken för att bakterierna överförs genom luften.
Historia
Patologen Alfred Whitmore och hans assistent Krishnaswami rapporterade först melioidos bland tiggare och morfinmissbrukare vid obduktion i Rangoon, nuvarande Myanmar , i en rapport som publicerades 1912. Arthur Conan Doyle kan ha läst rapporten från 1912 innan han skrev en novell som involverade den fiktiva tropisk sjukdom "Tapanuli -feber" i ett Sherlock Holmes -äventyr. I historien om " The Dying Detective " från 1913 fick Holmes en låda utformad för att inokulera offret med "Tapanuli -feber" vid öppnandet. "Tapanulifeber" ansågs av många representera melioidos. Begreppet ”melioidos” myntades första gången 1921. Det skilde sig från glanders, en sjukdom hos människor och djur som är liknande i presentationen, men orsakad av en annan mikroorganism. B. pseudomallei , även känd som Whitmore -basillen, identifierades 1917 i Kuala Lumpur . Det första mänskliga fallet av melioidos rapporterades i Sri Lanka 1927. År 1932 rapporterades 83 fall i Syd- och Sydostasien med 98% dödlighet. År 1936 rapporterades det första fallet av melioidos hos djur (får) i Madagaskar, Sydafrika. År 1937 identifierades jord och vatten som livsmiljöer för B. pseudomallei . Under Vietnamkriget från 1967 till 1973 rapporterades 343 amerikanska soldater med melioidos, med cirka 50 fall överförda genom inandning. Ett utbrott av melioidos vid Paris Zoo på 1970 -talet (känd som L'affaire du jardin des plantes ) tros ha härstammat från en importerad panda eller hästar från Iran. Det första beviset på B. pseudomallei (i jord) i Brasilien rapporterades 1983.
Före 1989 var standardbehandlingen för akut melioidos en kombination av tre läkemedel av kloramfenikol, co-trimoxazol och doxycyklin; denna behandling är associerad med en dödlighet på 80% och används inte längre om inte andra alternativ finns tillgängliga. Alla tre läkemedlen är bakteriostatiska (de stoppar bakterien från att växa, men dödar inte den) och verkan av co-trimoxazol motverkar både kloramfenikol och doxycyklin. Aerosoliserad B. pseudomallei isolerades första gången 1989. Samma år hade ceftazidim visat sig minska risken för död av melioidos från 74% till 37%. B. pseudomallei klassificerades tidigare som en del av släktet Pseudomonas fram till 1992. År 1992 fick patogenen formellt namnet B. pseudomallei . Namnet melioidos härrör från det grekiska melis (μηλις) som betyder "en ångest av åsnor" med suffixen -oid som betyder "liknande" och -osis som betyder "ett tillstånd", det vill säga ett tillstånd som liknar körtlar. År 2002 klassificerades B. pseudomallei som en "kategori B -agent". Ett levande försvagat vaccin utvecklades på möss samma år. År 2003 utvecklades multilokus sekvensskrivning för B. pseudomallei . År 2012 klassificerades B pseudomallei som ett "tier-1 select agent" av de amerikanska centra för sjukdomskontroll. 2014 etablerades co-trimoxazol som oral utrotningsterapi. År 2015 detekterades B. pseudomallei -DNA i filtrerad luft med hjälp av kvantitativ PCR. 2016 utvecklades en statistisk modell för att förutsäga förekomsten av global melioidos per år. År 2017 föreslog hela genom -sekvensering Australien som den tidiga reservoaren för melioidos.
Synonymer
- Pseudoglandare
- Whitmores sjukdom (efter kapten Alfred Whitmore , som först beskrev sjukdomen)
- Nightcliff gardeners sjukdom ( Nightcliff är en förort till Darwin, Australien där melioidos är endemisk)
- Fältsjukdom
- Morphia injektors septikemi
Biologisk krigföring
Intresset för melioidos har uttryckts eftersom det har potential att utvecklas som ett biologiskt vapen . En annan liknande bakterie, B. mallei , användes av tyskarna under första världskriget för att infektera boskap som skickades till de allierade länderna. Avsiktlig infektion av mänskliga krigsfångar och djur som använder B. mallei utfördes i Kinas Pingfang -distrikt av japanerna under andra världskriget. Den Sovjetunionen enligt uppgift använt B. mallei under afghansk-sovjetiska kriget 1982 och 1984. B. pseudomallei , som B. mallei , studerades av både USA och Sovjetunionen som en potentiell biologisk krigföring agent, men aldrig weaponized. Andra länder som Iran, Irak, Nordkorea och Syrien kan ha undersökt B. pseudomalleis egenskaper för biologiska vapen. Bakterien är lätt tillgänglig i miljön och är kostnadseffektiv att producera. Det kan också aerosoliseras och överföras via inandning. Men B. pseudomallei har aldrig använts i biologisk krigföring.
Referenser
externa länkar
| Klassificering | |
|---|---|
| Externa resurser |
- Burkholderia pseudomallei genomer och relaterad information på PATRIC , ett bioinformatik resurscenter finansierat av NIAID
- Monografi om melioidos ( ISBN 978-0-444-53479-8 ); Elsevier Press, 2012, https://www.researchgate.net/publication/354857974_Monograph_Melioidosis-a-century-of-observation-and-research_ISBN_978-0-444-53479-8