Programmerad celldöd - Programmed cell death
Programmerad celldöd ( PCD ; ibland kallad cellulärt självmord ) är den död av en cell som ett resultat av händelser inuti i en cell, såsom apoptos eller autophagy . PCD utförs i en biologisk process , som vanligtvis ger fördelar under en organism livscykel . Till exempel uppstår differentiering av fingrar och tår i ett utvecklande mänskligt embryo eftersom celler mellan fingrarna apoptoser ; resultatet är att siffrorna är separata. PCD tjänar grundläggande funktioner under både växt och djurvävnad utveckling.
Apoptos och autofagi är båda formerna av programmerad celldöd. Nekros är döden av en cell orsakad av yttre faktorer som trauma eller infektion och förekommer i flera olika former. Nekros sågs länge som en icke-fysiologisk process som uppstår som ett resultat av infektion eller skada, men på 2000-talet erkändes en form av programmerad nekros, kallad nekroptos , som en alternativ form av programmerad celldöd. Det antas att nekroptos kan fungera som en cell-death backup till apoptos när apoptos-signalen blockeras av endogena eller exogena faktorer som virus eller mutationer. Senast har andra typer av reglerad nekros också upptäckts, som delar flera signalhändelser med nekroptos och apoptos.
Historia
Begreppet "programmerad celldöd" användes av Lockshin & Williams 1964 i förhållande till insektsvävnadsutveckling, cirka åtta år innan "apoptos" myntades. Termen PCD har dock varit en källa till förvirring och Durand och Ramsey har utvecklat konceptet genom att tillhandahålla mekanistiska och evolutionära definitioner. PCD har blivit de allmänna termerna som hänvisar till alla de olika typerna av celldöd som har en genetisk komponent.
Den första inblick i mekanismen kom från att studera BCL2 , en produkt av en förmodad onkogen aktiveras av kromosomtransloka finns ofta i follikulärt lymfom . Till skillnad från andra cancergener, som främjar cancer genom att stimulera cellproliferation, främjade BCL2 cancer genom att stoppa lymfomceller från att kunna döda sig själva.
PCD har varit föremål för ökad uppmärksamhet och forskningsinsatser. Denna trend har lyfts fram med tilldelningen av 2002 års Nobelpris i fysiologi eller medicin till Sydney Brenner ( Storbritannien ), H. Robert Horvitz (USA) och John E. Sulston (Storbritannien).
Typer

- Apoptos eller celldöd av typ I.
- Autofagisk eller celldöd av typ II. ( Cytoplasmatisk : kännetecknas av bildandet av stora vakuoler som äter bort organeller i en specifik sekvens innan kärnans förstörelse .)
Apoptos
Apoptos är processen för programmerad celldöd (PCD) som kan uppstå i flercelliga organismer . Biokemiska händelser leder till karakteristiska cellförändringar ( morfologi ) och död. Dessa förändringar innefattar blebbing , cellkrympning, nukleär fragmentering, kromatinkondensation , och kromosomala DNA fragmentering. Man tror nu att celler i ett utvecklingssammanhang induceras att positivt begå självmord medan de är i ett homeostatiskt sammanhang; frånvaron av vissa överlevnadsfaktorer kan ge upphov till självmord. Det verkar finnas en viss variation i morfologin och faktiskt biokemin för dessa självmordsvägar; vissa trampar vägen för "apoptos", andra följer en mer generaliserad väg till radering, men båda är vanligtvis genetiskt och syntetiskt motiverade. Det finns vissa tecken på att vissa symtom på "apoptos", såsom endonukleasaktivering, kan framkallas falskt utan att ingå i en genetisk kaskad, dock måste sannolikt sann apoptos och programmerad celldöd vara genetiskt medierad. Det blir också klart att mitos och apoptos växlas eller kopplas på något sätt och att den uppnådda balansen beror på signaler från lämpliga tillväxt- eller överlevnadsfaktorer.
Autofagi
Makroautofagi , ofta kallad autofagi , är en katabolisk process som resulterar i autofagosomisk - lysosomal nedbrytning av bulkcytoplasmatiskt innehåll, onormala proteinaggregat och överskott eller skadade organeller .
Autofagi aktiveras i allmänhet av näringsbrist, men har också associerats med såväl fysiologiska som patologiska processer som utveckling, differentiering, neurodegenerativa sjukdomar , stress , infektion och cancer .
Mekanism
En kritisk regulator för autofaginduktion är kinas mTOR , som när det aktiveras undertrycker autofagi och när det inte aktiveras främjar det. Tre relaterade serin / treoninkinaser , UNC -51 -liknande kinas -1, -2 och -3 (ULK1, ULK2, UKL3), som spelar en liknande roll som jästen Atg1 , verkar nedströms mTOR -komplexet. ULK1 och ULK2 bilda en stor komplex med däggdjurshomologen av en autophagy relaterade (Atg) genprodukt (mAtg13) och scaffold protein FIP200. Klass III PI3K-komplex, innehållande hVps34, Beclin-1 , p150 och Atg14-liknande protein eller ultraviolett bestrålningsresistensassocierad gen (UVRAG), krävs för att inducera autofagi.
De ATG- gener styr autophagosome bildning genom ATG12 - ATG5 och LC3-II ( ATG8 -II) komplex. ATG12 konjugeras till ATG5 i en ubiquitinliknande reaktion som kräver ATG7 och ATG10 . Konjugatet Atg12 – Atg5 interagerar sedan icke-kovalent med ATG16 för att bilda ett stort komplex. LC3/ ATG8 klyvs vid sin C-terminal av ATG4- proteas för att generera det cytosoliska LC3-I. LC3-I konjugeras till fosfatidyletanolamin (PE) också i en ubiquitinliknande reaktion som kräver Atg7 och Atg3. Den lipiderade formen av LC3, känd som LC3-II, är fäst vid autofagosommembranet.
Autofagi och apoptos är kopplade både positivt och negativt, och omfattande överhörning finns mellan de två. Under näringsbrist , autophagy fungerar som en pro-överlevnadsmekanism, emellertid, överdriven autophagy kan leda till celldöd , en process morfologiskt distinkt från apoptos . Flera pro-apoptotiska signaler , såsom TNF , TRAIL och FADD , inducerar också autofagi. Dessutom hämmar Bcl-2 Beclin-1- beroende autofagi, och fungerar därmed både som en pro-survival och som en anti-autofagisk regulator.
Andra typer
Förutom ovanstående två typer av PCD har andra vägar upptäckts. Kallas "icke-apoptotisk programmerad celldöd" (eller " caspas- oberoende programmerad celldöd" eller "nekroptos"), dessa alternativa vägar till döden är lika effektiva som apoptos och kan fungera som antingen reservmekanismer eller huvudtypen av PCD .
Andra former av programmerad celldöd inkluderar anoikis , nästan identiska med apoptos utom i dess induktion; cornification , en form av celldöd exklusiv för ögonen; excitotoxicitet ; ferroptos , en järnberoende form av celldöd och Wallerian degeneration .
Nekroptos är en programmerad form av nekros eller inflammatorisk celldöd. Konventionellt är nekros associerad med oprogrammerad celldöd till följd av cellskada eller infiltration av patogener, i motsats till ordnad, programmerad celldöd via apoptos . Nemos är en annan programmerad form av nekros som sker i fibroblaster .
Eryptos är en form av suicidal erytrocytdöd .
Aponekros är en hybrid av apoptos och nekros och hänvisar till en ofullständig apoptotisk process som avslutas med nekros.
NETosis är processen för celldöd som genereras av NET .
Paraptos är en annan typ av nonapoptotisk celldöd som förmedlas av MAPK genom aktivering av IGF-1 . Det kännetecknas av den intracellulära bildningen av vakuoler och svullnad av mitokondrier.
Pyroptos , en inflammatorisk typ av celldöd, medieras unikt av caspas 1 , ett enzym som inte är involverat i apoptos, som svar på infektion av vissa mikroorganismer.
Växtceller genomgår särskilda processer för PCD liknande autofagisk celldöd. Vissa gemensamma särdrag hos PCD är dock mycket bevarade i både växter och metazoa.
Atrofiska faktorer
En atrofisk faktor är en kraft som får en cell att dö . Endast naturliga krafter på cellen anses vara atrofiska faktorer, medan till exempel medel för mekaniskt eller kemiskt missbruk eller lys av cellen anses inte vara atrofiska faktorer. Vanliga typer av atrofiska faktorer är:
- Minskad arbetsbörda
- Förlust av innervering
- Minskad blodtillförsel
- Otillräcklig näring
- Förlust av endokrin stimulering
- Senilitet
- Kompression
Roll i utvecklingen av nervsystemet
Den inledande expansionen av det utvecklande nervsystemet motverkas av avlägsnandet av neuroner och deras processer. Under utvecklingen av nervsystemet avlägsnas nästan 50% av de neuroner som utvecklas naturligt genom programmerad celldöd (PCD). PCD i nervsystemet först erkändes 1896 av John Beard. Sedan dess har flera teorier föreslagits för att förstå dess biologiska betydelse under neural utveckling .
Roll i neural utveckling
PCD i det utvecklande nervsystemet har observerats i prolifererande såväl som post-mitotiska celler. En teori antyder att PCD är en adaptiv mekanism för att reglera antalet stamceller . Hos människor börjar PCD i stamceller vid graviditetsvecka 7 och kvarstår till första trimestern. Denna process med celldöd har identifierats i de germinala områdena i cerebral cortex , cerebellum , thalamus , hjärnstam och ryggmärg bland andra regioner. Under graviditetsveckorna 19–23 observeras PCD i post-mitotiska celler. Den rådande teorin som förklarar denna observation är den neurotrofiska teorin som säger att PCD krävs för att optimera förbindelsen mellan neuroner och deras afferenta ingångar och efferenta mål. En annan teori föreslår att utvecklings -PCD i nervsystemet sker för att korrigera för fel i neuroner som har migrerat ektopiskt, innerverat felaktiga mål eller har axoner som har gått snett under sökandet av vägar. Det är möjligt att PCD under utvecklingen av nervsystemet tjänar olika funktioner som bestäms av utvecklingsstadiet, celltyp och till och med art.
Den neurotrofiska teorin
Den neurotrofiska teorin är den ledande hypotesen som används för att förklara vilken roll programmerad celldöd spelar i nervsystemet. Den postulerar att för att säkerställa optimal innervering av mål produceras först ett överskott av neuroner som sedan tävlar om begränsade mängder skyddande neurotrofiska faktorer och endast en bråkdel överlever medan andra dör av programmerad celldöd. Vidare säger teorin att förutbestämda faktorer reglerar mängden neuroner som överlever och storleken på den innerverande neuronala populationen korrelerar direkt med påverkan av deras målfält.
Den bakomliggande tanken att målceller utsöndrar attraktiva eller inducerande faktorer och att deras tillväxtkottar har en kemotaktisk känslighet presenterades först av Santiago Ramon y Cajal 1892. Cajal presenterade idén som en förklaring till den "intelligenta kraft" som axoner tycks ta när hitta sitt mål men erkände att han inte hade några empiriska data. Teorin fick mer attraktion när experimentell manipulation av axonmål gav döden för alla innerverande neuroner. Detta utvecklade konceptet målavledd reglering som blev huvudprincipen i den neurotrofiska teorin. Experiment som ytterligare stödde denna teori ledde till identifiering av den första neurotrofiska faktorn, nervtillväxtfaktor (NGF).
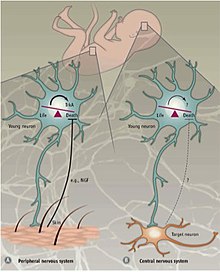
Perifert kontra centrala nervsystemet
Olika mekanismer reglerar PCD i det perifera nervsystemet (PNS) kontra centrala nervsystemet (CNS). I PNS är innerveringen av målet proportionell mot mängden av de målfrisatta neurotrofiska faktorerna NGF och NT3 . Uttryck av neurotrofinreceptorer, TrkA och TrkC , är tillräckligt för att inducera apoptos i frånvaro av deras ligander . Därför spekuleras det i att PCD i PNS är beroende av frisläppandet av neurotrofiska faktorer och följaktligen följer begreppet neurotrofisk teori.
Programmerad celldöd i CNS är inte beroende av externa tillväxtfaktorer utan är istället beroende av inneboende signaler. I neocortex upprätthålls ett 4: 1 -förhållande mellan excitatoriska och hämmande interneuroner av apoptotiska maskiner som verkar vara oberoende av miljön. Stödjande bevis kom från ett experiment där interneuron -stamfäder antingen transplanterades i musens neocortex eller odlades in vitro . Transplanterade celler dog vid två veckors ålder, samma ålder som endogena interneuroner genomgår apoptos. Oavsett transplantationens storlek förblev andelen celler som genomgår apoptos konstant. Dessutom påverkade inte störningen av TrkB , en receptor för neurotrofisk faktor från hjärnan (Bdnf), celldöd. Det har också visat sig att hos möss som är null för den proapoptotiska faktorn Bax (Bcl-2-associerat X-protein) överlevde en större andel internuroner jämfört med möss av vildtyp. Tillsammans tyder dessa fynd på att programmerad celldöd i CNS delvis utnyttjar Bax-medierad signalering och är oberoende av BDNF och miljön. Apoptotiska mekanismer i CNS är fortfarande inte väl förstådda, men man tror att apoptos av interneuroner är en självautonom process.
Utveckling av nervsystemet i dess frånvaro
Programmerad celldöd kan reduceras eller elimineras i nervsystemet som utvecklas genom riktad radering av pro-apoptotiska gener eller genom överuttryck av anti-apoptotiska gener. Frånvaro eller minskning av PCD kan orsaka allvarliga anatomiska missbildningar men kan också resultera i minimala konsekvenser beroende på genen som riktas, neuronpopulationen och utvecklingsstadiet. Överskott av proliferation av stamceller som leder till grova hjärnabnormaliteter är ofta dödlig, vilket kan ses hos caspase-3 eller caspase-9 knockout-möss som utvecklar exencefali i framhjärnan . Hjärnstammen, ryggmärgen och perifera ganglier hos dessa möss utvecklas normalt men tyder på att caspasas inblandning i PCD under utvecklingen beror på hjärnregionen och celltypen. Knockout eller hämning av apoptotisk proteasaktiverande faktor 1 ( APAF1 ) resulterar också i missbildningar och ökad embryonal dödlighet. Manipulation av apoptosregulatorproteiner Bcl-2 och Bax (överuttryck av Bcl-2 eller radering av Bax) ger en ökning av antalet neuroner i vissa regioner i nervsystemet, såsom näthinnan , trigeminalkärnan , cerebellum och ryggmärgen. PCD av neuroner på grund av Bax-borttagning eller Bcl-2-överuttryck resulterar dock inte i framträdande morfologiska eller beteendemässiga avvikelser hos möss. Till exempel har möss som överuttrycker Bcl-2 i allmänhet normala motoriska färdigheter och syn och visar bara försämring i komplexa beteenden som inlärning och ångest. De normala beteendemässiga fenotyperna hos dessa möss tyder på att en adaptiv mekanism kan vara involverad för att kompensera för överskott av neuroner.
Ryggradslösa djur och ryggradsdjur
Att lära sig om PCD hos olika arter är viktigt för att förstå den evolutionära grunden och orsaken till apoptos i utvecklingen av nervsystemet. Under utvecklingen av det ryggradslösa nervsystemet spelar PCD olika roller hos olika arter. Likheten hos den asymmetriska celldödsmekanismen i nematoden och iglen indikerar att PCD kan ha en evolutionär betydelse i utvecklingen av nervsystemet. I nematoden inträffar PCD under den första timmen av utveckling som leder till eliminering av 12% av icke-gonadala celler inklusive neuronala linjer. Celldöd hos leddjur sker först i nervsystemet när ektodermceller differentieras och en dottercell blir en neuroblast och den andra genomgår apoptos. Dessutom leder könsinriktad celldöd till olika neuronal innervering av specifika organ hos män och kvinnor. I Drosophila är PCD avgörande för segmentering och specifikation under utveckling.
I motsats till ryggradslösa djur har mekanismen för programmerad celldöd befunnits vara mer bevarad hos ryggradsdjur . Omfattande studier utförda på olika ryggradsdjur visar att PCD av neuroner och glia förekommer i de flesta delar av nervsystemet under utvecklingen. Det har observerats före och under synaptogenes i centrala nervsystemet såväl som i det perifera nervsystemet. Det finns dock några skillnader mellan ryggradsdjur. Till exempel uppvisar däggdjur omfattande arborisering följt av PCD i näthinnan medan fåglar inte gör det. Även om synaptisk förfining i ryggradsdjurssystem till stor del är beroende av PCD spelar andra evolutionära mekanismer också en roll.
I växtvävnad
Programmerad celldöd i växter har ett antal molekylära likheter med djurapoptos , men det har också skillnader, det mest uppenbara är närvaron av en cellvägg och bristen på ett immunsystem som tar bort bitarna i den döda cellen. I stället för ett immunsvar syntetiserar den döende cellen ämnen för att bryta ner sig och placerar dem i en vakuol som brister när cellen dör.
I "APL reglerar kärlvävnadsidentitet i Arabidopsis " hade Martin Bonke och hans kollegor uppgett att det ena av de två långväga transportsystemen i kärlväxter , xylem , består av flera celltyper "vars differentiering innebär deponering av utarbetade celler -vägg förtjockning och programmerad celldöd. " Författarna betonar att produkterna från växt -PCD spelar en viktig strukturell roll.
Grundläggande morfologiska och biokemiska egenskaper hos PCD har bevarats i både växt- och djurrikena . Specifika typer av växtceller utför unika celldödsprogram. Dessa har gemensamma särdrag med djurapoptos - till exempel kärnkrafts -DNA -nedbrytning - men de har också sina egna särdrag, till exempel kärnkraftsnedbrytning som utlöses av vakuolens kollaps i trakeariska element i xylemet.
Janneke Balk och Christopher J. Leaver, vid institutionen för växtvetenskap , University of Oxford , genomförs forskning om mutationer i mitokondriella genomet av sol-blomma celler. Resultat av denna forskning tyder på att mitokondrier spelar samma nyckelroll i kärlväxt -PCD som i andra eukaryota celler.
PCD i pollen förhindrar inavel
Under pollinering genomdriver växterna självinkompatibilitet ( SI ) som ett viktigt medel för att förhindra självbefruktning . Forskning om majsvalmo ( Papaver rhoeas ) har avslöjat att proteiner i pistill som pollen landar på, interagerar med pollen och utlöser PCD i inkompatibla (dvs. själv ) pollen. Forskarna, Steven G. Thomas och Vernonica E. Franklin-Tong , fann också att svaret innebär snabb inhibering av tillväxten av pollenrör , följt av PCD.
I slemformar
Den sociala slemsvamp Dictyostelium discoideum har den egenheten att antingen anta en predatory amoeba -liknande beteende i sin encellig form eller koalescera till en mobil snigel -liknande formen när dispergering av sporer som kommer att ge upphov till nästa generation .
Stjälken består av döda celler som har genomgått en typ av PCD som delar många funktioner i en autofagisk celldöd: massiva vakuoler som bildas inuti celler, en grad av kromatinkondensation , men ingen DNA-fragmentering . Den strukturella rollen för resterna som lämnas av de döda cellerna påminner om produkterna av PCD i växtvävnad.
D. discoideum är en slemform, en del av en gren som kan ha kommit från eukaryota förfäder ungefär en miljard år före nutiden. Det verkar som att de uppstod efter att förfäderna till gröna växter och förfäderna till svampar och djur hade differentierats. Men, förutom deras plats i det evolutionära trädet , har det faktum att PCD har observerats i den ödmjuka, enkla sexkromosomen D. discoideum ytterligare betydelse: Det tillåter studier av en utvecklings-PCD-väg som inte är beroende av caspaser kännetecknande för apoptos.
Evolutionärt ursprung för mitokondriell apoptos
Förekomsten av programmerad celldöd hos protister är möjlig, men den är fortfarande kontroversiell. Vissa kategoriserar döden i dessa organismer som oreglerad apoptosliknande celldöd.
Biologer hade länge misstänkt att mitokondrier härstammar från bakterier som hade införlivats som endosymbionter ("levande tillsammans inuti") av större eukaryota celler. Det var Lynn Margulis som från 1967 kämpade för denna teori , som sedan har blivit allmänt accepterad. Det mest övertygande beviset för denna teori är det faktum att mitokondrier har sitt eget DNA och är utrustade med gener och replikationsapparater .
Detta evolutionära steg skulle ha varit riskabelt för de primitiva eukaryota cellerna, som började uppsluka de energiproducerande bakterierna, liksom ett farligt steg för mitokondriernas förfäder, som började invadera deras protoukaryota värdar . Denna process är fortfarande uppenbar idag, mellan mänskliga vita blodkroppar och bakterier. För det mesta förstörs invaderande bakterier av de vita blodkropparna; Det är emellertid inte ovanligt att den kemiska krigföring som prokaryoter bedriver lyckas, med följden känd som infektion genom dess resulterande skada.
En av dessa sällsynta evolutionära händelser, ungefär två miljarder år före nutiden, gjorde det möjligt för vissa eukaryoter och energiproducerande prokaryoter att samexistera och ömsesidigt dra nytta av deras symbios .
Mitokondriata eukaryota celler lever stilla mellan liv och död, eftersom mitokondrier fortfarande behåller sin repertoar av molekyler som kan utlösa cellmord. Det är inte klart varför apoptotiska maskiner upprätthålls i de existerande encelliga organismerna. Denna process har nu utvecklats till att hända endast när den är programmerad. till celler (såsom återkoppling från grannar, stress eller DNA-skada ), mitokondrier frigör kaspasaktivatorer som utlöser den celldödsinducerande biokemiska kaskaden. Som sådan är cellmordsmordsmekanismen nu avgörande för alla våra liv.
Programmerad död av hela organismer
Klinisk signifikans
ABL
BCR-ABL-onkogen har visat sig vara involverad i utvecklingen av cancer hos människor.
c-Myc
c-Myc är involverad i reglering av apoptos via dess roll i nedreglering av Bcl-2- genen. Dess roll den störda tillväxten av vävnad.
Metastas
En molekylär egenskap hos metastatiska celler är deras förändrade uttryck av flera apoptotiska gener.
Se även
- Anoikis
- Apoptos-inducerande faktor
- Apoptos kontra pseudoapoptos
- Apoptosom
- Apoptotisk DNA -fragmentering
- Autolys (biologi)
- Autofagi
- Autoschizis
- Bcl-2
- BH3 interagerande domän dödsagonist (BID)
- Calpains
- Caspases
- Cellskada
- Cornification
- Cytokrom c
- Cytotoxicitet
- Diablo homolog
- Entos
- Excitotoxicitet
- Ferroptos
- Inflammatoriskt
- Mitokondriell permeabilitet övergår por
- Mitotisk katastrof
- Nekrobiologi
- Nekroptos
- Nekros
- p53 uppreglerad apoptosmodulator (PUMA)
- Paraptos
- Parthanatos
- Pyroptos
- RIP -kinaser
- Wallerisk degeneration
Anteckningar och referenser
- Srivastava, RE i molekylära mekanismer (Humana Press, 2007).
- Kierszenbaum, AL & Tres, LL (ed Madelene Hyde) (ELSEVIER SAUNDERS, Philadelphia, 2012).