Tyrotoxisk periodisk förlamning - Thyrotoxic periodic paralysis
| Tyrotoxisk periodisk förlamning | |
|---|---|
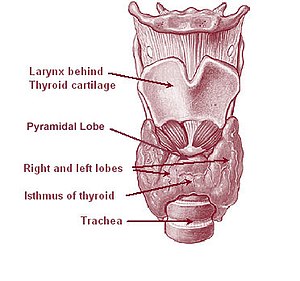 | |
| Tyrotoxisk periodisk förlamning uppstår när sköldkörteln frisätter alltför stora mängder tyroxin (sköldkörtelhormon). | |
| Specialitet | Endokrinologi |
Tyrotoxisk periodisk förlamning ( TPP ) är ett tillstånd med attacker av muskelsvaghet i närvaro av hypertyreos (överaktivitet i sköldkörteln ). Hypokalemi (en minskad kaliumnivå i blodet) förekommer vanligtvis under attacker. Tillståndet kan vara livshotande om svaghet i andningsmusklerna leder till andningssvikt eller om de låga kaliumnivåerna leder till hjärtarytmier (oregelbundenhet i hjärtfrekvensen). Om det inte behandlas är det vanligtvis återkommande.
Tillståndet har kopplats till genetiska mutationer i gener som kodar för vissa jonkanaler som transporterar elektrolyter ( natrium och kalium ) över cellmembran . De viktigaste är L-typ kalciumkanal α1-subenhet och kalium inre likriktare 2.6 ; det klassificeras därför som en kanalopati . Avvikelsen i kanalen tros leda till förskjutningar av kalium till celler , under förhållanden med höga tyroxin (sköldkörtelhormon) nivåer, vanligtvis med ytterligare ett fällningsmedel.
Behandling av hypokalemi, följt av korrigering av hypertyroidism, leder till fullständig lösning av attackerna. Det förekommer främst hos män av kinesisk, japansk, vietnamesisk, filippinsk och koreansk härkomst. TPP är ett av flera tillstånd som kan orsaka periodisk förlamning .
tecken och symtom
En attack börjar ofta med muskelsmärta, kramper och stelhet. Detta följs av svaghet eller förlamning som tenderar att utvecklas snabbt, vanligtvis sent på kvällen eller tidigt på morgonen. Svagheten är vanligtvis symmetrisk; extremiteterna närmare stammen (proximalt) påverkas övervägande, och svaghet tenderar att börja i benen och spridas till armarna. Muskler i mun och hals , ögon och andning påverkas vanligtvis inte, men ibland kan svaghet i andningsmusklerna orsaka livshotande andningssvikt . Attacker löser vanligtvis inom flera timmar till flera dagar, även i avsaknad av behandling. Vid neurologisk undersökning under en attack noteras slap svaghet i armar och ben; reflexer minskas vanligtvis, men sensoriska systemet är opåverkat. Mental status påverkas inte.
Attacker kan orsakas av fysisk ansträngning , dricker alkohol eller äter mat med mycket kolhydrater eller salt . Detta kan förklara varför attacker är vanligare på sommaren när fler dricker söta drycker och tränar. Träningsrelaterade attacker tenderar att inträffa under en viloperiod omedelbart efter träning; träning kan därför rekommenderas för att avbryta en attack.
Det kan finnas symtom på överaktivitet i sköldkörteln, såsom viktminskning , snabb hjärtfrekvens , tremor och svett ; men sådana symtom förekommer i bara hälften av alla fall. Den vanligaste typen av hypertyreoidism, Graves sjukdom , kan dessutom orsaka ögonproblem ( Graves oftalmopati ) och hudförändringar i benen ( pretibialt myxödem ). Sköldkörtelsjukdom kan också orsaka muskelsvaghet i form av tyrotoxisk myopati , men detta är konstant snarare än episodiskt.
Orsaker
Genetik
Genetiska mutationer i kalciumkanalen α1-subenhet av L-typ (Ca v 1.1) har beskrivits på södra kinesiska med TPP. Mutationerna ligger i en annan del av genen än de som beskrivs i det relaterade tillståndet familjär periodisk förlamning . I TPP är de beskrivna mutationerna enstaka nukleotidpolymorfier lokaliserade i hormonresponselementet som reagerar på sköldkörtelhormon, vilket antyder att transkription av genen och produktion av jonkanaler kan förändras genom ökade sköldkörtelhormonnivåer. Vidare har mutationer rapporterats i de gener som kodar för kaliumspänningskänsliga kanal, Shaw-besläktad underfamilj, elementet 4 (K v 3,4) och natriumkanalprotein typ 4 subenhet alfa (Na 4 1,4).
Av personer med TPP visades att 33% från olika populationer hade mutationer i KCNJ18 , genen som kodade för K ir 2,6, en kaliumjonkanal med inre likriktare . Denna gen har också ett sköldkörtelresponselement.
Vissa former av humant leukocytantigen (HLA) - speciellt B46, DR9, DQB1 * 0303, A2, Bw22, AW19, B17 och DRW8 - är vanligare i TPP. Koppling till särskilda former av HLA, som spelar en central roll i immunsvaret , kan innebära en orsak till immunsystemet, men det är osäkert om detta direkt orsakar TPP eller om det ökar mottagligheten för Graves sjukdom, en känd autoimmun sjukdom .
Sköldkörtelsjukdom
Den vanligaste underliggande formen av sköldkörtelsjukdom associerad med TPP är Graves sjukdom, ett syndrom på grund av en autoimmun reaktion som leder till överproduktion av sköldkörtelhormon. TPP har också beskrivits hos personer med andra sköldkörtelproblem såsom tyroidit , toxisk nodulär struma , toxiskt adenom , TSH -producerande hypofysadenom , överdrivet intag av tyroxin eller jod , och amiodaron -inducerad hypertyreos.
Mekanism

Muskelsvaghet och ökad risk för oregelbunden hjärtrytm i TPP beror på markant reducerade nivåer av kalium i blodomloppet. Kalium går faktiskt inte förlorat från kroppen, men ökad Na + / K + -ATPas- aktivitet ( enzymet som förflyttar kalium till celler och håller natrium i blodet) leder till förskjutning av kalium i vävnader och tömmer cirkulationen. I andra typer av kaliumnedbrytning störs syra-basbalansen vanligtvis, med metabolisk alkalos och metabolisk acidos ofta närvarande. I TPP är dessa störningar i allmänhet frånvarande. Hypokalemi leder till hyperpolarisering av muskelceller , vilket gör den neuromuskulära korsningen mindre lyhörd för normala nervimpulser och leder till minskad muskulatur.
Det är inte klart hur de beskrivna genetiska defekterna ökar Na + / K + -ATPas-aktiviteten, men man misstänker att enzymet blir mer aktivt på grund av ökade sköldkörtelhormonnivåer. Hypertyroidism ökar nivåerna av katekolaminer (såsom adrenalin ) i blodet, vilket ökar Na + / K + -ATPas-aktiviteten. Enzymaktiviteten ökar sedan ytterligare av utfällningsorsakerna. Till exempel leder ökat kolhydratintag till ökade insulinnivåer ; detta är känt för att aktivera Na + / K + -ATPase. När fällningsmedlet har avlägsnats återgår enzymaktiviteten till normala nivåer. Man har postulerat att manliga hormoner ökar Na + / K + -ATPas-aktiviteten, och att detta förklarar varför män löper högre risk för TPP trots att sköldkörtelsjukdom är vanligare hos kvinnor.
TPP betraktas som en modell för relaterade tillstånd, känd som "channelopathies", som har kopplats till mutationer i jonkanaler; majoriteten av dessa tillstånd uppträder episodiskt.
Diagnos
Hypokalemi (låga kaliumnivåer i blodet) förekommer ofta under attacker; nivåer under 3,0 mmol / l förekommer vanligtvis. Magnesium- och fosfatnivåer visar sig ofta vara minskade. Kreatinkinasnivåerna är förhöjda i två tredjedelar av fallen, vanligtvis på grund av en viss grad av muskelskada; allvarliga höjder som tyder på rabdomyolys (förstörelse av muskelvävnad) är sällsynta. Elektrokardiografi (EKG / EKG) kan visa takykardi (snabb hjärtfrekvens) på grund av sköldkörtelsjukdom, abnormiteter på grund av hjärtarytmi ( förmaksflimmer , ventrikulär takykardi ) och ledningsförändringar associerade med hypokalemi (U-vågor, QRS-utvidgning, QT-förlängning, och T-vågplattning). Elektromyografi visar förändringar som liknar dem som påträffas i myopatier (muskelsjukdomar), med en minskad amplitud av sammansatta muskelmekanismspotentialer (CMAP); de löser sig när behandlingen har börjat.
TPP skiljer sig från andra former av periodisk förlamning (särskilt hypokalemisk periodisk förlamning ) med sköldkörtelfunktionstester på blodet. Dessa är normala i de andra formerna, och i tyrotoxicos är nivåerna av tyroxin och triiodotyronin förhöjda, med resulterande undertryckande av TSH-produktion av hypofysen . Olika andra undersökningar utförs vanligtvis för att separera de olika orsakerna till hypertyreos .
Behandling
I den akuta fasen av en attack kommer administrering av kalium snabbt att återställa muskelstyrkan och förhindra komplikationer. Men försiktighet rekommenderas eftersom den totala mängden kalium i kroppen inte minskar och det är möjligt för kaliumnivåerna att överskridas ("rebound hyperkalemia "); långsam infusion av kaliumklorid rekommenderas därför medan annan behandling påbörjas.
Effekterna av överskott av sköldkörtelhormon svarar vanligtvis på administrering av en icke-selektiv beta-blockerare , såsom propranolol (eftersom de flesta symtomen drivs av ökade nivåer av adrenalin och dess effekt på β-adrenerga receptorer ). Efterföljande attacker kan förhindras genom att undvika kända fällningsmedel, såsom högt salt- eller kolhydratintag, tills sköldkörtelsjukdomen har behandlats tillräckligt.
Behandling av sköldkörtelsjukdom leder vanligtvis till att paralytiska attacker löses ut. Beroende på sjukdomens natur kan behandlingen bestå av tyrostatika (läkemedel som minskar produktionen av sköldkörtelhormon), radiojod eller ibland sköldkörtelkirurgi.
Epidemiologi
TPP förekommer huvudsakligen hos män av kinesisk, japansk, vietnamesisk, filippinsk och koreansk härkomst, liksom thailändare , med mycket lägre priser hos människor med andra etniciteter. Hos kineser och japaner med hypertyreoidism upplever 1,8-1,9% TPP. Detta står i kontrast till Nordamerika, där studier rapporterar en frekvens på 0,1–0,2%. Indianer , som delar en genetisk bakgrund med östasiatiska, har en ökad risk.
Den typiska startåldern är 20–40. Det är okänt varför män främst påverkas, med frekvenser hos män som är 17- till 70-faldiga hos kvinnor, trots att överaktivitet i sköldkörteln är mycket vanligare hos kvinnor.
Historia
Efter flera fallrapporter på 1700- och 1800-talet beskrivs periodisk förlamning först i sin helhet av den tyska neurologen Carl Friedrich Otto Westphal (1833–1890) 1885. År 1926 observerade den japanska läkaren Tetsushiro Shinosaki från Fukuoka den höga sköldkörtelsjukdom hos japanska personer med periodisk förlamning. Den första engelskspråkiga rapporten 1931 härstammar från Dunlap och Kepler, läkare vid Mayo Clinic ; de beskrev tillståndet hos en patient med drag av Graves sjukdom . År 1937 var periodisk förlamning kopplad till hypokalemi, liksom utfällning av attacker med glukos och insulin. Detta fenomen har använts som ett diagnostiskt test.
1974 upptäcktes att propranolol kunde förhindra attacker. Begreppet kanalopatier och kopplingen till specifika jonkanalmutationer uppstod i slutet av 1900-talet.
Referenser
externa länkar
| Klassificering | |
|---|---|
| Externa resurser |