Insulin (medicinering) - Insulin (medication)
 Injektionsflaskor med insulin
| |
| Kliniska data | |
|---|---|
| Handelsnamn | Humulin, Novolin, Insuman, andra |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a682611 |
| Licensdata | |
| Vägar administrering |
Subkutan, intravenös, intramuskulär, inandad |
| ATC -kod | |
| Rättslig status | |
| Rättslig status | |
| Identifierare | |
| CAS-nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| Kemiska och fysiska data | |
| Molmassa | 5793,5999 g/mol |
| Densitet | 1,09 g / cm 3 |
| Smältpunkt | 233 ° C (451 ° F) |
Insulin är ett proteinhormon som används som medicin för att behandla högt blodsocker . Detta inkluderar diabetes mellitus typ 1 , diabetes mellitus typ 2 , graviditetsdiabetes och komplikationer av diabetes såsom diabetisk ketoacidos och hyperosmolära hyperglykemiska tillstånd . Det används också tillsammans med glukos för att behandla höga blodkaliumnivåer . Vanligtvis ges det genom injektion under huden , men vissa former kan också användas genom injektion i en ven eller muskel .
Den vanliga biverkningen är lågt blodsocker . Andra biverkningar kan inkludera smärta eller hudförändringar på injektionsställena, lågt kaliumnivå i blodet och allergiska reaktioner . Användning under graviditeten är relativt säker för barnet. Insulin kan framställas från bukspottkörteln hos grisar eller kor. Mänskliga versioner kan göras antingen genom att modifiera grisversioner eller rekombinant teknik . Det finns i tre huvudtyper: kortverkande (som vanligt insulin ), mellanverkande (som neutralt protamin Hagedorn (NPH) insulin) och längre verkande (som insulin glargin ).
Insulin användes först som läkemedel i Kanada av Charles Best och Frederick Banting 1922. Det finns på Världshälsoorganisationens lista över viktiga läkemedel . År 2017 var humant insulin det 73: e vanligaste förskrivna läkemedlet i USA, med mer än tio miljoner recept.
Medicinsk användning

Insulin används för att behandla ett antal sjukdomar, inklusive diabetes och dess akuta komplikationer, såsom diabetisk ketoacidos och hyperosmolära hyperglykemiska tillstånd . Det används också tillsammans med glukos för att behandla höga blodkaliumnivåer . Insulin användes tidigare i en psykiatrisk behandling som kallas insulinchockterapi .
Bieffekter
Allergi
Allergi mot insulin påverkade cirka 2% av människorna, varav de flesta reaktionerna inte beror på själva insulinet utan på konserveringsmedel som tillsätts till insulin som zink, protamin och metakresol . De flesta reaktionerna är överkänslighetsreaktioner av typ I och orsakar sällan anafylaksi . En misstänkt allergi mot insulin kan bekräftas genom hudpricktest , plåstestning och ibland hudbiopsi . Första linjens terapi mot insulinöverkänslighetsreaktioner inkluderar symptomatisk behandling med antihistaminer. De drabbade personerna byts sedan till ett preparat som inte innehåller det specifika ämne de reagerar på eller genomgår avkänslighet .
Kutana biverkningar
Upprepad subkutan injektion utan platsrotation kan leda till lipohypertrofi och amyloidom, som manifesteras som fasta påtagliga knölar under huden.
Principer
| Aminosyrasekvens av insulinpreparat | |||||||
|---|---|---|---|---|---|---|---|
| Aminosyraersättningar | |||||||
|
|
A-kedjeposition |
B-kedjeposition |
|||||
| Källa Arter |
A-8 | A-10 | A-21 | B-28 | B-29 | B-30 | B-31 B-32 |
| Nötkreatur | Ala | Val | Asn | Proffs | Lys | Ala | Ej tillgängligt |
| Gris | Thr | Ile | Asn | Proffs | Lys | Ala | Ej tillgängligt |
| Mänsklig | Thr | Ile | Asn | Proffs | Lys | Thr | Ej tillgängligt |
| Aspart (Novolog) | Thr | Ile | Asn | Asp | Lys | Thr | Ej tillgängligt |
| Lispro (Humalog) | Thr | Ile | Asn | Lys | Proffs | Thr | Ej tillgängligt |
| Glulisine (Apidra) | Thr | Ile | Asn | Proffs | Glu | Thr | Ej tillgängligt |
| Glargine (Lantus) | Thr | Ilc | Gly | Proffs | Lys | Thr | Arg |
| Detemir (Levemir) | Thr | Ile | Asn | Proffs | Lys | Ej tillgängligt | Myristinsyra |
| Degludec (Tresiba) | Thr | Ile | Asn | Proffs | Lys | Ej tillgängligt | Hexadekandioinsyra |
|
|
|||||||
Insulin är ett endogent hormon som produceras av bukspottkörteln . Insulinet proteinet har varit mycket konserverad över evolutionär tid, och är närvarande i både däggdjur och ryggradslösa djur . Den insulin/ insulinliknande tillväxtfaktorsignaleringsvägen (IIS) har studerats ingående i arter inklusive nematodmaskar (t.ex. C. elegans ), flugor ( Drosophila melanogaster ) och möss ( Mus musculus ). Dess verkningsmekanismer är mycket lika för olika arter.
Både diabetes mellitus typ 1 och diabetes mellitus typ 2 präglas av en förlust av bukspottkörteln, men i olika grad. Personer som har någon typ av diabetes löper risk för lågt och högt blodsocker , med potentiellt allvarliga konsekvenser. Många människor behöver insulinbehandling för att hantera sina blodsockernivåer och hålla dem inom ett målintervall.
År 1916 lyckades Nicolae C. Paulescu (1869-1931) utveckla ett vattenhaltigt pankreasextrakt som normaliserade en diabeteshund. År 1921 publicerade han 4 artiklar i Society of Biology i Paris med fokus på de framgångsrika effekterna av bukspottskörtelekstraktet hos diabetiker. Forskning om bukspottkörtelns roll i matassimilering av Paulescu publicerades i augusti 1921 i Archives Internationales de Physiologie, Liège, Belgien. Ursprungligen var det enda sättet att få insulin för klinisk användning att extrahera det från bukspottkörteln hos en annan varelse. Djurkörtlar kunde erhållas som en avfallsprodukt från köttförpackningsindustrin. Insulinet härrör främst från kor ( Eli Lilly och Company ) och grisar ( Nordisk Insulinlaboratorium ). Tillverkning av åtta uns renat insulin kan kräva så mycket som två ton grisdelar. Insulin från dessa källor är effektivt hos människor eftersom det är mycket likt humant insulin (tre aminosyror skillnad i nötkreaturinsulin, en aminosyra skillnad i svin). Inledningsvis resulterade lägre preparatrenhet i allergiska reaktioner mot närvaron av icke-insulinsubstanser. Renheten har förbättrats stadigt sedan 1920-talet och i slutändan nådde en renhet på 99% i mitten av 1970-talet tack vare högtrycksvätskekromatografi (HPLC) metoder. Mindre allergiska reaktioner förekommer fortfarande ibland, även till syntetiska "humana" insulinsorter.
Från och med 1982 har biosyntetiskt "humant" insulin tillverkats för klinisk användning genom gentekniska tekniker med användning av rekombinant DNA -teknik. Genentech utvecklade tekniken som användes för att producera det första insulinet Humulin, men marknadsförde inte själva produkten kommersiellt. Eli Lilly marknadsförde Humulin 1982. Humulin var den första medicinen som producerades med hjälp av moderna gentekniska tekniker där verkligt mänskligt DNA sätts in i en värdcell ( E. coli i detta fall). Värdcellerna får sedan växa och reproducera normalt, och på grund av det insatta mänskliga DNA: t producerar de en syntetisk version av humant insulin. Tillverkare hävdar att detta minskar förekomsten av många föroreningar. Emellertid skiljer sig de kliniska preparaten framställda från sådana insuliner från endogent humant insulin i flera viktiga avseenden; ett exempel är frånvaron av C-peptid som under de senaste åren har visat sig ha systemiska effekter i sig. Novo Nordisk har också utvecklat ett genetiskt manipulerat insulin oberoende av en jästprocess.
Enligt en undersökning som International Diabetes Federation genomförde 2002 om tillgång till och tillgänglighet av insulin i sina medlemsländer är cirka 70% av det insulin som för närvarande säljs i världen rekombinant, biosyntetiskt 'humant' insulin. En majoritet av insulin som används kliniskt idag produceras på detta sätt, även om klinisk erfarenhet har gett motstridiga bevis på om dessa insuliner är mindre benägna att producera en allergisk reaktion. Biverkningar har rapporterats; dessa inkluderar förlust av varningstecken på att drabbade kan glida i koma genom hypoglykemi , kramper, minnesförlust och koncentrationsförlust. Internationella diabetesförbundets ställningstagande från 2005 är emellertid mycket tydligt med att "det finns INGET överväldigande bevis för att föredra en insulinsort framför en annan" och "[moderna, mycket renade] djurinsuliner förblir ett helt acceptabelt alternativ."
Sedan januari 2006 är alla insuliner som distribueras i USA och några andra länder syntetiska "mänskliga" insuliner eller deras analoger. En särskild FDA -importprocess krävs för att erhålla insulin från nötkreatur eller svin för användning i USA, även om det kan finnas några återstående lager av svininsulin tillverkat av Lilly 2005 eller tidigare, och svin lente -insulin säljs och marknadsförs också under varumärket namn Vetsulin (SM) i USA för veterinär användning vid behandling av sällskapsdjur med diabetes.
Basalt insulin
Vid typ 1 -diabetes är insulinproduktionen extremt låg, och som sådan kräver kroppen exogent insulin. Vissa personer med typ 2 -diabetes, särskilt de med mycket höga hemoglobin A1c -värden, kan också kräva en insulinnivå, eftersom deras kropp är avkänslig för insulinets nivå. Basalt insulin reglerar kroppens blodglukos mellan måltiderna och över natten. Denna basalhastighet för insulinverkan uppnås i allmänhet genom användning av ett mellanverkande insulin (t.ex. NPH) eller en långverkande insulinanalog. Hos typ 1-diabetiker kan det också uppnås genom kontinuerlig infusion av snabbverkande insulin med hjälp av en insulinpump . Ungefär hälften av en persons dagliga insulinbehov administreras som ett basalt insulin, vanligtvis administreras en gång om dagen på natten.
Prandial insulin
När en person äter mat som innehåller kolhydrater och glukos hjälper insulin till att reglera kroppens ämnesomsättning. Prandial insulin, även kallat måltids- eller bolusinsulin, är utformat som en bolusdos insulin före en måltid för att reglera ökningen av blodsockret som uppstår efter en måltid. Dosen av prandial insulin kan vara statisk eller beräknas av patienten med antingen deras nuvarande blodsocker, planerat kolhydratintag eller båda. Denna beräkning kan också utföras av en insulinpump hos patienter som använder en pump. Insulinregimenter som består av doser beräknade på detta sätt betraktas som intensiva insulinregimer . Prandialinsulin ges vanligtvis inte mer än 15–30 minuter före en måltid med hjälp av ett snabbverkande insulin eller ett vanligt insulin. Hos vissa patienter kan ett kombinationsinsulin användas som innehåller både NPH (långtidsverkande) insulin och ett snabbt/regelbundet insulin för att ge både basalt insulin och prandial insulin.
Utmaningar i behandlingen
Det finns flera utmaningar i användningen av insulin som en klinisk behandling för diabetes:
- Administrationssätt.
- Välj rätt dos och tidpunkt. Mängden kolhydrater som en enhet insulin hanterar varierar mycket mellan personer och över dagen men värden mellan 7 och 20 gram per 1 IE är typiska.
- Välj ett lämpligt insulinpreparat (vanligtvis på grund av "hastighet för början och verkningstid").
- Justera dosering och timing för att passa matintag, belopp och typer.
- Justera dosering och timing för att passa träning.
- Justera dosering, typ och tidpunkt för att passa andra förhållanden, till exempel den ökade stressen av sjukdom.
- Variation i absorption i blodomloppet via subkutan leverans
- Dosen är icke-fysiologisk genom att en subkutan bolusdos av insulin enbart administreras istället för att kombinationen av insulin och C-peptid frigörs gradvis och direkt i portvenen .
- Det är helt enkelt ett problem för människor att injicera när de äter kolhydrater eller har en hög blodsockermätning.
- Det är farligt vid misstag (särskilt 'för mycket' insulin).
Typer
Medicinska preparat av insulin är aldrig bara "insulin i vatten". Kliniska insuliner är specialberedda blandningar av insulin plus andra ämnen inklusive konserveringsmedel. Dessa fördröjer absorptionen av insulin, justerar lösningens pH för att minska reaktionerna på injektionsstället och så vidare.
Små variationer av den humana insulinmolekylen kallas insulinanaloger , (tekniskt "insulinreceptorligander ") kallas så eftersom de inte är tekniskt insulin, snarare de är analoger som bibehåller den hormonets glukoshantering funktionalitet. De har absorptions- och aktivitetsegenskaper som för närvarande inte är möjliga med subkutant injicerat insulin. De absorberas antingen snabbt i ett försök att efterlikna verkligt betacellinsulin (som med insulin lispro , insulin aspart och insulin glulisin ), eller absorberas stadigt efter injektion istället för att ha en 'topp' följt av en mer eller mindre snabb minskning av insulin verkan (som med insulin detemir och insulin glargin ), samtidigt som insulins glukossänkande verkan bibehålls i människokroppen. Ett antal metaanalyser , inklusive de som gjordes av Cochrane Collaboration 2005, Tysklands institut för kvalitet och kostnadseffektivitet inom hälso- och sjukvårdssektorn [IQWiG] släpptes 2007, och Canadian Agency for Drugs and Technology in Health (CADTH ) som också släpptes 2007 har inte visat några entydiga fördelar vid klinisk användning av insulinanaloger jämfört med mer konventionella insulintyper.
Att välja insulintyp och dosering/tidpunkt bör göras av en erfaren läkare som arbetar nära personer med diabetes.
De vanliga typerna av insulin är följande.
Snabbt agerande
Inkluderar insulinanalogerna aspart , lispro och glulisin . Dessa börjar fungera inom 5 till 15 minuter och är aktiva i 3 till 4 timmar. De flesta insuliner bildar hexamerer , som fördröjer inträdet i blodet i aktiv form; dessa analoga insuliner har inte bara normal insulinaktivitet. Nyare sorter väntar nu på myndighetsgodkännande i USA som är utformade för att fungera snabbt, men behåller samma genetiska struktur som vanligt humant insulin .
Kortverkande
Inkluderar vanligt insulin , som börjar verka inom 30 minuter och är aktivt cirka 5 till 8 timmar.
Medelverkande
Inkluderar NPH -insulin , som börjar arbeta om 1 till 3 timmar och är aktivt i 16 till 24 timmar.
Långverkande
Inkluderar analogerna glargin U100 och detemir , som alla börjar arbeta inom 1 till 2 timmar och fortsätter att vara aktiva, utan större toppar eller nedgångar, i cirka 24 timmar, även om detta varierar hos många individer.
Ultralångt skådespeleri
Inkluderar analogerna insulin glargin U300 och degludec , som börjar verka inom 30 till 90 minuter och fortsätter att vara aktiva i mer än 24 timmar.
Kombinerade insulinprodukter
Inkluderar en kombination av antingen snabbverkande eller kortverkande insulin med ett längre verkande insulin, vanligtvis ett NPH-insulin . Kombinationsprodukterna börjar arbeta med det kortverkande insulinet (5–15 minuter för snabbverkande och 30 minuter för kortverkande) och förblir aktiva i 16 till 24 timmar. Det finns flera variationer med olika proportioner av de blandade insulinerna (t.ex. Novolog Mix 70/30 innehåller 70% aspartprotamin [liknande NPH] och 30% aspart.)
Administreringssätt
Till skillnad från många läkemedel kan insulin inte tas oralt för närvarande. Liksom nästan alla andra proteiner som introduceras i mag -tarmkanalen reduceras det till fragment (enstaka aminosyrakomponenter), varefter all aktivitet går förlorad. Det har gjorts en del forskning om sätt att skydda insulin från matsmältningskanalen, så att det kan administreras i ett piller. Än så länge är detta helt experimentellt.
Subkutan
Insulin tas vanligen som subkutana injektioner av engångssprutor med nålar , en insulinpump , eller genom upprepad användningsområden insulinpennor med nålar. Personer som vill minska upprepad hudpunktur av insulininjektioner använder ofta en injektionsport i kombination med sprutor.
Användningen av subkutana injektioner av insulin är utformad för att efterlikna den naturliga fysiologiska cykeln för insulinsekretion, samtidigt som man tar hänsyn till de olika egenskaperna hos formuleringarna som används, såsom halveringstid, verkningsstart och verkningstid. Hos många används både en snabb- eller kortverkande insulinprodukt samt en mellan- eller långverkande produkt för att minska mängden injektioner per dag. Hos vissa kan insulininjektioner kombineras med annan injektionsterapi, t.ex. GLP-1-agonister . Rengöring av injektionsstället och injektionsteknik krävs för att säkerställa effektiv insulinbehandling.
Insulinpump
Insulinpumpar är en rimlig lösning för vissa. Fördelar för personen är bättre kontroll över bakgrunden eller basal insulindos, Bolusdoser beräknas bråkdelar av en enhet, och räknare i pump som kan hjälpa till med att bestämma bolus infusions doser. Begränsningarna är kostnad, potential för hypoglykemiska och hyperglykemiska episoder, kateterproblem och inga "slutna kretsar" för att kontrollera insulintillförsel baserat på nuvarande blodsockernivåer.
Insulinpumpar kan vara som "elektriska injektorer" kopplade till en tillfälligt implanterad kateter eller kanyl . Vissa som inte kan uppnå tillräcklig glukoskontroll genom konventionell (eller jet) injektion kan göra det med lämplig pump.
Inbyggda katetrar utgör risken för infektion och sårbildning, och vissa människor kan också utveckla lipodystrofi på grund av infusionsuppsättningarna. Dessa risker kan ofta minimeras genom att infusionsställen hålls rena. Insulinpumpar kräver omsorg och ansträngning för att använda dem på rätt sätt.
Dosering och tidpunkt
Doseringsenheter
En internationell enhet insulin (1 IE) definieras som den "biologiska ekvivalenten" för 34,7 μg rent kristallint insulin.
Den första definitionen av en enhet insulin var den mängd som krävs för att inducera hypoglykemi hos en kanin. Detta fastställdes av James Collip vid University of Toronto 1922. Naturligtvis berodde detta på kaninernas storlek och kost. Insulinenheten fastställdes av insulinkommittén vid University of Toronto. Enheten utvecklades så småningom till den gamla USP insulinenhet, där en enhet (U) insulin sattes lika med den mängd insulin som krävs för att minska koncentrationen av blodglukos i ett fastande kanin till 45 m g / d l (2,5 m mol / L ). När väl den kemiska strukturen och massan av insulin var känd, definierades insulinets enhet av massan av rent kristallint insulin som krävs för att erhålla USP -enheten.
Den måttenhet som används vid insulinbehandling är inte en del av International System of Units (förkortat SI) som är den moderna formen av det metriska systemet . Istället definieras den farmakologiska internationella enheten (IU) av WHO: s expertkommitté för biologisk standardisering .
Potentiella komplikationer
Det centrala problemet för dem som behöver externt insulin är att välja rätt dos insulin och rätt tidpunkt.
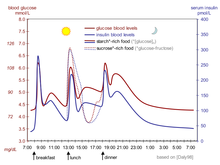
Fysiologisk reglering av blodglukos, liksom hos icke-diabetiker, vore bäst. Ökade blodsockernivåer efter en måltid är en stimulans för snabb frisättning av insulin från bukspottkörteln. Den ökade insulinnivån orsakar glukosabsorption och lagring i celler, reducerar glykogen till glukosomvandling, minskar blodsockernivån och minskar insulinfrisättningen. Resultatet är att blodsockernivån stiger något efter att ha ätit och inom någon timme återgår till den normala fastande nivån. Även den bästa diabetesbehandlingen med syntetiskt humant insulin eller till och med insulinanaloger, dock administrerat, faller långt ifrån normal glukoskontroll hos den som inte är diabetiker.
Det som komplicerar är att maten som äts (se glykemiskt index ) påverkar tarmabsorptionshastigheten. Glukos från vissa livsmedel absorberas mer (eller mindre) snabbt än samma mängd glukos i andra livsmedel. Dessutom orsakar fetter och proteiner förseningar i absorptionen av glukos från kolhydrater som äts samtidigt. Träning minskar också behovet av insulin även när alla andra faktorer förblir desamma, eftersom arbetande muskler har en viss förmåga att ta upp glukos utan hjälp av insulin.
På grund av de komplexa och samverkande faktorerna är det i princip omöjligt att med säkerhet veta hur mycket insulin (och vilken typ) som behövs för att 'täcka' en viss måltid för att uppnå en rimlig blodsockernivå inom en eller två timmar efter att ha ätit . Icke-diabetikeres betaceller hanterar detta rutinmässigt och automatiskt genom kontinuerlig glukosnivåövervakning och insulinfrisättning. Alla sådana beslut av en diabetiker måste baseras på erfarenhet och utbildning (dvs. på ledning av en läkare, PA eller på vissa ställen en specialist diabetiker) och, vidare, specifikt baserat på individens individuella erfarenhet. Men det är inte enkelt och bör aldrig göras med vana eller rutin. Med viss omsorg kan det dock göras ganska bra i klinisk praxis. Till exempel kräver vissa personer med diabetes mer insulin efter att ha druckit skummjölk än de gör efter att ha tagit motsvarande mängd fett, protein, kolhydrater och vätska i någon annan form. Deras särskilda reaktion på skummjölk skiljer sig från andra personer med diabetes, men samma mängd helmjölk kommer sannolikt att orsaka en ännu annorlunda reaktion även hos den personen. Helmjölk innehåller mycket fett medan skummjölk har mycket mindre. Det är en ständig balansgång för alla personer med diabetes, särskilt för dem som tar insulin.
Personer med insulinberoende diabetes kräver vanligtvis en viss basnivå av insulin (basalt insulin), liksom kortverkande insulin för att täcka måltider (bolus, även känd som måltids- eller prandialinsulin ). Att bibehålla basalhastigheten och bolushastigheten är en kontinuerlig balansgång som människor med insulinberoende diabetes måste hantera varje dag. Detta uppnås normalt genom regelbundna blodprov, även om kontinuerlig blodsockertestutrustning (kontinuerliga glukosmonitorer eller CGM) nu blir tillgängliga, vilket kan hjälpa till att förfina denna balansgång när en utbredd användning blir vanlig.
Strategier
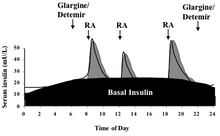
Ett långtidsverkande insulin används för att approximera den basala utsöndringen av insulin från bukspottkörteln, vilket varierar under dagen. NPH/isofan, lente, ultralente, glargine och detemir kan användas för detta ändamål. Fördelen med NPH är dess låga kostnad, det faktum att du kan blanda det med kortverkande former av insulin och därigenom minimera antalet injektioner som måste administreras och att NPH: s aktivitet kommer att nå sin topp 4-6 timmar efter administrering, låta en sovdos balansera tendensen för glukos att stiga med gryningen , tillsammans med en mindre morgondos för att balansera det lägre basala behovet på eftermiddagen och eventuellt en eftermiddagsdos för att täcka kvällsbehovet. En nackdel med NPH vid sänggåendet är att om den inte tas tillräckligt sent (nära midnatt) för att nå sin topp strax före gryningen, kan den orsaka hypoglykemi. En teoretisk fördel med glargin och detemir är att de bara behöver administreras en gång om dagen, även om många i praktiken tycker att ingen av dem varar hela 24 timmar. De kan också administreras när som helst under dagen, förutsatt att de ges vid samma tidpunkt varje dag. En annan fördel med långtidsverkande insuliner är att baskomponenten i en insulinkur (som ger en miniminivå av insulin hela dagen) kan kopplas från prandial- eller boluskomponenten (som ger måltidsskydd via ultrakortverkande insuliner), medan behandlingar som använder NPH och vanligt insulin har nackdelen att varje dosjustering påverkar både basal och prandial täckning. Glargine och detemir är betydligt dyrare än NPH, lente och ultralente, och de kan inte blandas med andra former av insulin.
Ett kortverkande insulin används för att simulera den endogena insulinflödet som produceras i väntan på att äta. Vanligt insulin, lispro, aspart och glulisin kan användas för detta ändamål. Vanligt insulin bör ges med cirka 30 minuters ledtid före måltiden för att vara maximalt effektiv och för att minimera risken för hypoglykemi. Lispro, aspart och glulisin är godkända för dosering med den första biten i måltiden och kan till och med vara effektiva om de ges efter att maten är klar. Det kortverkande insulinet används också för att korrigera hyperglykemi.
Det vanliga schemat för att kontrollera blodsockret för fingerstick och administrera insulin är före alla måltider och ibland även vid sänggåendet. Nyare riktlinjer kräver också en kontroll 2 timmar efter en måltid för att säkerställa att måltiden har täckts effektivt.
Glidande vågar
Först beskrivet 1934, vad läkare vanligtvis kallar glidande insulin (SSI) är endast snabb- eller snabbverkande insulin, givet subkutant, typiskt vid måltider och ibland sänggåendet, men bara när blodsockret är över ett tröskelvärde (t.ex. 10 mmol/L, 180 mg/dL). Inget basalt insulin ges, vilket vanligtvis resulterar i ett förhöjt blodsocker varje morgon, som sedan jagas hela dagen, med cykeln upprepad nästa dag. Den så kallade "glidskalan" -metoden lärs fortfarande allmänt, även om den har kritiserats hårt. Glidande insulin (SSI) är inte ett effektivt sätt att hantera långsiktig diabetes hos personer som bor på vårdhem. Glidande insulin leder till större obehag och ökad omvårdnadstid.
| före frukost | före lunch | före middagen | vid läggdags | |
|---|---|---|---|---|
| NPH -dos | 12 enheter | 6 enheter | ||
| vanlig insulindos om fingersticksglukos är (mg/dl) [mmol/L]: |
||||
| 70–100 [3.9–5.5] | 4 enheter | 4 enheter | ||
| 101–150 [5.6–8.3] | 5 enheter | 5 enheter | ||
| 151–200 [8.4–11.1] | 6 enheter | 6 enheter | ||
| 201–250 [11.2–13.9] | 7 enheter | 7 enheter | ||
| 251–300 [14.0–16.7] | 8 enheter | 1 enhet | 8 enheter | 1 enhet |
| > 300 [> 16,7] | 9 enheter | 2 enheter | 9 enheter | 2 enheter |
Provplan med insulin glargin och insulin lispro:
- Insulin glargin: 20 enheter vid sänggåendet
| om glukos för fingerstick är (mg/dl) [mmol/L]: |
före frukost | före lunch | före middagen | vid läggdags |
|---|---|---|---|---|
| 70–100 [3.9–5.5] | 5 enheter | 5 enheter | 5 enheter | |
| 101–150 [5.6–8.3] | 6 enheter | 6 enheter | 6 enheter | |
| 151–200 [8.4–11.1] | 7 enheter | 7 enheter | 7 enheter | |
| 201–250 [11.2–13.9] | 8 enheter | 8 enheter | 8 enheter | 1 enhet |
| 251–300 [14.0–16.7] | 9 enheter | 9 enheter | 9 enheter | 2 enheter |
| > 300 [> 16,7] | 10 enheter | 10 enheter | 10 enheter | 3 enheter |
Kolhydrater och DAFNE
En mer komplicerad metod som möjliggör större frihet med måltider och mellanmål är " kolhydraträkning ". Detta tillvägagångssätt lärs ut till personer som är diabetiker i Storbritannien och på andra ställen som "Dosjustering för normal kost" eller DAFNE .
I Europa kan personer som inte känner till DAFNE -regimen gå en utbildningskurs där den grundläggande riktlinjen för insulindos är "för varje 10 g kolhydrater du äter, ta 1 enhet insulin". DAFNE -kurser täcker också ämnen som naturligt fungerar tillsammans med denna regim, såsom blodsockermätning, träning och kolhydratuppskattning för att hjälpa personen att utarbeta sina personliga kontrollkrav.
Människor kan också använda sin totala dagliga dos (TDD) insulin för att uppskatta hur många gram kolhydrater som "täcks" av 1 enhet insulin, och med hjälp av detta resultat uppskatta hur många enheter insulin som ska administreras beroende på kolhydratinnehållet av deras måltid. Till exempel, om personen bestämmer att 1 enhet insulin kommer att täcka 15 gram kolhydrater, måste de administrera 5 enheter insulin innan de äter en måltid som innehåller 75 gram kolhydrater.
Vissa alternativa metoder tar också hänsyn till proteinhalten i måltiden (eftersom överskott av kostprotein kan omvandlas till glukos via glukoneogenes ).
Med DAFNE innebär de flesta doser en rättvis gissning, särskilt med icke-märkta livsmedel, och fungerar bara ganska konsekvent från en dos till nästa om personen är medveten om sin kropps krav. Till exempel finner en person att de kan ta 1 enhet insulin till 10 g kolhydrater på morgonen och kvällen, men upptäcker att deras kropp kräver mer insulin för en måltid mitt på dagen så att de måste justera till 1 enhet per 8,5 g kolhydrater.
Andra mindre uppenbara faktorer som påverkar kroppens användning av insulin måste också beaktas. Till exempel kan vissa människor upptäcka att deras kroppar bearbetar insulin bättre under varma dagar så kräver mindre insulin. Med detta måste personen återigen anpassa sin dos efter bästa förståelse från sina tidigare erfarenheter.
DAFNE -regimen kräver att personen lär sig om sin kropps behov genom erfarenhet, vilket tar tid och tålamod, men det kan sedan bli effektivt.
Closed-loop prediktiv modellering
Personer med fluktuerande insulinbehov kan dra nytta av en metod för förutsebar modellering med sluten slinga . Som en förlängning på "kolhydraträkning" justeras kontinuerligt de fyra dagliga insulindoseringarna som behövs för att uppnå målblodsockernivåerna för den "normala" dagliga kolhydratförbrukningen och mängden fysisk aktivitet baserat på den slutna prediktiva modelleringsmetoden. avläsningarna före blodsockernivån och före natten. Varje ny blodsockermätning ger feedback för att finjustera och spåra kroppens insulinbehov. Inom denna strategi är de viktigaste specifika faktorerna, som måste bestämmas experimentellt, blodsockerkorrigeringsfaktorn och kolhydratkvoten. Blodsockerkorrigeringsfaktorn anger både "proportionell förstärkning" och "integral förstärkning" -faktorer för de fyra återkopplingsslingorna . Om det tas för lågt, korrigeras inte avvikelser från målblodsockernivån för effektivt, om det tas för högt blir blodsockervärden instabil. Eftersom kolhydratförhållandet i detta tillvägagångssätt endast används för att redogöra för icke-standardiserade kolhydratintag, är det vanligtvis inte nödvändigt att arbeta med måltidsspecifika förhållanden.
Korrekt modellering av mängden insulin som återstår för att verka i personens kropp är väsentlig i denna strategi, till exempel för att säkerställa att eventuell justering av mängden basalinsulin beaktas vid beräkning av de bolusmängder som behövs för måltiderna. På grund av behovet av att redogöra för varje insulins aktivitetsprofil, analysera tidigare blodsockertrender och ta hänsyn till icke-standardiserade kolhydratintag och träningsnivåer, kräver denna strategi en dedikerad smarttelefonapplikation för att hantera alla beräkningar och returnera meningsfulla doseringsrekommendationer och förväntade blodsockernivåer.
Dosberäkning
Insulindosering ges av formeln
baserat på personens blodglukos- och kolhydratintag och dessa konstanter:
- TR = målhastighet
- CF = korrigerande faktor
- KF = kolhydratfaktor
Blodsocker och målhastighet uttrycks i mg/dL eller mmol/L. Konstanter bör bestämmas av en läkare eller klinisk farmaceut.
Missbruk
Missbruk av exogent insulin medför en medföljande risk för hypoglykemisk koma och död när mängden som används överstiger den som krävs för att hantera förtärda kolhydrater. Akuta risker inkluderar hjärnskador , förlamning och död . Symtomen kan vara yrsel, svaghet, darrningar, hjärtklappning , anfall, förvirring, huvudvärk, dåsighet, koma, diafores och illamående . Alla personer som lider av överdoser bör remitteras för medicinsk bedömning och behandling, som kan pågå i timmar eller dagar.
Data från US National Poison Data System (2013) indikerar att 89,3% av insulinfallen som rapporteras till giftcentraler är oavsiktliga till följd av terapeutiska fel. Ytterligare 10% av fallen är avsiktliga och kan återspegla självmordsförsök, övergrepp, brottsligt uppsåt, sekundär vinst eller andra okända skäl. Hypoglykemi som har inducerats av exogent insulin kan detekteras kemiskt genom att undersöka förhållandet mellan insulin och C-peptid i perifer cirkulation. Det har föreslagits att denna typ av tillvägagångssätt skulle kunna användas för att upptäcka exogent insulinmissbruk av idrottare.
Möjligheten att använda insulin i ett försök att förbättra idrottsprestationerna föreslogs redan vid vinter -OS 1998 i Nagano, Japan , vilket rapporterades av Peter Sönksen i juli 2001 av Journal of Endocrinology . Frågan om idrottare som inte är diabetiker lagligt kunde använda insulin togs upp av en rysk läkare. Huruvida insulin faktiskt skulle förbättra idrottsprestanda är oklart, men oro för dess användning fick Internationella olympiska kommittén att förbjuda användning av hormonet för icke-diabetiker i 1998.
Boken Game of Shadows (2001), av reportrarna Mark Fainaru-Wada och Lance Williams, inkluderade påståenden om att basebollspelaren Barry Bonds använde insulin (liksom andra droger) i den uppenbara tron att det skulle öka effektiviteten av det tillväxthormon han påstods ha tagit. Obligationer vittnade så småningom inför en federal jury som en del av en regeringsutredning av BALCO .
Kroppsbyggare påstås att de använder exogent insulin och andra läkemedel i tron att de kommer att öka muskelmassan. Kroppsbyggare har beskrivits som att injicera upp till 10 IE vanligt syntetiskt insulin innan de äter söta måltider. En rapport från 2008 föreslog att insulin ibland används i kombination med anabola steroider och tillväxthormon (GH) och att "Idrottare utsätter sig för potentiell skada genom att själv administrera stora doser GH, IGF -I och insulin". Insulinmissbruk har nämnts som en möjlig faktor vid dödsfallet av kroppsbyggare Ghent Wakefield och Rich Piana .
Insulin, humant tillväxthormon (HGH) och insulinliknande tillväxtfaktor 1 (IGF-1) administreras själv av dem som vill öka muskelmassan utöver omfattningen som erbjuds av anabola steroider ensam. Deras motivering är att eftersom insulin och HGH verkar synergistiskt för att främja tillväxt, och eftersom IGF-1 är en primär medlare för muskuloskeletal tillväxt, bör "staplingen" av insulin, HGH och IGF-1 erbjuda en synergistisk tillväxteffekt på skelettmuskeln. Denna teori har under de senaste åren stöttats av kroppsbyggare på högsta nivå, vars tävlingsvikt överstiger 23 kg muskler, större än konkurrenterna tidigare och med ännu lägre kroppsfett.
Detektion i biologiska vätskor
Insulin mäts ofta i serum, plasma eller blod för att övervaka behandlingen hos personer som är diabetiker, bekräfta en förgiftningsdiagnos hos sjukhuspersoner eller hjälpa till med en medicinsk legal undersökning av misstänkt död. Tolkningen av de resulterande insulinkoncentrationerna är komplex, med tanke på de många olika insulintyperna, olika administreringssätt, förekomsten av anti-insulinantikroppar hos insulinberoende diabetiker och läkemedlets ex vivo- instabilitet. Andra potentiella förvirrande faktorer inkluderar den omfattande korsreaktiviteten hos kommersiella insulinimmunanalyser för de biosyntetiska insulinanalogerna, användningen av högdos intravenöst insulin som ett motgift mot överdosering av antihypertensiva läkemedel och omdistribution av insulin inom kroppen. Användningen av en kromatografisk teknik för insulinanalys kan under vissa omständigheter vara att föredra framför immunanalys, för att undvika frågan om korsreaktivitet som påverkar det kvantitativa resultatet och även för att identifiera den specifika insulintypen i provet.
Kombination med andra diabetesläkemedel
En kombinationsterapi av insulin och andra antidiabetika verkar vara mest fördelaktig för personer som är diabetiker, som fortfarande har kvar insulinsekretionsförmåga. En kombination av insulinterapi och sulfonylurea är mer effektivt än insulin enbart vid behandling av personer med typ 2 -diabetes efter sekundärt misslyckande med orala läkemedel, vilket leder till bättre glukosprofiler och/eller minskat insulinbehov.
Historia
Detta är en kronologi över viktiga milstolpar i historien om medicinsk användning av insulin. För mer information om upptäckten, extraktionen, rening, klinisk användning och syntes av insulin, se Insulin
- 1921 Forskning om bukspottkörtelns roll i näringsassimileringen
- 1922 Frederick Banting , Charles Best och James Collip använder extrakt av bovint insulin hos människor på Connaught Laboratories i Toronto, Kanada.
- 1922 Leonard Thompson blir den första människan som behandlas med insulin.
- 1922 James D. Havens , son till den tidigare kongressledamoten James S. Havens , blir den första amerikanen som behandlas med insulin.
- 1922 Elizabeth Hughes Gossett , dotter till USA: s utrikesminister, blir den första amerikanen som (officiellt) behandlas i Toronto.
- 1923 Eli Lilly producerar kommersiella mängder av mycket renare bovint insulin än Banting et al. hade använt
- 1923 Farbwerke Hoechst , en av föregångarna till dagens Sanofi Aventis , producerar kommersiella mängder bovint insulin i Tyskland
- 1923 grundar Hans Christian Hagedorn Nordisk Insulinlaboratorium i Danmark - föregångaren till dagens Novo Nordisk
- 1923 Constance Collier återvänder till hälsan efter att ha behandlats framgångsrikt med insulin i Strasbourg
- 1926 får Nordisk ett danskt charter för att producera insulin som ideellt
- 1936 kanadensarna David M. Scott och Albert M. Fisher formulerar en zinkinsulinblandning på Connaught Laboratories i Toronto och licensierar den till Novo
- 1936 Hagedorn upptäcker att tillsats av protamin till insulin förlänger insulinets verkningstid
- 1946 Nordisk formulerar Isophane porcine insulin aka Neutral Protamine Hagedorn eller NPH insulin
- 1946 Nordisk kristalliserar en blandning av protamin och insulin
- 1950 Nordisk marknadsför NPH -insulin
- 1953 Novo formulerar Lente -svin- och nötkreaturinsuliner genom att tillsätta zink för längre insulin
- 1955 Frederick Sanger bestämmer insulinets aminosyrasekvens
- 1965 Syntetiserad genom total syntes av Wang Yinglai , Chen-Lu Tsou , et al.
- 1969 Dorothy Crowfoot Hodgkin löser kristallstrukturen för insulin genom röntgenkristallografi
- 1973 Renat monokomponent (MC) insulin införs
- 1973 USA "officiellt" standardiserat insulin som såldes för mänskligt bruk i USA till U-100 (100 enheter per milliliter). Innan dess såldes insulin i olika styrkor, inklusive U-80 (80 enheter per milliliter) och U-40-formuleringar (40 enheter per milliliter), så ansträngningen att "standardisera" styrkan syftade till att minska doseringsfel och underlätta läkare 'jobb med att förskriva insulin för människor. Andra länder följde också efter.
- 1978 Genentech producerar biosyntetiskt humant insulin i Escherichia coli -bakterier med rekombinant DNA -teknik, licenser till Eli Lilly
- 1981 Novo Nordisk omvandlar kemiskt och enzymatiskt svin till humant insulin
- 1982 Genentech syntetiskt humant insulin (ovan) godkänt
- 1983 Eli Lilly and Company producerar biosyntetiskt humant insulin med rekombinant DNA -teknik, Humulin
- 1985 Axel Ullrich sekvenserar en human cellmembran insulinreceptor.
- 1988 Novo Nordisk producerar rekombinant biosyntetiskt humant insulin
- 1996 Lilly Humalog "lispro" insulinanalog godkänd.
- 2000 Sanofi Aventis Lantus insulin "glargine" analog godkänd för klinisk användning i USA och Europa.
- 2004 Sanofi Aventis Apidra insulin "glulisin" insulinanalog godkänt för klinisk användning i USA.
- 2006 Novo Nordisk Levemir "detemir" insulinanalog godkänd för klinisk användning i USA.
Ekonomi
I USA har enhetspriset på insulin ökat stadigt från 1991 till 2019. Det steg trefaldigt från 2002 till 2013. Kostnaderna kan bli så höga som 900 dollar per månad. Oron väcktes 2016 för läkemedelsföretag som samarbetade för att höja priserna. I januari 2019 skickade lagstiftare från USA: s representanthus brev till insulintillverkarna Eli Lilly och Co. , Sanofi och Novo Nordisk och bad om förklaringar till deras snabbt stigande insulinpriser. Den årliga kostnaden för insulin för personer med typ 1 -diabetes i USA fördubblades nästan från 2 900 dollar till 5 700 dollar under perioden 2012 till 2016.
Människor i USA betalar två till sex gånger mer än resten av världen, inklusive Kanada, för receptbelagda läkemedel enligt International Federation of Health Plans. Kanada, liksom många andra industriländer, har priskontroller av läkemedelskostnaderna.
Forskning
Inandning
År 2006 godkände US Food and Drug Administration användningen av Exubera , det första inhalerbara insulinet. Det togs bort från marknaden av tillverkaren från och med tredje kvartalet 2007, på grund av bristande acceptans.
Inhalerat insulin påstods ha samma effekt som injicerat insulin, både när det gäller att kontrollera glukosnivåer och blodhalveringstid. För närvarande är inhalerat insulin kortverkande och intas vanligtvis före måltider; en injektion av långtidsverkande insulin på natten krävs ofta fortfarande. När människor bytte från injicerat till inhalerat insulin sågs ingen signifikant skillnad i Hb A1c -nivåer under tre månader. Noggrann dosering var ett särskilt problem, även om människor inte visade någon signifikant viktökning eller nedsatt lungfunktion under försökets längd, jämfört med baslinjen.
Efter den kommersiella lanseringen 2005 i Storbritannien rekommenderades den inte (i juli 2006) av National Institute for Health and Clinical Excellence för rutinmässig användning, utom i fall där det finns "bevisad injektionsfobi diagnostiserad av en psykiater eller psykolog" .
I januari 2008 meddelade också världens största insulintillverkare, Novo Nordisk , att företaget avbryter all vidareutveckling av företagets egen version av inhalerbart insulin, kallat AERx iDMS inhalationsinsulinsystem. På samma sätt avslutade Eli Lilly och Company sina ansträngningar för att utveckla sitt inhalationsluftinsulin i mars 2008. MannKind Corp. (majoritetsägare, Alfred E. Mann ) är dock optimistisk med tanke på konceptet.
Transdermal
Det finns flera metoder för transdermal tillförsel av insulin. Pulserande insulin använder mikrostrålar för att pulsera insulin till personen, vilket efterliknar de fysiologiska utsöndringarna av insulin från bukspottkörteln. Jetinjektion hade olika insulintillförselstoppar och varaktigheter jämfört med nålinjektion. Vissa diabetiker kan föredra jetinjektorer framför injektion.
Både elektricitet med jontofores och ultraljud har visat sig göra huden tillfälligt porös. Insulinadministrationsaspekten förblir experimentell, men blodglukosprovningsaspekten för "handledsapparater" är kommersiellt tillgänglig.
Forskare har tagit fram en klockliknande enhet som testar blodsockernivåer genom huden och administrerar korrigerande doser av insulin genom porer i huden. En liknande enhet, men som förlitar sig på hudgenomträngande "mikronålar", var i djurförsöksstadiet 2015.
Intranasalt
Intranasalt insulin undersöks. En randomiserad kontrollerad studie som avgör om intranasalt insulin kan fördröja eller förhindra uppkomsten av typ 1-diabetes hos riskfyllda barn och unga vuxna förväntas ge resultat 2016.
Via mun
Den grundläggande överklagan för hypoglykemiska medel via munnen är att de flesta människor föredrar ett piller eller en oral vätska framför en injektion. Insulin är dock ett peptidhormon , som smälts i magen och tarmen och för att vara effektivt för att kontrollera blodsockret, kan det inte tas oralt i sin nuvarande form.
Den potentiella marknaden för en oral form av insulin antas vara enorm, så många laboratorier har försökt att utforma sätt att flytta tillräckligt med intakt insulin från tarmen till portalvenen för att ha en mätbar effekt på blodsockret.
Ett antal derivatiserings- och formuleringsstrategier pågår för närvarande för att försöka utveckla ett oralt tillgängligt insulin. Många av dessa tillvägagångssätt använder nanopartikelleveranssystem och flera testas i kliniska prövningar .
Bukspottkörteltransplantation
En annan förbättring skulle vara en transplantation av bukspottkörteln eller betacellen för att undvika periodisk insulinadministrering. Detta skulle resultera i en självreglerande insulinkälla. Transplantation av en hel bukspottkörtel (som ett enskilt organ ) är svårt och relativt ovanligt. Det är ofta utförs i samband med lever- eller njurtransplantat, även om det kan ske av sig själv. Det är också möjligt att transplantera endast betacellerna i bukspottkörteln. Ö -transplantationer hade dock varit mycket experimentella i många år, men vissa forskare i Alberta, Kanada , har utvecklat tekniker med hög initial framgång (cirka 90% i en grupp). Nästan hälften av dem som fick en holme-celltransplantation var insulinfria ett år efter operationen; i slutet av det andra året sjunker den siffran till ungefär en av sju. Forskare vid University of Illinois i Chicago (UIC) har emellertid något modifierat Edmonton-protokollförfarandet för holme celltransplantation och uppnått insulinoberoende hos diabetiker, med färre men bättre fungerande pankreas ö-celler. Långsiktiga studier behövs för att validera om det förbättrar insulinoberoendehastigheten.
Betacellstransplantation kan bli praktisk inom en snar framtid. Dessutom har vissa forskare undersökt möjligheten att transplantera genetiskt manipulerade icke-betaceller för att utsöndra insulin. Kliniskt testbara resultat är långt ifrån realiserade vid denna tidpunkt. Flera andra icke-transplanterade metoder för automatisk insulinleverans utvecklas i forskningslaboratorier, men ingen är nära kliniskt godkännande.
Referenser
externa länkar
- "Insulin" . Läkemedelsinformationsportal . US National Library of Medicine.
- "Insulin regelbundet" . Läkemedelsinformationsportal . US National Library of Medicine.
- "Insulin [injektion], tvåfasigt" . Läkemedelsinformationsportal . US National Library of Medicine.


