Glukoneogenes - Gluconeogenesis
Glukoneogenes ( GNG ) är en metabolisk väg som resulterar i bildning av glukos från vissa kolhydrater utan kolhydrater . Det är en allestädes närvarande process som finns i växter, djur, svampar, bakterier och andra mikroorganismer. I vertebrater, förekommer glukoneogenes huvudsakligen i levern och, i mindre utsträckning, i cortex av njurarna . Det är en av två primära mekanismer - den andra är nedbrytning av glykogen ( glykogenolys ) - som används av människor och många andra djur för att bibehålla blodsockernivåer , undvika låga nivåer ( hypoglykemi ). Hos idisslare , eftersom kostkolhydrater tenderar att metaboliseras av våmorganismer , sker glukoneogenes oavsett fasta, lågkolhydratkost, träning etc. I många andra djur sker processen under fasta , svält , lågkolhydratkost eller intensiv träning .
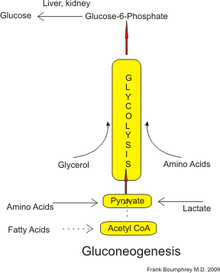
Hos människor kan substrat för glukoneogenes komma från alla icke-kolhydratkällor som kan omvandlas till pyruvat eller mellanprodukter av glykolys (se figur). För nedbrytning av proteiner inkluderar dessa substrat glukogena aminosyror (även om de inte är ketogena aminosyror ); från nedbrytning av lipider (såsom triglycerider ) inkluderar de glycerol , udda-kedjiga fettsyror (även om de inte är jämnkedjiga fettsyror, se nedan); och från andra delar av metabolism inkluderar de laktat från Cori -cykeln . Under förhållanden med långvarig fasta kan aceton som härrör från ketonkroppar också fungera som ett substrat, vilket ger en väg från fettsyror till glukos. Även om de flesta glukoneogenes sker i levern, ökar det relativa bidraget av glukoneogenes från njuren vid diabetes och långvarig fasta.
Glukoneogenesvägen är mycket endergonisk tills den kopplas till hydrolysen av ATP eller GTP , vilket effektivt gör processen exergonisk . Till exempel kräver vägen som leder från pyruvat till glukos-6-fosfat 4 molekyler ATP och 2 molekyler GTP för att gå spontant. Dessa ATP tillförs från fettsyrakatabolism via beta -oxidation .
Prekursorer

- Glukogena aminosyror har denna förmåga
- Ketogena aminosyror gör det inte. Dessa produkter kan fortfarande användas för ketogenes eller lipidsyntes .
- Vissa aminosyror kataboliseras till både glukogena och ketogena produkter.
Hos människor är de främsta glukoneogena prekursorerna laktat , glycerol (som är en del av triglyceridmolekylen ), alanin och glutamin . Sammantaget står de för över 90% av den totala glukoneogenesen. Andra glukogena aminosyror och alla mellanprodukter av citronsyracykeln (genom omvandling till oxaloacetat ) kan också fungera som substrat för glukoneogenes. Generellt leder inte människors konsumtion av glukoneogena substrat i livsmedel till ökad glukoneogenes.
Hos idisslare är propionat det huvudsakliga glukoneogena substratet. I nonruminants, inklusive människor, uppstår propionat från p-oxidationen av udda och grenade fettsyror är ett (relativt mindre) substrat för glukoneogenes.
Laktat transporteras tillbaka till levern där det omvandlas till pyruvat genom Cori -cykeln med hjälp av enzymet laktat dehydrogenas . Pyruvat, det första avsedda substratet för den glukoneogena vägen, kan sedan användas för att generera glukos. Transaminering eller deaminering av aminosyror underlättar inträde av deras kolskelett i cykeln direkt (som pyruvat eller oxaloacetat), eller indirekt via citronsyracykeln. Bidraget från Cori -cykellaktat till den totala glukosproduktionen ökar med fastans varaktighet. Specifikt, efter 12, 20 och 40 timmars fasta av mänskliga frivilliga, var bidraget från Cori -cykellaktat till glukoneogenes 41%, 71%respektive 92%.
Huruvida fettsyror med jämn kedja kan omvandlas till glukos hos djur har varit en långvarig fråga inom biokemi. Udda-kedjiga fettsyror kan oxideras för att ge acetyl-CoA och propionyl-CoA , det senare fungerar som en föregångare till succinyl-CoA , som kan omvandlas till pyruvat och gå in i glukoneogenes. Däremot oxideras jämkedjiga fettsyror för att ge endast acetyl-CoA, vars inträde i glukoneogenes kräver närvaro av en glyoxylatcykel (även känd som glyoxylatshunt) för att producera fyrkolsdikarboxylsyra-prekursorer. Glyoxylatshunten består av två enzymer, malatsyntas och isocitratlyas, och finns i svampar, växter och bakterier. Trots vissa rapporter om glyoxylatshunt enzymatiska aktiviteter som detekterats i djurvävnader har gener som kodar för båda enzymatiska funktionerna endast hittats i nematoder , där de existerar som ett enda bi-funktionellt enzym. Gener som kodar för malatsyntas enbart (men inte isocitratlyas) har identifierats hos andra djur inklusive leddjur , pikdjur och till och med vissa ryggradsdjur . Däggdjur som befinner sig inneha malatsyntasgenen inkluderar monotremes ( näbbdjur ) och pungdjur ( opossum ), men inte placentaldäggdjur .
Förekomsten av glyoxylatcykeln hos människor har inte fastställts, och det är allmänt menat att fettsyror inte direkt kan omvandlas till glukos hos människor. Kol-14 har visat sig hamna i glukos när det levereras i fettsyror, men detta kan förväntas från införlivandet av märkta atomer som härrör från acetyl-CoA i mellanprodukter av citronsyracykel som är utbytbara med de som härrör från andra fysiologiska källor såsom glukogena aminosyror. I avsaknad av andra glukogena källor kan 2- kolacetyl-CoA som härrör från oxidationen av fettsyror inte producera ett nettoutbyte av glukos via citronsyracykeln , eftersom motsvarande två kolatomer frigörs som koldioxid under cykeln. Under ketos ger dock acetyl-CoA från fettsyror ketonkroppar , inklusive aceton , och upp till ~ 60% aceton kan oxideras i levern till pyruvatprekursorerna acetol och metylglyoxal . Således kan ketonkroppar härledda från fettsyror stå för upp till 11% av glukoneogenesen under svält. Katabolism av fettsyror producerar också energi i form av ATP som är nödvändig för glukoneogenesvägen.
Plats
Hos däggdjur har glukoneogenes antagits vara begränsad till levern, njuren, tarmen och musklerna, men nyligen bevisade tyder på att glukoneogenes förekommer i astrocyter i hjärnan. Dessa organ använder något olika glukoneogena prekursorer. Levern använder företrädesvis laktat, glycerol och glukogena aminosyror (särskilt alanin ) medan njuren företrädesvis använder laktat, glutamin och glycerol. Laktat från Cori -cykeln är kvantitativt den största källan till substrat för glukoneogenes, särskilt för njuren. Levern använder både glykogenolys och glukoneogenes för att producera glukos, medan njuren endast använder glukoneogenes. Efter en måltid skiftar levern till glykogensyntes , medan njuren ökar glukoneogenesen. Tarmarna använder mest glutamin och glycerol.
Propionat är det huvudsakliga substratet för glukoneogenes i idisslare, och levern för idisslare kan använda ökad användning av glukoneogena aminosyror (t.ex. alanin) när glukosbehovet ökar. Levercellernas förmåga att använda laktat för glukoneogenes minskar från förhandsstadiet till idisslare hos kalvar och lamm. I fårnjursvävnad har mycket höga glukoneogeneshastigheter från propionat observerats.
I alla arter är bildandet av oxaloacetat från pyruvat- och TCA-cykelmellanprodukter begränsat till mitokondrion, och enzymerna som omvandlar fosfoenolpyruvinsyra (PEP) till glukos-6-fosfat finns i cytosolen. Platsen för enzymet som länkar dessa två delar av glukoneogenesen genom att omvandla oxaloacetat till PEP - PEP -karboxykinas (PEPCK) - är varierande efter art: det kan hittas helt inom mitokondrierna , helt inom cytosolen eller dispergeras jämnt mellan de två, som det är hos människor. Transport av PEP över mitokondriemembranet åstadkommes med dedikerade transportproteiner; dock finns inga sådana proteiner för oxaloacetat . Därför måste oxaloacetat hos arter som saknar intra-mitokondriellt PEPCK omvandlas till malat eller aspartat , exporteras från mitokondrionen och omvandlas tillbaka till oxaloacetat för att glukoneogenes ska kunna fortsätta.
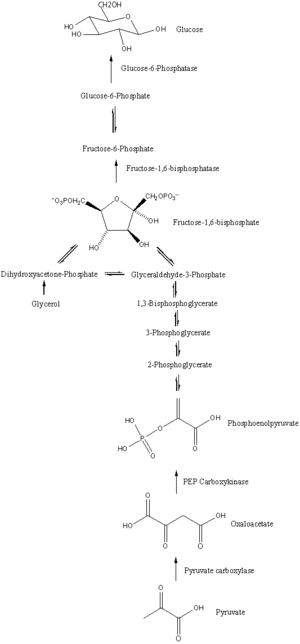
Väg
Glukoneogenes är en väg som består av en serie av elva enzymkatalyserade reaktioner. Vägen kommer att börja antingen i levern eller njuren, i mitokondrier eller cytoplasma hos dessa celler, detta är beroende av substratet som används. Många av reaktionerna är motsatsen till stegen som finns i glykolys .
- Glukoneogenes börjar i mitokondrier med bildandet av oxaloacetat genom karboxylering av pyruvat. Denna reaktion kräver också en molekyl ATP och katalyseras av pyruvatkarboxylas . Detta enzym stimuleras av höga nivåer av acetyl-CoA (produceras i β-oxidation i levern) och hämmas av höga nivåer av ADP och glukos.
- Oxaloacetat reduceras till malat med NADH , ett steg som krävs för att transportera det ur mitokondrier.
- Malat oxideras till oxaloacetat med NAD + i cytosolen, där de återstående stegen av glukoneogenes äger rum.
- Oxaloacetat dekarboxyleras och fosforyleras sedan för att bilda fosfoenolpyruvat med användning av enzymet PEPCK . En molekyl av GTP hydrolyseras till BNP under denna reaktion.
- De nästa stegen i reaktionen är desamma som omvänd glykolys . Emellertid, fruktos-1,6-bisfosfatas omvända fruktos 1,6-bisfosfat till fruktos 6-fosfat , med användning av en vattenmolekyl och frigöra en fosfat (i glykolysen, fosfofruktokinas 1 konverterar F6P och ATP till F1,6BP och ADP ). Detta är också det hastighetsbegränsande steget för glukoneogenes.
- Glukos-6-fosfat bildas av fruktos-6-fosfat av fosfoglukoisomeras (baksidan av steg 2 i glykolys). Glukos-6-fosfat kan användas i andra metaboliska vägar eller defosforyleras till fritt glukos. Medan fri glukos lätt kan diffundera in och ut ur cellen, låses den fosforylerade formen (glukos-6-fosfat) i cellen, en mekanism genom vilken intracellulära glukosnivåer styrs av celler.
- Den slutliga glukoneogenesen, bildandet av glukos, sker i lumen i det endoplasmatiska retikulumet , där glukos-6-fosfat hydrolyseras av glukos-6-fosfatas för att producera glukos och frigöra ett oorganiskt fosfat. Precis som två steg tidigare är detta steg inte en enkel reversering av glykolys, där hexokinas katalyserar omvandlingen av glukos och ATP till G6P och ADP. Glukos transporteras in i cytoplasman av glukostransportörer som finns i det endoplasmatiska retikulets membran.
| Metabolism av vanliga monosackarider , inklusive glykolys , glukoneogenes, glykogenes och glykogenolys |
|---|
Förordning
Medan de flesta stegen i glukoneogenesen är det motsatta av de som finns i glykolys , ersätts tre reglerade och starkt endergoniska reaktioner med mer kinetiskt gynnsamma reaktioner. Hexokinas / glukokinas , fosfofruktokinas och pyruvatkinas- enzymer för glykolys ersätts med glukos-6-fosfatas , fruktos-1,6-bisfosfatas och PEP-karboxykinas / pyruvatkarboxylas. Dessa enzymer regleras vanligtvis av liknande molekyler, men med motsatta resultat. Till exempel aktiverar acetyl CoA och citrat glukoneogenesenzymer (pyruvatkarboxylas respektive fruktos-1,6-bisfosfatas), samtidigt som det hämmar det glykolytiska enzymet pyruvatkinas . Detta system för ömsesidig kontroll tillåter glykolys och glukoneogenes att hämma varandra och förhindrar en meningslös cykel av syntetisering av glukos för att bara bryta ner den. Pyruvatkinas kan också kringgås med 86 vägar som inte är relaterade till glukoneogenes, i syfte att bilda pyruvat och därefter laktat; några av dessa vägar använder kolatomer som härrör från glukos.
Majoriteten av de enzymer som är ansvariga för glukoneogenes finns i cytosolen ; undantagen är mitokondriell pyruvat -karboxylas och, hos djur, fosfoenolpyruvat -karboxykinas . Det senare existerar som ett isozym som finns i både mitokondrionen och cytosolen . Glukoneogeneshastigheten styrs slutligen av verkan av ett nyckelenzym, fruktos-1,6-bisfosfatas , som också regleras genom signaltransduktion av cAMP och dess fosforylering.
Global kontroll av glukoneogenes förmedlas av glukagon ( frigörs när blodsockret är lågt ); det utlöser fosforylering av enzymer och regulatoriska proteiner med proteinkinas A (ett cykliskt AMP -reglerat kinas) vilket resulterar i hämning av glykolys och stimulering av glukoneogenes. Insulin motverkar glukagon genom att hämma glukoneogenes. Typ 2 -diabetes präglas av överskott av glukagon och insulinresistens från kroppen. Insulin kan inte längre hämma genuttrycket av enzymer som PEPCK vilket leder till ökade nivåer av hyperglykemi i kroppen. Det antidiabetiska läkemedlet metformin minskar blodglukos främst genom hämning av glukoneogenes, vilket övervinner insulinets misslyckande att hämma glukoneogenes på grund av insulinresistens.
Studier har visat att frånvaron av hepatisk glukosproduktion inte har någon större effekt på kontrollen av fastande plasmaglukoskoncentration. Kompenserande induktion av glukoneogenes sker i njurarna och tarmen, driven av glukagon , glukokortikoider och acidos.
Insulinresistens
I levern främjar FOX -proteinet FOXO6 normalt glukoneogenes i fastande tillstånd, men insulin blockerar FOXO6 vid matning. I ett tillstånd av insulinresistens misslyckas insulin med att blockera FOXO6 vilket resulterar i fortsatt glukoneogenes även vid matning, vilket resulterar i högt blodsocker ( hyperglykemi ).
Insulinresistens är en vanlig egenskap hos metaboliskt syndrom och typ 2 -diabetes . Av denna anledning är glukoneogenes ett mål för terapi för typ 2 -diabetes, såsom det antidiabetiska läkemedlet metformin , som hämmar glukoneogen glukosbildning och stimulerar glukosupptag genom celler.