Henoch – Schönlein purpura - Henoch–Schönlein purpura
| Henoch-Schönlein purpura | |
|---|---|
| Andra namn | IgA -vaskulit, anafylaktoid purpura, purpura rheumatica, Schönlein – Henoch purpura |
 | |
| Typisk purpura på underben och rumpa | |
| Uttal | |
| Specialitet | Reumatologi , immunologi |
Henoch – Schönlein purpura ( HSP ), även känd som IgA -vaskulit , är en sjukdom i hud , slemhinnor och ibland andra organ som oftast drabbar barn . I huden orsakar sjukdomen påtaglig purpura (små, upphöjda blödningsområden under huden), ofta med ledvärk och buksmärta . Med njurinvolvering kan det finnas en förlust av små mängder blod och protein i urinen ( hematuri och proteinuri ), men detta går vanligtvis obemärkt förbi; i en liten andel av fallen fortsätter njurengagemanget till kronisk njursjukdom . HSP föregås ofta av en infektion , såsom en halsinfektion .
HSP är en systemisk vaskulit ( inflammation i blodkärl ) och kännetecknas av avsättning av immunkomplex som innehåller antikroppen immunglobulin A (IgA); den exakta orsaken till detta fenomen är okänd. Hos barn försvinner det vanligtvis inom flera veckor och kräver ingen behandling förutom symptomkontroll, men kan återkomma i en tredjedel av fallen och orsaka irreversibel njurskada i ungefär ett av hundra fall. Hos vuxna är prognosen annorlunda än hos barn. Den genomsnittliga varaktigheten av kutana lesioner är 27,9 månader. För många tenderar det att återfalla-överlåta över en längre tid, snarare än självbegränsande och det tenderar att finnas fler komplikationer.
tecken och symtom

Purpura , artrit och buksmärtor är kända som den "klassiska triaden" av Henoch – Schönlein purpura. Purpura förekommer i alla fall, ledvärk och artrit hos 80%och buksmärtor hos 62%. Vissa inkluderar gastrointestinal blödning som ett fjärde kriterium; detta inträffar i 33% av fallen, ibland, men inte nödvändigtvis alltid, på grund av intussusception . Purpura visas vanligtvis på benen och skinkorna, men kan också ses på armar, ansikte och bål. Buksmärtorna är kolikartade och kan åtföljas av illamående, kräkningar, förstoppning eller diarré. Det kan finnas blod eller slem i avföringen. De involverade lederna tenderar att vara anklar , knän och armbågar , men artrit i händer och fötter är möjligt; artrit är icke -erosivt och orsakar därför ingen permanent deformitet. Fyrtio procent har bevis på njurinblandning , främst i form av hematuri (blod i urinen), men bara en fjärdedel kommer att ha detta i tillräckliga mängder för att märkas utan laboratorietester. Problem i andra organ, såsom centrala nervsystemet (hjärna och ryggmärg) och lungor kan förekomma, men är mycket mindre vanligt än i hud, tarm och njurar.
Av de 40% av patienterna som utvecklar njurengagemang har nästan alla bevis (synliga eller vid urinanalys ) av blod i urinen. Mer än hälften har också proteinuri (protein i urinen), vilket i en åttondel är tillräckligt allvarligt för att orsaka nefrotiskt syndrom (generaliserad svullnad på grund av lågt proteininnehåll i blodet). Även om avvikelser vid urinalys kan fortsätta under lång tid, utvecklar endast 1% av alla HSP -patienter kronisk njursjukdom . Hypertoni (högt blodtryck) kan förekomma. Proteinförlust och högt blodtryck, liksom funktionerna i biopsi av njurarna om de utförs, kan förutsäga progression till avancerad njursjukdom. Vuxna är mer benägna än barn att utveckla avancerad njursjukdom.
Patofysiologi
Henoch – Schönlein purpura är en vaskulit i små kärl där komplex av immunglobulin A (IgA) och komplementkomponent 3 (C3) deponeras på arterioler, kapillärer och vener (därför är det en överkänslighetsreaktion av typ III). Som med IgA -nefropati är serumnivåerna av IgA höga i HSP och det finns identiska fynd på njurbiopsi; IgA -nefropati har dock en förkärlek för unga vuxna medan HSP är mer dominerande bland barn. Vidare påverkar IgA -nefropati vanligtvis bara njurarna medan HSP är en systemisk sjukdom. HSP involverar hud och bindväv, pungen, leder, mag -tarmkanalen och njurarna. Den genetiska grunden är fortfarande oklar förutom inblandning av genomets humana leukocytantigenregion. Det antas att autoimmunitet utlöses av infektioner, särskilt Staphylococcus aureus, Mycoplasma och adenovirus.
Diagnos
Diagnosen bygger på kombinationen av symtomen, eftersom väldigt få andra sjukdomar orsakar samma symptom tillsammans. Blodprov kan visa förhöjda kreatinin- och ureanivåer (vid njurinblandning), förhöjda IgA- nivåer (i cirka 50%) och förhöjda C-reaktiva proteiner (CRP) eller erytrocytsedimenteringshastighet (ESR) resultat; ingen är specifik för Henoch – Schönlein purpura. Den blodplättsräkning kan höjas, och skiljer den från sjukdomar där låga trombocyter är orsaken till purpura, såsom idiopatisk trombocytopenisk purpura och trombotisk trombocytopen purpura .
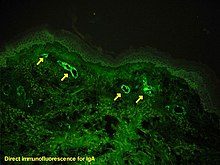
Om det råder tvivel om orsaken till hudskadorna kan en biopsi av huden utföras för att skilja purpuran från andra sjukdomar som orsakar den, såsom vaskulit på grund av kryoglobulinemi ; vid mikroskopi är uppträdandena av en överkänslighetsvaskulit , och immunfluorescens visar IgA och C3 (ett protein i komplementsystemet ) i blodkärlens vägg. De totala serumkomplementnivåerna är emellertid normala.
På grundval av symtom är det möjligt att skilja HSP från överkänslighetsvaskulit (HV). I en serie som jämför 85 HSP -patienter med 93 HV -patienter befanns fem symptom indikera HSP: påtaglig purpura, bukangina , matsmältningskanalblödning (inte på grund av intussussception), hematuri och ålder under 20. Förekomst av tre eller fler av dessa indikatorer har en 87% känslighet för att förutsäga HSP.
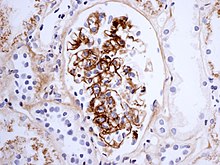
Biopsi av njuren kan utföras både för att fastställa diagnosen eller för att bedöma svårighetsgraden av redan misstänkt njursjukdom. De viktigaste resultaten på njurbiopsi är ökade celler och Ig -avsättning i mesangium (del av glomerulus , där blod filtreras), vita blodkroppar och utveckling av halvmånar . Förändringarna går inte att skilja från de som observerats vid IgA -nefropati .
HSP kan utvecklas efter infektioner med streptokocker ( β-hemolytisk, Lancefield grupp A ), hepatit B , herpes simplexvirus , parvovirus B19 , Coxsackievirus , adenovirus , Helicobacter pylori , mässling , påssjuka , röda hund , Mycoplasma och många andra. Läkemedel kopplade till HSP, vanligtvis som en idiosynkratisk reaktion, inkluderar antibiotika vancomycin och cefuroxim , ACE-hämmare enalapril och captopril , antiinflammatoriskt medel diklofenak , liksom ranitidin och streptokinas . Flera sjukdomar har rapporterats vara associerade med HSP, ofta utan orsakssamband. Endast i cirka 35% av fallen kan HSP spåras till någon av dessa orsaker.
Den exakta orsaken till HSP är okänd, men de flesta av dess egenskaper beror på avsättning av onormala antikroppar i blodkärlens vägg, vilket leder till vaskulit . Dessa antikroppar är av underklassen IgA 1 i polymerer ; det är osäkert om huvudorsaken är överproduktion (i matsmältningskanalen eller benmärgen ) eller minskat avlägsnande av onormalt IgA från cirkulationen. Det misstänks att abnormiteter i IgA 1 -molekylen kan ge en förklaring till dess onormala beteende i både HSP och det relaterade tillståndet IgA -nefropati . En av egenskaperna hos IgA 1 (och IgD ) är närvaron av en 18 aminosyralång "gångjärnsregion" mellan komplementfixerande områden 1 och 2. Av aminosyrorna är hälften prolin , medan de andra huvudsakligen är serin och treonin . Majoriteten av serinerna och treoninerna har genomarbetade sockerkedjor, anslutna genom syreatomer ( O-glykosylering ). Denna process tros stabilisera IgA -molekylen och göra den mindre benägen för proteolys . Det första sockret är alltid N-acetyl-galaktosamin (GalNAc), följt av andra galaktoser och sialinsyra . I HSP och IgAN verkar dessa sockerkedjor vara bristfälliga. Den exakta orsaken till dessa abnormiteter är inte känd.
Klassificering
Det finns flera standarder för att definiera Henoch – Schönlein purpura, inklusive 1990 års American College of Rheumatology (ACR) klassificering och 1994 Chapel Hill Consensus Conference (CHCC). Vissa har rapporterat att ACR -kriterierna är mer känsliga än CHCC: s.
Nyare klassificeringar, 2006 European League Against Rheumatism (EULAR) och Pediatric Rheumatology Society (PReS) -klassificering, inkluderar palperbar purpura som ett obligatoriskt kriterium, tillsammans med minst ett av följande resultat: diffus buksmärta, dominerande IgA -deponering (bekräftat på hudbiopsi), akut artrit i alla leder och njurinvolvering (vilket framgår av närvaron av blod och/eller protein i urinen).
Differentialdiagnos
Henoch – Schönlein purpura kan uppvisa en atypisk manifestation som kan förväxlas med papulär urtikaria , systemisk lupus erythematosus , meningokockemi , dermatit herpetiformis och akut hemorragiskt ödem i spädbarn .
Behandling
Från och med 2017 är det optimala sättet att behandla Henoch – Schönlein purpura kontroversiellt. Smärtstillande medel kan behövas för buksmärta och ledvärk. Sårvård är motiverad om huddöd och sår uppstår. Det är osäkert om HSP behöver behandling utöver att kontrollera symptomen. De flesta människor får inte terapi på grund av den höga spontana återhämtningsgraden. Experter är oense om huruvida man rutinmässigt ska använda kortikosteroider som behandling för HSP. Men om de ges tidigt i sjukdomsepisoden kan symptomens varaktighet förkortas och buksmärtor kan förbättras avsevärt. Dessutom kan risken för allvarliga njurproblem minskas. En systematisk granskning fann inga bevis för att steroidbehandling ( prednison ) är effektiv för att minska sannolikheten för att utveckla långvarig njursjukdom.
Bevis på förvärrad njurskada skulle normalt leda till en njurbiopsi. Behandling kan anges på grundval av utseendet på biopsiprovet; olika behandlingar kan användas, allt från steroider genom munnen till en kombination av intravenös metylprednisolon (steroid), cyklofosfamid och dipyridamol följt av prednison. Andra behandlingar inkluderar steroider/ azatioprin och steroider/ cyklofosfamid (med eller utan heparin och warfarin ). Intravenöst immunglobulin (IVIG) används ibland.
Det finns inga goda bevis för att behandling av barn som har HSP med trombocythämmande medel förhindrar ihållande njursjukdom. Det finns inte heller några bevis för att behandling av barn eller vuxna med cyklofosfamid förhindrar allvarlig njursjukdom. Heparinbehandling är inte motiverat.
Prognos
Övergripande prognos är bra för de flesta patienter, med en studie som visar återhämtning hos 94% respektive 89% av barnen och vuxna (vissa har behövt behandling). Hos barn under tio år återkommer tillståndet i ungefär en tredjedel av alla fall, vanligtvis inom fyra månader efter den första attacken. Återfall är vanligare hos äldre barn och vuxna.
Njurengagemang
Hos vuxna utvecklas njurengagemanget till njursjukdom i slutstadiet (ESKD) oftare än hos barn. I en brittisk serie med 37 patienter utvecklade 10 (27%) avancerad njursjukdom. Proteinuri, högt blodtryck vid presentation och patologiska egenskaper (halvmåneförändringar, interstitiell fibros och tubulär atrofi) förutsade progression. Ungefär 20% av barnen som uppvisar nefrotiska eller nefritiska drag upplever långvarig nedsatt njurfunktion.
Fynden på njurbiopsi korrelerar med svårighetsgraden av symtom: de med asymptomatisk hematuri kan bara ha fokal mesangial proliferation medan de med proteinuri kan ha markerad cellproliferation eller till och med halvmånebildning. Antalet crescentic glomeruli är en viktig prognostisk faktor för att avgöra om patienten kommer att utveckla kronisk njursjukdom.
I ESKD behöver vissa så småningom hemodialys eller motsvarande njurbytesbehandling (RRT). Om en njurtransplantation hittas för en patient på RRT kommer sjukdomen att återkomma i transplantatet (transplanterad njure) i cirka 35% av fallen, och i 11% kommer transplantatet att misslyckas helt (kräver återupptagande av RRT och en ytterligare transplantation ).
Epidemiologi
HSP förekommer oftare hos barn än hos vuxna och följer vanligtvis en övre luftvägsinfektion . Hälften av de drabbade patienterna är under sex år och 90% är under tio. Det förekommer ungefär dubbelt så ofta hos pojkar som hos tjejer. Den Förekomsten av HSP hos barn är cirka 20 per 100.000 barn per år, vilket gör den till den vanligaste vaskulit hos barn.
Fall av HSP kan inträffa när som helst under året, men vissa studier har funnit att färre fall uppstår under sommarmånaderna.
Historia
Sjukdomen är uppkallad efter Eduard Heinrich Henoch (1820–1910), en tysk barnläkare (brorson till Moritz Heinrich Romberg ) och hans lärare Johann Lukas Schönlein (1793–1864), som beskrev det på 1860 -talet. Schönlein associerade purpura och artrit, och Henoch purpura och gastrointestinal involvering. Den engelska läkaren William Heberden (1710–1801) och hudläkaren Robert Willan (1757–1812) hade redan beskrivit sjukdomen 1802 respektive 1808, men namnet Heberden – Willans sjukdom har fallit i onödan. William Osler var den första som kände igen den bakomliggande allergiska mekanismen för HSP.
Se även
Referenser
externa länkar
| Klassificering | |
|---|---|
| Externa resurser |