Sitagliptin - Sitagliptin
 | |
 | |
| Kliniska data | |
|---|---|
| Uttal |
/ S ɪ t ə ɡ l ɪ p t ɪ n / ( lyssna ) |
| Handelsnamn | Januvia, Tesavel, Xelevia, andra |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a606023 |
| Licensdata | |
| graviditet kategori |
|
| Vägar administrering |
Via mun |
| ATC -kod | |
| Rättslig status | |
| Rättslig status | |
| Farmakokinetiska data | |
| Biotillgänglighet | 87% |
| Proteinbindning | 38% |
| Ämnesomsättning | Lever ( CYP3A4 - och CYP2C8 -förmedlad) |
| Eliminering halveringstid | 8 till 14 timmar |
| Exkretion | Njurar (80%) |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.217.948 |
| Kemiska och fysiska data | |
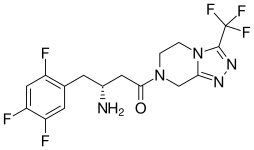
| Formel | C 16 H 15 F 6 N 5 O |
| Molmassa | 407,320 g · mol −1 |
| 3D -modell ( JSmol ) | |
| |
| |
| (kontrollera) | |
Sitagliptin , som bland annat säljs under varumärket Januvia , är ett läkemedel mot diabetes som används för att behandla typ 2-diabetes . I Storbritannien är det listat som mindre föredraget än metformin eller en sulfonylurea . Det tas genom munnen . Det finns även i den fasta doskombinationen medicinering sitagliptin / metformin (Janumet, Janumet XR).
Vanliga biverkningar inkluderar huvudvärk, svullnad i benen och infektioner i övre luftvägarna . Allvarliga biverkningar kan inkludera angioödem , lågt blodsocker , njurproblem , pankreatit och ledvärk . Om användning under graviditet eller amning är säker är oklart. Det är i dipeptidylpeptidas-4 (DPP-4) -inhibitorklassen och fungerar genom att öka produktionen av insulin och minska produktionen av glukagon i bukspottkörteln.
Sitagliptin utvecklades av Merck & Co. och godkändes för medicinsk användning i USA 2006. År 2019 var det den 88: e vanligaste förskrivna medicinen i USA, med mer än 8 miljoner recept.
Medicinsk användning
Sitagliptin används för att behandla typ 2 -diabetes. Det är i allmänhet mindre föredraget än metformin eller sulfonylurea . Det tas genom munnen. Det är också tillgängligt som kombinationer med fast dos av sitagliptin/metformin (Janumet, Janumet XR) och sitagliptin/simvastatin (Juvisync).
Sitagliptin ska inte användas för att behandla typ 1 -diabetes. I december 2020 godkände US Food and Drug Administration (FDA) märkningsändringar som säger att Januvia (sitagliptin), Janumet (sitagliptin och metforminhydroklorid) och Janumet XR (sitagliptin och metforminhydroklorid förlängd frisättning) inte har visat sig förbättra glykemiska ( blodsocker) kontroll hos barn i åldern 10 till 17 år med typ 2 -diabetes. Läkemedlen är godkända för att förbättra blodsockerkontrollen hos vuxna 18 år och äldre med typ 2 -diabetes.
Biverkningar
Biverkningar från sitagliptin liknar placebo , med undantag för sällsynta illamående , vanliga förkylningsliknande symptom och ljuskänslighet. Det ökar inte risken för diarré. Det finns ingen signifikant skillnad i förekomsten av hypoglykemi mellan placebo och sitagliptin. Hos dem som tar sulfonylurea ökar risken för lågt blodsocker .
Förekomsten av sällsynta fallrapporter om njursvikt och överkänslighetsreaktioner noteras i USA föreskrivande information, men en orsakande roll för sitagliptin har inte fastställts.
Flera eftermarknadsföringsrapporter om pankreatit (en del dödlig) har gjorts hos personer som behandlats med sitagliptin och andra DPP-4-hämmare, och den amerikanska bipacksedeln varnar för detta, även om orsakssambandet mellan sitagliptin och pankreatit ännu inte är fullständigt underbyggt . En studie med labråttor som publicerades 2009 drog slutsatsen att några av de möjliga riskerna för pankreatit eller bukspottskörtelcancer kan minska när de används tillsammans med metformin. Även om DPP-4-hämmare visade en ökning av sådana riskfaktorer, från och med 2009, har ingen ökning av bukspottskörtelcancer rapporterats hos personer som tar DPP-4-hämmare.
År 2015 lade US Food and Drug Administration (FDA) till en ny varning och försiktighetsåtgärd om risken för "allvarlig och handikappande" ledvärk på etiketterna för alla DPP-4-hämmande läkemedel.
Handlingsmekanism
Sitagliptin arbetar för att kompetitivt inhiberar den enzym dipeptidylpeptidas 4 (DPP-4). Detta enzym bryter ner inkretinerna GLP-1 och GIP, gastrointestinala hormoner som frigörs som svar på en måltid. Genom att förhindra nedbrytning av GLP-1 och GIP kan de öka utsöndringen av insulin och undertrycka frisättningen av glukagon av alfacellerna i bukspottkörteln. Detta driver blodsockernivån mot det normala. När blodsockernivån närmar sig normal, minskar mängden insulin som frigörs och glukagon undertrycks, vilket tenderar att förhindra ett "överskott" och efterföljande lågt blodsocker (hypoglykemi), vilket ses med några andra orala hypoglykemiska medel.
Sitagliptin har visat sig sänka HbA1c -nivån med cirka 0,7% -poäng jämfört med placebo. Det är något mindre effektivt än metformin när det används som monoterapi . Det orsakar inte viktökning och har mindre hypoglykemi jämfört med sulfonylurea. Sitagliptin rekommenderas som ett andra läkemedel (i kombination med andra läkemedel) efter att kombinationen av kost/träning och metformin misslyckats.
Historia
Sitagliptin godkändes av US Food and Drug Administration den 17 oktober 2006 och marknadsförs i USA som Januvia av Merck & Co. Den 2 april 2007 godkände FDA en oral kombination av sitagliptin/metformin som marknadsförs i USA som Janumet. Den 7 oktober 2011 godkände FDA en oral kombination av sitagliptin/simvastatin som marknadsförs i USA som Juvisync.
Referenser
externa länkar
- "Sitagliptin" . Läkemedelsinformationsportal . US National Library of Medicine.
- "Sitagliptinfosfat" . Läkemedelsinformationsportal . US National Library of Medicine.
