Neurostimulering - Neurostimulation
| Neurostimulering | |
|---|---|
| OPS-301-kod | 8-631 |
Neurostimulering är den målmedvetna moduleringen av nervsystemets aktivitet med hjälp av invasiva (t.ex. mikroelektroder ) eller icke-invasiva medel (t.ex. transkraniell magnetisk stimulering eller transkraniell elektrisk stimulering , tES, såsom tDCS eller transkraniell växelströmsstimulering , tACS). Neurostimulering avser vanligtvis de elektromagnetiska tillvägagångssätten för neuromodulering .
Neurostimuleringsteknik kan förbättra livskvaliteten för dem som är kraftigt förlamade eller lider av stora förluster för olika sinnesorgan, liksom för permanent minskning av svår, kronisk smärta som annars skulle kräva konstant (dygnet runt) hög dos opioidbehandling (såsom neuropatisk smärta och ryggmärgsskada). Det fungerar som en viktig del av neurala proteser för hörapparater , konstgjord syn, konstgjorda lemmar och hjärn-maskin-gränssnitt . När det gäller neural stimulering används mestadels en elektrisk stimulering och laddningsbalanserade bifasiska konstanta strömvågformer eller kapacitivt kopplade laddningsinjektionsmetoder antas. Alternativt har transkraniell magnetisk stimulering och transkraniell elektrisk stimulering föreslagits som icke-invasiva metoder där antingen ett magnetfält eller transkraniellt applicerade elektriska strömmar orsakar neurostimulering.
Hjärnstimulering
Hjärnstimulering har potential att behandla vissa sjukdomar som epilepsi . I denna metod tillämpas schemalagd stimulering på specifika kortikala eller subkortiska mål. Det finns kommersiella enheter som kan leverera en elektrisk puls vid schemalagda tidsintervaller. Schemalagd stimulering antas förändra de inneboende neurofysiologiska egenskaperna hos epileptiska nätverk. De mest utforskade målen för schemalagd stimulering är thalamus och hippocampus främre kärna . Thalamus främre kärna har studerats, vilket har visat en signifikant minskning av anfall med stimulatorn på kontra av under flera månader efter stimulatorimplantation. Dessutom kan klusterhuvudvärken (CH) behandlas med hjälp av en tillfällig stimulerande elektrod vid sphenopalatin -ganglion (SPG). Smärtlindring rapporteras inom flera minuter efter stimulering i denna metod. För att undvika användning av implanterade elektroder har forskare konstruerat sätt att skriva in ett "fönster" av zirkoniumoxid som har modifierats för att vara transparent och implanterat i mössskallar, för att låta optiska vågor tränga djupare in, som i optogenetik , för att stimulera eller hämma enskilda neuroner.
Djup hjärnstimulering
Djup hjärnstimulering (DBS) har visat fördelar för rörelsestörningar som Parkinsons sjukdom , tremor och dystoni och affektiva störningar som depression , tvångssyndrom , Tourettes syndrom , kronisk smärta och klusterhuvudvärk. Eftersom DBS direkt kan ändra hjärnaktiviteten på ett kontrollerat sätt används den för att kartlägga grundläggande mekanismer för hjärnans funktioner tillsammans med neuroimaging -metoder.
Ett enkelt DBS -system består av två olika delar. Först implanteras små mikroelektroder i hjärnan för att leverera stimuleringspulser till vävnaden. För det andra genererar en elektrisk pulsgenerator (PG) stimuleringspulser, som den skickar till elektroderna genom mikrokablar.
Tillämpningen och effekterna av DBS, på både normala och sjuka hjärnor, involverar många parametrar. Dessa inkluderar hjärnvävnadens fysiologiska egenskaper, som kan förändras med sjukdomstillstånd. Viktiga är också stimuleringsparametrarna, såsom amplitud och tidsegenskaper, och den geometriska konfigurationen av elektroden och vävnaden som omger den.
Trots ett stort antal studier på DBS är dess verkningsmekanism fortfarande inte väl förstådd. Att utveckla DBS -mikroelektroder är fortfarande utmanande.
Icke-invasiv för hjärnstimulering
Transkraniell magnet för stimulering
Jämfört med elektrisk stimulering som använder kort, högspännings elektrisk stöt för att aktivera neuroner, som potentiellt kan aktivera smärtfibrer, utvecklades transkraniell magnetisk stimulering (TMS) av Baker 1985. TMS använder en magnetisk tråd ovanför hårbotten , som bär en skarp och hög strömpuls. Ett tidsvariant magnetfält induceras vinkelrätt mot spolen på grund av den applicerade pulsen som följaktligen genererar ett elektriskt fält baserat på Maxwells lag. Det elektriska fältet ger den nödvändiga strömmen för en icke-invasiv och mycket mindre smärtsam stimulans. Det finns två TMS -enheter som kallas enkelpuls -TMS och repetitiv puls -TMS (rTMS) medan den senare har större effekt men kan orsaka anfall. TMS kan användas för terapi, särskilt inom psykiatri , som ett verktyg för att mäta central motorisk ledning och ett forskningsverktyg för att studera olika aspekter av mänsklig hjärnfysiologi såsom motorisk funktion, syn och språk. RTMS -metoden har använts för att behandla epilepsi med frekvenser på 8–25 Hz i 10 sekunder. De andra terapeutiska användningarna av rTMS inkluderar parkinsonsjukdomar, dystoni och humörsjukdomar. TMS kan också användas för att bestämma hur kortikala nätverk bidrar till specifika kognitiva funktioner genom att störa aktiviteten i fokal hjärnregionen. Tidiga, otydliga resultat har erhållits vid återhämtning från koma ( ihållande vegetativt tillstånd ) av Pape et al. (2009).
Transkraniell elektrisk stimulering
- Transkraniell likströmsstimulering (tDCS)
- Transkraniell växelströmsstimulering (tACS)
- Transkraniell pulsad strömstimulering (tPCS)
- Transkraniell slumpmässig brusstimulering (tRNS)
Ryggmärgsstimulering
Ryggmärgsstimulering (SCS) är en effektiv behandling för behandling av kronisk och svårlöslig smärta, inklusive diabetisk neuropati , misslyckat ryggkirurgiskt syndrom , komplext regionalt smärtsyndrom , fantomsmärta , ischemisk lemvärk , eldfast ensidigt ledsmärta, postherpetisk neuralgi och akut herpes zoster smärta. Ett annat smärttillstånd som är en potentiell kandidat för SCS-behandling är Charcot-Marie-Tooth (CMT) sjukdom, som är förknippad med måttlig till svår kronisk extremitetsvärk. SCS -terapi består av elektrisk stimulering av ryggmärgen för att "maskera" smärta. Den grindteorin föreslås i 1965 av Melzack och Wall tillhandahålls en teoretisk konstruktion för att försöka SCS som en klinisk behandling för kronisk smärta. Denna teori postulerar att aktivering av myeliniserade primära afferenta fibrer med stor diameter undertrycker svaret från dorsala hornneuroner vid inmatning från små, omyeliniserade primära afferenter. Ett enkelt SCS -system består av tre olika delar. För det första implanteras mikroelektroder i epiduralrummet för att leverera stimuleringspulser till vävnaden. För det andra, en elektrisk pulsgenerator implanterad i det nedre bukområdet eller glutealområdet medan den är ansluten till elektroderna via trådar, och för det tredje en fjärrkontroll för att justera stimulansparametrarna såsom pulsbredd och pulsfrekvens i PG. Förbättringar har gjorts både i de kliniska aspekterna av SCS, såsom övergång från subdural placering av kontakter till epidural placering, vilket minskar risken och sjukligheten för SCS-implantation, och även tekniska aspekter av SCS såsom förbättring av perkutana ledningar och fullt implanterbar multi- kanalstimulatorer. Det finns dock många parametrar som måste optimeras, inklusive antal implanterade kontakter, kontaktstorlek och avstånd, och elektriska källor för stimulering. Stimulanspulsbredden och pulsfrekvensen är viktiga parametrar som måste justeras i SCS, som vanligtvis är 400 us respektive 8–200 Hz.
Transkutan supraorbital nervstimulering
Preliminärt bevis stöder transkutan supraorbital nervstimulering. Biverkningar är få.
Cochleaimplantat
Cochleaimplantat har gett partiell hörsel till mer än 120 000 personer världen över från och med 2008. Den elektriska stimuleringen används i ett cochleaimplantat för att ge funktionell hörsel hos helt döva. Cochleaimplantat inkluderar flera delsystemkomponenter från den externa talprocessorn och radiofrekvens (RF) överföringslänk till den interna mottagaren, stimulatorn och elektrodmatriserna. Modern forskning på cochleaimplantat startade på 1960- och 1970 -talen. 1961 implanterades en rå enda elektrodanordning i två döva patienter och användbar hörsel med elektrisk stimulering rapporterades. Den första FDA-godkända kompletta enkelkanalsenheten släpptes 1984. I cochleaimplantat tas ljudet upp av en mikrofon och överförs till den bakom örat externa processorn för att konverteras till digital data. De digitaliserade data moduleras sedan på en radiofrekvenssignal och överförs till en antenn inuti ett huvudstycke. Data- och kraftbäraren överförs via ett par kopplade spolar till den hermetiskt förslutna inre enheten. Genom att extrahera kraften och demodulera data skickas kommandon för elektrisk ström till snäckan för att stimulera hörselnerven genom mikroelektroder. Nyckelpunkten är att den interna enheten inte har ett batteri och den ska kunna extrahera den nödvändiga energin. För att minska infektionen överförs data trådlöst tillsammans med ström. Induktivt kopplade spolar är bra kandidater för kraft- och datatelemetri, även om radiofrekvensöverföring kan ge bättre effektivitet och datahastigheter. Parametrar som behövs av den interna enheten inkluderar pulsamplituden, pulslängd, pulsgap, aktiv elektrod och returelektrod som används för att definiera en bifasisk puls och stimuleringsläget. Ett exempel på de kommersiella enheterna inkluderar Nucleus 22 -enhet som utnyttjade en bärvågsfrekvens på 2,5 MHz och senare i den nyare versionen som kallas Nucleus 24 -enhet ökades bärfrekvensen till 5 MHz. Den interna enheten i cochleaimplantaten är ett ASIC - chip ( applikationsspecifikt integrerat kretslopp ) som ansvarar för säker och pålitlig elektrisk stimulering. Inuti ASIC -chipet finns det en framåtgående väg, en bakåtgående väg och styrenheter. Framåtvägen återställer digital information från RF -signalen som inkluderar stimuleringsparametrar och några handskakningsbitar för att minska kommunikationsfelet. Den bakåtgående vägen innehåller vanligtvis en provtagare för bakre telemetri som läser spänningen över en tidsperiod på inspelningselektroden. Stimulatorblocket är ansvarigt för att leverera förutbestämd ström av extern enhet till mikroelektroderna. Detta block inkluderar en referensström och en digital till analog omvandlare för att omvandla digitala kommandon till en analog ström.
Visuell protes
Teoretiska och experimentella kliniska bevis tyder på att direkt elektrisk stimulering av näthinnan kan ge visioner för personer som har tappat fotoreceptiva element i näthinnan . Därför utvecklas visuella proteser för att återställa syn för blinda genom att använda stimuleringen. Beroende på vilken visuell vägplats som är inriktad på neural stimulering har olika tillvägagångssätt övervägts. Visuell väg består huvudsakligen av ögat , synnerven , lateral geniculate nucleus (LGN) och visuell cortex . Därför är retinal, optisk nerv och visuell cortex stimulering de tre olika metoderna som används i visuella proteser. Retinala degenerativa sjukdomar, såsom retinitis pigmentosa (RP) och åldersrelaterad makuladegeneration (AMD), är två troliga kandidatsjukdomar där retinalstimulering kan vara till hjälp. Tre tillvägagångssätt som kallas intraokulär epiretinal, subretinal och extraokulär transretinal stimulans följs i retinalanordningar som stimulerar kvarvarande retinala neurala celler att kringgå förlorade fotoreceptorer och låta den visuella signalen nå hjärnan via den normala synvägen. Vid epiretinalt tillvägagångssätt placeras elektroder på ovansidan av näthinnan nära ganglionceller , medan elektroderna placeras under näthinnan i subretinala tillvägagångssätt. Slutligen är den bakre sklerala ytan av ögat den plats där extraokulära inflygningselektroder är placerade. Second Sight och Humayun -gruppen vid USC är de mest aktiva grupperna i utformningen av intraokulära retinalproteser. ArgusTM 16 retinalimplantatet är en intraokulär retinalprotes som använder teknik för videoprocessering. När det gäller den visuella cortexstimuleringen var Brindley och Dobelle de första som gjorde experimenten och visade att genom att stimulera ovansidan av den visuella cortexen kan de flesta elektroderna producera visuell uppfattning. På senare tid byggde Sawan ett komplett implantat för intrakortikal stimulering och validerade operationen hos råttor.
LGN, som ligger i mitthjärnan för att vidarebefordra signaler från näthinnan till den visuella cortexen, är ett annat potentiellt område som kan användas för stimulering. Men detta område har begränsad tillgång på grund av kirurgiska svårigheter. Den senaste tidens framgångar med djupa hjärnstimuleringstekniker som riktar sig mot mitthjärnan har uppmuntrat forskningen att fortsätta tillvägagångssättet för LGN -stimulering för en visuell protes.
Hjärtelektrostimuleringsanordningar
Implanterbara pacemaker föreslogs för första gången 1959 och blev mer sofistikerade sedan dess. Den terapeutiska tillämpningen av pacemakers består av många rytmstörningar, inklusive vissa former av takykardi (för snabb hjärtslag), hjärtsvikt och till och med stroke . Tidiga implanterbara pacemaker arbetade bara en kort tid och behövde periodisk laddning med en induktiv länk. Dessa implanterbara pacemakrar behövs en pulsgenerator för att stimulera hjärtmuskulaturen med en viss hastighet utöver elektroder. Idag programmeras moderna pulsgeneratorer icke-invasivt av sofistikerade datoriserade maskiner som använder RF, för att få information om patientens och enhetens status genom telemetri. De använder också en enda hermetiskt förseglad litiumjodid (LiI) cell som batteri. Pacemakerkretsarna inkluderar avkänningsförstärkare för att detektera hjärtats inneboende elektriska signaler, som används för att spåra hjärtaktivitet, hastighetsadaptiv krets, som bestämmer behovet av ökad eller minskad stimuleringsfrekvens, en mikroprocessor, minne för att lagra parametrarna, telemetrikontroll för kommunikation protokoll och strömförsörjning för att tillhandahålla reglerad spänning.
Stimulering mikroelektrod teknik
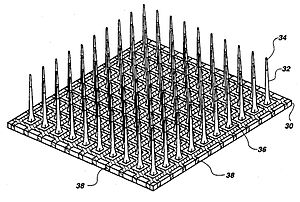
Mikroelektroder är en av nyckelkomponenterna i neurostimuleringen, som levererar strömmen till neuroner. Typiska mikroelektroder har tre huvudkomponenter: ett substrat ( bäraren ), ett ledande metallskikt och ett isoleringsmaterial. I cochleaimplantat bildas mikroelektroder från platina-iridiumlegering . Toppmoderna elektroder inkluderar djupare insättning för att bättre matcha den tonotopiska platsen för stimulering till frekvensbandet som tilldelas varje elektrodkanal, vilket förbättrar stimuleringens effektivitet och minskar insättningsrelaterat trauma. Dessa elektroder för cochleaimplantat är antingen raka eller spiralformade, till exempel Med El Combi 40+ respektive Advanced Bionics Helix mikroelektroder. I visuella implantat finns det två typer av elektroduppsättningar som kallas plan typ eller tredimensionell nål eller pelartyp, där nåltypsuppsättning som Utah -array mest används för kortikala och optiska nervstimuleringar och sällan används i retinalimplantat på grund av den eventuella skadan av näthinnan. Emellertid, en pelare-formade guld elektroduppsättningen på tunnfilms polyimid har använts i en extraokulär implantat. Å andra sidan bildas plana elektroduppsättningar av flexibla polymerer, såsom silikon , polyimid och Parylene som kandidater för näthinnesimplantat. När det gäller DBS -mikroelektroder skulle en array, som kan styras oberoende, fördelad över målkärnan möjliggöra exakt kontroll av den rumsliga fördelningen av stimuleringen och därmed möjliggöra bättre personlig DBS. Det finns flera krav på DBS-mikroelektroder som inkluderar lång livslängd utan skada på vävnaden eller nedbrytning av elektroderna, anpassade för olika hjärnplatser, långsiktig biokompatibilitet för materialet, mekaniskt hållbar för att nå målet utan att skadas under hantering av implantatkirurgen och slutligen enhetlighet i prestanda över mikroelektroderna i en viss grupp. Volfram micro, iridium- mikrotrådar, och finfördelat eller galvan Platina-iridiumlegering mikroelektroder är de exempel på mikroelektrod som används i DBS. Kiselkarbid är ett potentiellt intressant material för att förverkliga biokompatibla halvledaranordningar.
Historia
De primära resultaten om neurostimulering härstammar från idén att stimulera nerver för terapeutiska ändamål. Den första registrerade användningen av elektrisk stimulering för smärtlindring går tillbaka till 46 e.Kr., då Scribonius Largus använde torpedofisk (elstråle) för att lindra huvudvärk. I slutet av 1700 -talet upptäckte Luigi Galvani att musklerna i döda groda ben ryckte när de träffades av likström på nervsystemet. Modulationen av hjärnaktiviteten genom elektrisk stimulering av motorbarken hos hundar visades 1870 vilket resulterade i extremiteter. Från slutet av 1700 -talet till idag har många milstolpar utvecklats. Numera, sensoriska protesanordningar, såsom synimplantat, cochleaimplantat, hörselimplantat i hjärnan och ryggmärgsstimulatorer och även motorproteser, till exempel djupa hjärnstimulatorer, Bion-mikrostimulatorer, hjärnans kontroll- och avkänningsgränssnitt och elektrostimuleringsanordningar i hjärtat används flitigt.
År 2013 myntade det brittiska läkemedelsföretaget GlaxoSmithKline (GSK) termen "elektroceutisk" för att i stort omfatta medicintekniska produkter som använder elektrisk, mekanisk eller ljusstimulering för att påverka elektrisk signalering i relevanta vävnadstyper. Kliniska neurala implantat, såsom cochleaimplantat för att återställa hörseln, näthinnesimplantat för att återställa synen, ryggmärgsstimulatorer för smärtlindring eller hjärtstimulatorer och implanterbara defibrillatorer är föreslagna exempel på elektriska apparater. GSK bildade en riskkapitalfond och sa att det skulle vara värd för en konferens 2013 för att lägga fram en forskningsagenda för området. En 2016 -granskning av forskning om interaktioner mellan nervsystemet och immunsystemet vid autoimmuna sjukdomar nämnde "elektroceuticals" i förbifarten och citattecken, med hänvisning till neurostimuleringsanordningar under utveckling för tillstånd som artrit.
Forskning
Förutom den enorma användningen av neurostimulering för kliniska tillämpningar, används den också i stor utsträckning i laboratorier som började från 1920 -talet av människor som Delgado som använde stimulering som en experimentell manipulation för att studera grunderna i hur hjärnan fungerar. De primära verken var på hjärnans belöningscentrum där stimulering av dessa strukturer ledde till nöje som krävde mer stimulans. Ett annat senaste exempel är den elektriska stimuleringen av MT -området i den primära visuella cortexen till partiskhet. I synnerhet representeras rörelsens riktning på ett regelbundet sätt i MT -området. De presenterade apor med rörliga bilder på skärmen och apen genomströmning var att bestämma vad riktningen är. De fann att genom att systematiskt införa några fel i apans svar, genom att stimulera MT -området som är ansvarigt för att uppfatta rörelsen i en annan riktning, svarade apan någonstans mellan den faktiska rörelsen och den stimulerade. Detta var en elegant användning av stimulans för att visa att MT -området är viktigt i själva uppfattningen av rörelse. Inom minnesfältet används stimulering mycket ofta för att testa styrkan hos förbindelsen mellan ett bunt celler till ett annat genom att applicera en liten ström i en cell vilket resulterar i frisättning av signalsubstanser och mätning av den postsynaptiska potentialen .
Generellt hjälper en kort men högfrekvent ström i intervallet 100 Hz att stärka anslutningen som kallas långsiktig potentiering . Längre men lågfrekvent ström tenderar dock att försvaga anslutningarna som kallas långvarig depression .