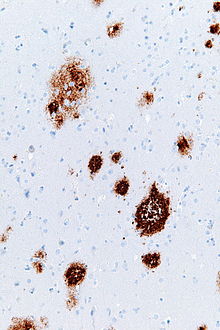
Amyloid -plack - Amyloid plaques
Amyloidplack (även känd som neuritiska plack , Aβ -plack eller senila plack ) är extracellulära avlagringar av amyloid beta (Aβ) -proteinet huvudsakligen i hjärnans grå substans . Degenerativa neuronelement och ett överflöd av mikroglia och astrocyter kan associeras med amyloidplack. Vissa plack förekommer i hjärnan till följd av åldrande (åldrande), men ett stort antal plack och neurofibrillära nystan är kännetecknen för Alzheimers sjukdom . Onormala neuriter i amyloidplack är krångliga, ofta svullna axoner och dendriter . Neuriterna innehåller en mängd olika organeller och cellulärt skräp, och många av dem inkluderar karakteristiska parade spiralformade filament , den ultrastrukturella komponenten i neurofibrillära trassel. Placken är mycket varierande i form och storlek; i vävnadssektioner immunfärgade för Aβ, innefattar de en log-normal storleksfördelningskurva med en genomsnittlig plackyta på 400-450 kvadrat mikrometer (µm²). De minsta placken (mindre än 200 µm²), som ofta består av diffusa avlagringar av Aβ, är särskilt många. Plackernas skenbara storlek påverkas av typen av fläckar som används för att detektera dem, och av planet genom vilket de sektioneras för analys under mikroskopet. Plack bildas när Aβ fälls ihop och aggregeras till oligomerer och längre polymerer , av vilka de senare är karakteristiska för amyloid . Misstänkt och aggregerat Aβ anses vara neurotoxiskt , särskilt i dess oligomera tillstånd.
Historia
År 1892 beskrev Paul Blocq och Gheorghe Marinescu först förekomsten av plack i grå substans. De hänvisade till placken som "knölar av neuroglial skleros". År 1898 rapporterade Emil Redlich plack hos tre patienter, varav två hade kliniskt verifierat demens . Redlich använde termen "miliär skleros" för att beskriva plack eftersom han tyckte att de liknade hirsfrön, och han var den första som hänvisade till lesionerna som "plack". I början av 1900-talet noterade Oskar Fischer deras likhet med actinomyces 'Drusen' (geode-liknande lesioner), vilket ledde till att han kallade degenerativa processen 'drusige Nekrose'. Alois Alzheimer krediteras ofta för att först koppla plack till demens i en presentation från 1906 (publicerad 1907), men denna korta rapport fokuserade främst på neurofibrillära trassel och plack nämndes bara kort. Alzheimers första materiella beskrivning av plack uppträdde 1911. Däremot publicerade Oskar Fischer en rad omfattande undersökningar av plack och demens 1907, 1910 och 1912. År 1911 föreslog Max Bielschowsky plackavlagringar av amyloid-karaktär. Detta bekräftades senare av Paul Divry, som visade att plack som är färgade med färgämnet Kongoröd visar den optiska egenskapen för dubbelbrytning , som är karakteristisk för amyloider i allmänhet. År 1911 introducerade Teofil Simchowicz termen 'senila plack' för att beteckna deras frekventa närvaro i hjärnan hos äldre individer. År 1968 bekräftade en kvantitativ analys av Gary Blessed, Bernard Tomlinson och Martin Roth sambandet mellan senila plack med demens . Henryk Wisniewski och Robert Terry myntade termen 'neuritiska plack' 1973 för att beteckna plack som inkluderar onormala neuronala processer (neuriter). Ett viktigt framsteg 1984 och 1985 var identifiering av Aβ som proteinet som bildar kärnorna på plack. Denna upptäckt ledde till att nya verktyg skapades för att studera plack, särskilt antikroppar mot Aβ, och presenterade ett molekylärt mål för utveckling av potentiella terapier för Alzheimers sjukdom. Kunskap om aminosyrasekvensen för Aβ gjorde det också möjligt för forskare att upptäcka genetiska mutationer som orsakar autosomalt dominant Alzheimers sjukdom, som alla ökar sannolikheten för att Aβ kommer att samlas i hjärnan.
Generationen av amyloid beta
Amyloid beta (Aβ) är ett litet protein, oftast 40 eller 42 aminosyror i längd, som frigörs från ett längre moderprotein som kallas Aβ-prekursorproteinet (APP). APP produceras av många celltyper i kroppen, men det är särskilt rikligt i neuroner . Det är ett enkelpassat transmembranprotein , det vill säga det passerar en gång genom cellmembranen . Ap -segmentet i APP är delvis inom membranet och delvis utanför membranet. För att frigöra Aβ klyvs APP sekventiellt av två enzymer : för det första av betasekretas (eller β-amyloid-klyvningsenzym (BACE)) utanför membranet, och för det andra av gammasekretas (γ-sekretas), ett enzymkomplex inom membranet . De sekventiella verkningarna av dessa sekretaser resulterar i Aβ -proteinfragment som släpps ut i det extracellulära utrymmet Urladdningen av Aβ ökas av synapsenas aktivitet . Förutom Aβ -peptider som är 40 eller 42 aminosyror långa genereras också flera mindre rikliga Aβ -fragment. Aβ kan modifieras kemiskt på olika sätt, och proteinets längd och kemiska modifieringar kan påverka både dess tendens att aggregera och dess toxicitet.
Identifiering

Amyloidplack är synliga med ljusmikroskop med hjälp av olika färgningstekniker, inklusive silverfärgningar , röd Kongo , tioflavin , kresylviolett , PAS-reaktionen , och luminiscerande konjugerade oligothiophenes (LCoS). Dessa metoder färgar ofta olika komponenter i placken, och de varierar i deras känslighet Plack kan också visualiseras immunhistokemiskt med antikroppar riktade mot Aβ eller andra komponenter i lesionerna. Immunhistokemiska fläckar är särskilt användbara eftersom de är både känsliga och specifika för antigener som är associerade med plack.
Sammansättning
Aβ -avlagringar som omfattar amyloidplack är varierande i storlek och utseende. Under ljusmikroskopet sträcker de sig från små, klumpiga ansamlingar som har några mikron i diameter till mycket större täta eller diffusa massor. Så kallade 'klassiska plack' består av en kompakt Aβ-amyloidkärna som omges av en corona av något mindre tätt packad Aβ. Klassiska plack inkluderar också onormala, svullna neuronala processer ( neuriter ) som härrör från många olika typer av neuroner, tillsammans med aktiverade astrocyter och mikroglia . Onormala neuriter och aktiverade glialceller är inte typiska för de flesta diffusa plack, och det har föreslagits att diffusa avlagringar är ett tidigt skede i utvecklingen av plack.
Anatomisk fördelning
Dietmar Thal och hans kollegor har föreslagit en sekvens av stadier av plackbildning i hjärnan hos Alzheimers patienter I fas 1 visas plack i neocortex ; i fas 2 förekommer de i allocortex , hippocampusbildning och amygdala ; i fas 3 påverkas de basala ganglierna och diencephalon ; i fas 4 uppträder plack i mitthjärnan och medulla oblongata ; och i fas 5 visas de i pons och lillhjärnan . Således kan plack i slutstadiet av Alzheimers sjukdom hittas i de flesta delar av hjärnan. De är ovanliga i ryggmärgen .
Bildande och spridning
Den normala funktionen hos Aβ är inte säker, men plack uppstår när proteinet fälls fel och börjar ackumuleras i hjärnan genom en process av molekylär mallning ('sådd'). Mathias Jucker och Lary Walker har liknat denna process med bildandet och spridningen av prioner vid sjukdomar som kallas spongiforma encefalopatier eller prionsjukdomar . Enligt prionparadigmet, fälls vissa proteiner fel till former som är rika på beta-ark sekundär struktur . I detta tillstånd får de andra proteiner av samma typ att anta samma onormala beta-arkrika struktur. De felveckade proteinerna håller fast vid varandra och staplas så småningom samman för att bilda oligomerer som smälter samman för att göra amyloidfibrillerna som är typiska för mogna plack.
Deltagande i sjukdom
Rikliga Aβ -plack, tillsammans med neurofibrillära trassel som består av aggregerat tauprotein , är de två skador som krävs för den neuropatologiska diagnosen Alzheimers sjukdom. Även om antalet neurofibrillära trassel korrelerar starkare med graden av demens än antalet plack, indikerar genetiska och patologiska fynd att Aβ spelar en central roll i risken, uppkomsten och utvecklingen av Alzheimers sjukdom. Av särskild betydelse är de längre (42 aminosyror) arterna av Aβ som kallas Aβ42. Förhöjda nivåer av Aβ, liksom en ökning av förhållandet mellan Aβ42 och 40-aminosyraformen (Aβ40), är viktiga tidiga händelser i patogenesen av Alzheimers sjukdom.
Fram till nyligen krävde diagnosen Alzheimers sjukdom en mikroskopisk analys av plack och trassel i hjärnvävnad, vanligtvis vid obduktion. Men Aβ-plack (tillsammans med cerebral Aβ-amyloid angiopati ) kan nu detekteras i hjärnan hos levande försökspersoner. Detta görs genom att förbereda radiomärkta medel som selektivt binder till Aβ -avlagringar i hjärnan efter att de har infunderats i blodomloppet. De ligander korsa blod-hjärnbarriären och fäst till aggregerad Ap, och deras retention i hjärnan bedöms av positronemissionstomografi (PET). Dessutom kan förekomsten av plack och trassel uppskattas genom att mäta mängden Aβ- och tau -proteiner i cerebrospinalvätskan .
Förekomst
Sannolikheten för att ha plack i hjärnan ökar med stigande ålder. Från 60 års ålder (10%) till 80 års ålder (60%) ökar andelen människor med senila plack linjärt. Kvinnor är något mer benägna att få plack än män. Både plack och Alzheimers sjukdom är också vanligare hos åldrande personer med trisomi -21 ( Downs syndrom ). Detta antas bero på överproduktion av Aβ eftersom APP -genen finns på kromosom 21, som finns som tre kopior i Downs syndrom.
Amyloidplack förekommer naturligt i åldrande hjärnor hos icke -mänskliga arter, allt från fåglar till stora apor. I icke -mänskliga primater, som är de närmaste biologiska släktingarna till människor, har plack hittats i alla arter som undersökts hittills. Neurofibrillära trassel är dock sällsynta och inga icke -mänskliga arter har visat sig ha demens tillsammans med den fullständiga neuropatologin vid Alzheimers sjukdom.
Forskning
Forskning har riktats mot att förstå de biokemiska , cytologiska och inflammatoriska egenskaperna hos plack, bestämma hur plack uppstår och sprida sig i hjärnan, identifiera genetiska och miljömässiga riskfaktorer, upptäcka metoder för att upptäcka dem i den levande hjärnan och utveckla terapeutiska strategier för att förebygga eller ta bort dem. Forskning om bildning och spridning av amyloidplack har påskyndats av utvecklingen av genetiskt modifierade musmodeller. Trots vissa begränsningar har dessa modeller också bidragit till upptäckten av nya terapeutiska strategier. Till exempel har en växande mängd behandlingar som reducerar Aβ -nivåer och antalet plack i hjärnan identifierats med hjälp av transgena gnagarmodeller. Dessa strategier inkluderar immunterapeutiska tillvägagångssätt och hämmare av sekretaserna som frigör Ap från APP. Sådana behandlingar utvärderas nu kliniskt för behandling av Alzheimers sjukdom. Fynden hittills tyder på att avlägsnande av plack hos patienter med demens är till liten nytta, möjligen eftersom hjärnan är allvarligt skadad när tecken och symtom på Alzheimers sjukdom först uppträder. Mikroglia-medierad plackbildning kan i själva verket vara fördelaktig genom att inkapsla Aβ i täta plackkärnor. Av denna anledning tror många forskare att tidigare hämning av Aβ -aggregering och plackbildning behövs för att bromsa eller förhindra tauopati och demens av Alzheimers sjukdom. Annan forskning är inriktad på att förstå inflammationen som ofta är förknippad med plack eller identifiera miljömässiga, fysiologiska och genetiska riskfaktorer för plackbildning och Alzheimers sjukdom.
Se även
Referenser
- ^ a b Cras P; Kawai M; Lowery D; Gonzalez-DeWhitt P; Greenberg B; Perry G (september 1991). "Senilplackneuriter vid Alzheimers sjukdom ackumulerar amyloidprekursorprotein" . Förfaranden vid National Academy of Sciences i USA . 88 (17): 7552–6. Bibcode : 1991PNAS ... 88.7552C . doi : 10.1073/pnas.88.17.7552 . PMC 52339 . PMID 1652752 .
- ^ Purves, Dale; Augustine, George J .; Fitzpatrick, David; Hall, William C .; LaManita, Anthony-Samuel; White, Leonard E .; Mooney, Richard D .; Platt, Michael L. (2012). Neurovetenskap (5: e upplagan). Sunderland, MA: Sinauer Associates. sid. 713. ISBN 978-0-87893-695-3.
- ^ a b c d Dickson DW (1997). "Patogenesen av senila plack" . J Neuropathol Exp Neurol . 56 (4): 321–339. doi : 10.1097/00005072-199704000-00001 . PMID 9100663 .
- ^ a b c d e f g h i j k l m n o Walker LC (2020). "Aβ -plack" . Gratis neuropatologi . 1 (31): 31. doi : 10.17879/freeneuropathology-2020-3025 . PMC 7745791 . PMID 33345256 .
- ^ Ballard, C; Gauthier, S; Corbett, A; Brayne, C; Aarsland, D; Jones, E (19 mars 2011). "Alzheimers sjukdom". Lancet . 377 (9770): 1019–31. doi : 10.1016/S0140-6736 (10) 61349-9 . PMID 21371747 . S2CID 20893019 .
- ^ Hyman BT; West HL; Rebeck GW; Buldyrev SV; Mantegna RN; Ukleja M; Havlin S; Stanley HE (1995). "Kvantitativ analys av senila plack vid Alzheimers sjukdom: observation av log-normal storleksfördelning och molekylär epidemiologi av skillnader associerade med apolipoprotein E-genotyp och trisomi 21 (Downs syndrom)" . Förfaranden vid National Academy of Sciences i USA . 92 (8): 3586–3590. Bibcode : 1995PNAS ... 92.3586H . doi : 10.1073/pnas.92.8.3586 . PMC 42212 . PMID 7724603 .
- ^ a b c Röhr D, Boon BD, et al. (December 2020). "Etikettfri vibrationsavbildning av olika Aβ-placktyper vid Alzheimers sjukdom avslöjar sekventiella händelser vid plackutveckling" . Acta Neuropathologica Communications . 8 (1): 222. doi : 10.1186/s40478-020-01091-5 . PMC 7733282 . PMID 33308303 .
- ^ Haass C; Selkoe DJ (2007). "Lösliga proteinoligomerer i neurodegeneration: lärdomar från Alzheimers amyloid beta-peptid". Nat Rev Mol Cell Biol . 8 (2): 101–112. doi : 10.1038/nrm2101 . PMID 17245412 . S2CID 32991755 .
- ^ Blocq, Paul; Marinesco, Georges (1892). Sur les lesions et la pathogenie de l'epilepsie dite essentielle . s. 445–6. OCLC 492619936 .
- ^ Buda O; Arsene D; Ceausu M; Dermengiu D; Curca GC (januari 2009). "Georges Marinesco och den tidiga forskningen inom neuropatologi". Neurologi . 72 (1): 88–91. doi : 10.1212/01.wnl.0000338626.93425.74 . PMID 19122036 . S2CID 45428057 .
- ^ Redlich E (1898). "Ueber miliare Sklerose der Hirnrinde bei seniler Atrophie". Jahrbücher für Psychiatrie und Neurologie . 17 : 208–216.
- ^ a b c Goedert M (2009). "Oskar Fischer och studiet av demens" . Hjärnan . 132 (4): 1102–1111. doi : 10.1093/brain/awn256 . PMC 2668940 . PMID 18952676 .
- ^ Alzheimer, A (1907). "Uber einen eigenartige Erkranung der Hirnrinde". Allgemeine Zeitschrift für Psychiatrie und Psychisch-Gerichtlich Medizin . 64 : 146–8.
- ^ Divry P (1927). "Etude histo-chimique des plaques séniles". Journal Belge de Neurologie et de Psychiatrie . 9 : 643–657.
- ^ Buxbaum JN; Linke RP (2012). "En molekylär historia av amyloidoserna". Journal of Molecular Biology . 421 (2–3): 142–159. doi : 10.1016/j.jmb.2012.01.024 . PMID 22321796 .
- ^ Simchowicz T .: Histologische Studien über die senile Demenz. i: Nissl F., Alzheimer A. (Hrsg.): Histologische und histopathologische Arbeiten über die Grosshirnrinde mit besonderer Berücksichtigung der pathologischen Anatomie der Geisteskrankheiten . Jena: G. Fischer, 1911, sid. 267–444.
- ^ Ohry A; Buda O (2015). "Teofil Simchowicz (1879-1957): forskaren som myntade senila plack i neuropatologi". Rumänska tidskriften för morfologi och embryologi . 56 (4): 1545–1548. PMID 26743308 .
- ^ Grzybowski A; Pieta A; Pugaczewska M (2017). "Teofil Simchowicz (1879-1957)" . Journal of Neurology . 264 (8): 1831–1832. doi : 10.1007/s00415-017-8460-9 . PMC 5533842 . PMID 28315959 .
- ^ Välsignad G; Tomlinson BE; Roth M (1968). "Sambandet mellan kvantitativa mått på demens och senil förändring i den cerebrala grå substansen hos äldre försökspersoner". British Journal of Psychiatry . 114 (512): 797–811. doi : 10.1192/bjp.114.512.797 . PMID 5662937 .
- ^ Wisniewski, Henryk M .; Terry, Robert D. (1973). "Kapitel 1: Ny undersökning av patogenesen hos den senila placken". I Zimmerman, HM (red.). Progress in Neuropathology, volym 2 . Grune och Stratton. s. 1–26. ISBN 978-0-808-90775-6.
- ^ Glenner GG; Wong CW (1984). "Alzheimers sjukdom: första rapporten om rening och karakterisering av ett nytt cerebrovaskulärt amyloidprotein". Biokemisk och biofysisk forskningskommunikation . 120 (3): 885–890. doi : 10.1016/s0006-291x (84) 80190-4 . PMID 6375662 .
- ^ Glenner GG; Wong CW (1984). "Alzheimers sjukdom och Downs syndrom: delning av ett unikt cerebrovaskulärt amyloidfibrilprotein". Biokemisk och biofysisk forskningskommunikation . 122 (3): 1131–1135. doi : 10.1016/0006-291x (84) 91209-9 . PMID 6236805 .
- ^ Mästare CL; Simms G; Weinman NA; Multhaup G; McDonald BL; Beyreuther K (1985). "Amyloid plack core protein i Alzheimers sjukdom och Downs syndrom" . Proceedings of the National Academy of Sciences USA . 82 (12): 4245–4249. Bibcode : 1985PNAS ... 82.4245M . doi : 10.1073/pnas.82.12.4245 . PMC 397973 . PMID 3159021 .
- ^ a b c Walsh DM; Selkoe DJ (2020). "Amyloid beta-protein och bortom: vägen framåt i Alzheimers sjukdom". Nuvarande åsikt i neurobiologi . 61 : 116–124. doi : 10.1016/j.conb.2020.02.003 . PMID 32197217 . S2CID 214600892 .
- ^ a b c d e f Lång JM; Holtzman DM (2019). "Alzheimers sjukdom: en uppdatering om patobiologi och behandlingsstrategier" . Cell . 179 (2): 312–339. doi : 10.1016/j.cell.2019.09.001 . PMC 6778042 . PMID 31564456 .
- ^ Walker LC (2015). "Proteopatiska stammar och neurodegenerativa sjukdomars heterogenitet" . Årlig granskning av genetik . 50 : 329–346. doi : 10.1146/annurev-genet-120215-034943 . PMC 6690197 . PMID 27893962 .
- ^ Selkoe, DJ (1999). "Kapitel 19: Biologi av β-amyloidprekursorprotein och mekanismen för Alzheimers sjukdom". I Terry, RD; Katzman, R; Bick, KL; Sisodia, SS (red.). Alzheimers sjukdom . Lippincott Williams och Wilkins. s. 293–310. ISBN 0-7817-1503-2.
- ^ a b c Haass C; Kaether C; Thinakaran G; Sisodia S (2012). "Trafficking och proteolytisk bearbetning av APP" . Cold Spring Harbour Perspectives in Medicine . 2 (5: a006270): a006270. doi : 10.1101/cshperspect.a006270 . PMC 3331683 . PMID 22553493 .
- ^ Suh YH; Checler F (september 2002). "Amyloidprekursorprotein, preseniliner och alfa-synuklein: molekylär patogenes och farmakologiska tillämpningar vid Alzheimers sjukdom". Farmakologiska recensioner . 54 (3): 469–525. doi : 10.1124/pr.54.3.469 . PMID 12223532 . S2CID 86686003 .
- ^ Dunys J; Valverde A; Checler F (2018). "Är N- och C-terminalt trunkerade Aβ-arter viktiga patologiska utlösare vid Alzheimers sjukdom?" . Journal of Biological Chemistry . 293 (40): 15419–15428. doi : 10.1074/jbc.R118.003999 . PMC 6177599 . PMID 30143530 .
- ^ Kummer MP; Heneka MT (2014). "Avkortad och modifierad amyloid-beta-art" . Alzheimers forskning och terapi . 6 (3): 28. doi : 10.1186/alzrt258 . PMC 4055046 . PMID 25031638 .
- ^ Lamy C, Duyckaerts C, Delaere P, et al. (1989). "Jämförelse av sju färgningsmetoder för senila plack och neurofibrillära trassel i en potentiell serie om 15 äldre patienter". Neuropatologi och tillämpad neurobiologi . 15 (6): 563–78. doi : 10.1111/j.1365-2990.1989.tb01255.x . PMID 2482455 . S2CID 25220224 .
- ^ Klingstedt T; Nilsson KPR (2012). "Luminescerande konjugerade poly- och oligo-tiofener: optiska ligander för spektral tilldelning av en uppsjö av proteinaggregat". Biokemiska samhällstransaktioner . 40 (4): 704–710. doi : 10.1042/BST20120009 . PMID 22817720 .
- ^ Mavrogiorgou P; Gertz HJ; Ferszt R; Wolf R; Bär KJ; Juckel G (december 2011). "Är rutinmetoder tillräckligt bra för att fläcka senila plack och neurofibrillära trassel i olika hjärnregioner hos dementa patienter?" (PDF) . Psychiatria Danubina . 23 (4): 334–9. PMID 22075733 . Arkiverad från originalet (PDF) 2017-08-11 . Hämtad 2014-06-22 .
- ^ Braak H; Thal DR; Ghebremedhin E; Del Tredici K (2011). "Stadier av den patologiska processen vid Alzheimers sjukdom: ålderskategorier från 1 till 100 år" . Journal of Neuropathology and Experimental Neurology . 70 (11): 960–969. doi : 10.1097/NEN.0b013e318232a379 . PMID 22002422 .
- ^ Thal DR; Rüb O; Orantes M; Braak H (2002). "Faser av Abeta-deponering i den mänskliga hjärnan och dess relevans för utvecklingen av AD". Neurologi . 58 (12): 1791–1800. doi : 10.1212/wnl.58.12.1791 . PMID 12084879 . S2CID 41133337 .
- ^ Thal DR; Walter J; Saido TC; Fändrich M (2015). "Neuropatologi och biokemi av Aβ och dess aggregat vid Alzheimers sjukdom" . Acta Neuropathologica . 129 (2): 167–182. doi : 10.1007/s00401-014-1375-y . PMID 25534025 . S2CID 19701015 .
- ^ a b Jucker, M; Walker, LC (2013). "Självförökning av patogena proteinaggregat vid neurodegenerativa sjukdomar" . Natur . 501 (7465): 45–51. Bibcode : 2013Natur.501 ... 45J . doi : 10.1038/nature12481 . PMC 3963807 . PMID 24005412 .
- ^ Walker LC; Jucker M (2015). "Neurodegenerativa sjukdomar: Utöka prionkonceptet" . Årlig granskning av neurovetenskap . 38 : 87–103. doi : 10.1146/annurev-neuro-071714-033828 . PMC 4803040 . PMID 25840008 .
- ^ Prusiner SB (1998). "Prioner" . Proceedings of the National Academy of Sciences USA . 95 (23): 13363–13383. Bibcode : 1998PNAS ... 9513363P . doi : 10.1073/pnas.95.23.13363 . PMC 33918 . PMID 9811807 .
- ^ Eisenberg D; Jucker M (2015). "Amyloidtillståndet för proteiner vid mänskliga sjukdomar" . Cell . 148 (6): 1188–1203. doi : 10.1016/j.cell.2012.02.022 . PMC 3353745 . PMID 22424229 .
- ^ Nelson PT, Alafuzoff I, Bigio EH, et al. (2012). "Korrelation av Alzheimers sjukdom neuropatologiska förändringar med kognitiv status: en genomgång av litteraturen" . Journal of Neuropathology and Experimental Neurology . 71 (5): 362–381. doi : 10.1097/NEN.0b013e31825018f7 . PMC 3560290 . PMID 22487856 .
- ^ a b Findeis MA (november 2007). "Rollen av amyloid beta -peptid 42 vid Alzheimers sjukdom". Farmakologi och terapi . 116 (2): 266–86. doi : 10.1016/j.pharmthera.2007.06.006 . PMID 17716740 .
- ^ Thal DR, Ronisz A, Tousseyn T, et al. (2019). "Olika aspekter av Alzheimers sjukdom-relaterade amyloid β-peptidpatologi och deras relation till amyloid positronemissionstomografi och demens" . Acta Neuropathologica Communications . 7 (1): 178. doi : 10.1186/s40478-019-0837-9 . PMC 6854805 . PMID 31727169 .
- ^ Mathis CA; Lopresti BJ; Ikonomovic MD; Klunk WE (2017). "PET-spårare med små molekyler för avbildning av proteinopatier" . Seminarier i kärnmedicin . 47 (5): 553–575. doi : 10.1053/j.semnuclmed.2017.06.003 . PMC 5657567 . PMID 28826526 .
- ^ Ritchie C; Smailagic N; Noel-Storr AH; Ukoumunne O; Ladds EC; Martin S (2017). "CSF tau och CSF tau/ABeta -förhållandet för diagnos av Alzheimers sjukdom demens och andra demens hos personer med lätt kognitiv funktionsnedsättning (MCI)" . Cochrane Database of Systematic Reviews . 3 (3): CD010803. doi : 10.1002/14651858.CD010803.pub2 . PMC 6464349 . PMID 28328043 .
- ^ Hansson O; Lehmann S; Otto M; Zetterberg H; Lewczuk P (2019). "Fördelar och nackdelar med användningen av CSF Amyloid beta (Abeta) 42/40 -förhållandet vid diagnos av Alzheimers sjukdom" . Alzheimers forskning och terapi . 11 (1): 34. doi : 10.1186/s13195-019-0485-0 . PMC 6477717 . PMID 31010420 .
- ^ a b Stam FC; Wigboldus JM; Smeulders AW (1986). "Åldersincidens av senil hjärnamyloidos" (PDF) . Patologi - forskning och praktik . 181 (5): 558–562. doi : 10.1016/S0344-0338 (86) 80149-2 . PMID 3786248 .
- ^ Franke, M (1976). "Statistische Untersuchungen über die senilen Drusen im menschlichen Gehirn / Thesen" . Berlin, Tyskland: Neuropathologische Abteilung. Arkiverad från originalet 2011-07-19.
- ^ a b Huvud E; Powell D; Guld BT; Schmitt FA (2012). "Alzheimers sjukdom i Downs syndrom" . European Journal of Neurodegenerative Disease . 1 (3): 353–364. PMC 4184282 . PMID 25285303 .
- ^ Heuer E; Rosen RF; Cintron A; Walker LC (2012). "Omänskliga primatmodeller av Alzheimer-liknande cerebral proteopati" . Nuvarande läkemedelsdesign . 18 (8): 1159–1169. doi : 10.2174/138161212799315885 . PMC 3381739 . PMID 22288403 .
- ^ Walker LC; Jucker M (2017). "Människors exceptionella sårbarhet för Alzheimers sjukdom" . Trender inom molekylär medicin . 23 (6): 534–545. doi : 10.1016/j.molmed.2017.04.001 . PMC 5521004 . PMID 28483344 .
- ^ Jucker M (2010). "Fördelar och begränsningar av djurmodeller för translationell forskning i neurodegenerativa sjukdomar". Naturmedicin . 16 (11): 1210–1214. doi : 10.1038/nm.2224 . PMID 21052075 . S2CID 30167302 .
- ^ Myers A; McGonigle P (2010). "Översikt över transgena musmodeller för Alzheimers sjukdom". Nuvarande protokoll inom neurovetenskap . 89 (1: e81): 1210–1214. doi : 10.1002/cpns.81 . PMID 31532917 . S2CID 202024310 .
- ^ Huang Y, Happonen KE (april 2021). "Microglia använder TAM -receptorer för att detektera och uppsluka amyloid β -plack" . Naturimmunologi . 8 (1): 222. doi : 10.1186/s40478-020-01091-5 . PMC 7733282 . PMID 33308303 .
- ^ Heppner FL; Ransohoff RM; Becher B (2015). "Immunattack: inflammationens roll vid Alzheimers sjukdom". Naturrecensioner Neurovetenskap . 16 (6): 358–372. doi : 10.1038/nrn3880 . PMID 25991443 . S2CID 6116253 .
- ^ De Strooper B; Karran E (2016). "Cellfasen av Alzheimers sjukdom" . Cell . 164 (4): 603–615. doi : 10.1016/j.cell.2015.12.056 . PMID 26871627 .
- ^ Killin LOJ; Starr JM; Shiue IJ; Russ TC (2016). "Miljöriskfaktorer för demens: en systematisk översyn" . BMC Geriatrics . 16 (1): 175. doi : 10.1186/s12877-016-0342-y . PMC 5059894 . PMID 27729011 .
Vidare läsning
- Jellinger KA (2005). "Neurodegenerative Erkrankungen (ZNS) - Eine aktuelle Übersicht" (PDF) . Journal für Neurologie, Neurochirurgie und Psychiatrie . 6 (1): 9–18.
- Cruz L, Urbanc B, Buldyrev SV, et al. (Juli 1997). "Aggregering och uppdelning av senila plack vid Alzheimers sjukdom" . Förfaranden vid National Academy of Sciences i USA . 94 (14): 7612–6. Bibcode : 1997PNAS ... 94.7612C . doi : 10.1073/pnas.94.14.7612 . PMC 23870 . PMID 9207140 .