Poliovaccin -Polio vaccine
 | |
| Vaccinbeskrivning | |
|---|---|
| Mål | Polio |
| Vaccin typ | IPV: inaktiverad OPV: dämpad |
| Kliniska data | |
| Handelsnamn | Ipol, Poliovax, andra |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a601177 |
| Licensdata | |
| Graviditetskategori _ |
|
| Administreringsvägar _ |
IPV: parenteral OPV: oral |
| ATC-kod | |
| Rättslig status | |
| Rättslig status | |
| Identifierare | |
| CAS-nummer | |
| DrugBank | |
| ChemSpider | |
|
| |
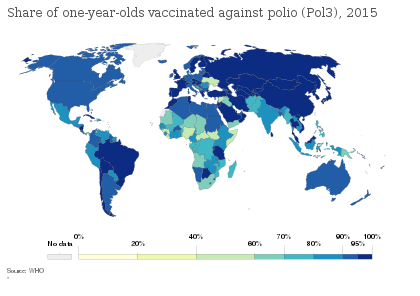
Poliovaccin är vacciner som används för att förebygga poliomyelit (polio). Två typer används: ett inaktiverat poliovirus som ges genom injektion (IPV) och ett försvagat poliovirus som ges via munnen (OPV). Världshälsoorganisationen ( WHO ) rekommenderar alla barn att vaccineras helt mot polio. De två vaccinerna har eliminerat polio från större delen av världen och minskat antalet fall som rapporteras varje år från uppskattningsvis 350 000 1988 till 33 år 2018.
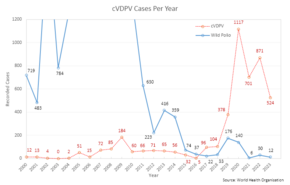
De inaktiverade poliovaccinerna är mycket säkra. Mild rodnad eller smärta kan förekomma på injektionsstället. Orala poliovacciner orsakar cirka tre fall av vaccinassocierad paralytisk poliomyelit per miljon ges. Det kan jämföras med 5 000 fall per miljon som är förlamade efter en polioinfektion. Båda typerna av vaccin är i allmänhet säkra att ge under graviditet och hos dem som har hiv/aids men i övrigt mår bra. Emellertid har uppkomsten av cirkulerande vaccinhärlett poliovirus (cVDPV), en form av vaccinviruset som har återgått till att orsaka poliomyelit, lett till utvecklingen av ett nytt oralt poliovaccin typ 2 (nOPV2) som syftar till att göra vaccinet säkrare och därmed stoppa ytterligare utbrott av cVDPV2.
Den första framgångsrika demonstrationen av ett poliovaccin var av Hilary Koprowski 1950, med ett levande försvagat virus som människor drack. Vaccinet godkändes inte för användning i USA, men användes framgångsrikt på andra håll. Framgången för ett inaktiverat (dödat) poliovaccin, utvecklat av Jonas Salk , tillkännagavs 1955 . Ett annat försvagat levande oralt poliovaccin utvecklades av Albert Sabin och kom i kommersiell användning 1961.
Poliovaccin finns på Världshälsoorganisationens lista över nödvändiga läkemedel .
Medicinsk användning
Avbrott av person-till-person-överföring av viruset genom vaccination är viktigt vid global polio-utrotning , eftersom det inte finns något långvarigt bärartillstånd för poliovirus hos individer med normal immunfunktion, poliovirus har ingen icke-primatreservoar i naturen, och överlevnad av viruset i miljön under en längre tidsperiod verkar vara avlägsen. Det finns två typer av vaccin: inaktiverat poliovaccin (IPV) och oralt poliovaccin (OPV).
Inaktiverad
När IPV (injektion) används utvecklar 90 % eller fler av individerna skyddande antikroppar mot alla tre serotyper av poliovirus efter två doser av inaktiverat poliovaccin (IPV), och minst 99 % är immuna mot poliovirus efter tre doser. Varaktigheten av immunitet inducerad av IPV är inte känd med säkerhet, även om en komplett serie tros ge skydd i många år. IPV ersatte det orala vaccinet i många utvecklade länder på 1990-talet, främst på grund av den (lilla) risken för vaccinhärledd polio i det orala vaccinet.
Dämpad
Orala poliovacciner var lättare att administrera än IPV, eftersom det eliminerade behovet av sterila sprutor och därför var mer lämpligt för massvaccinationskampanjer. OPV gav också mer långvarig immunitet än Salk-vaccinet, eftersom det ger både humoral immunitet och cellmedierad immunitet .
En dos OPV ger immunitet mot alla tre poliovirusserotyperna hos ungefär 50 % av mottagarna. Tre doser av levande försvagad OPV producerar skyddande antikroppar mot alla tre typer av poliovirus hos mer än 95 % av mottagarna. OPV producerar utmärkt immunitet i tarmen , den primära platsen för vilda poliovirus, vilket hjälper till att förhindra infektion med vilda virus i områden där viruset är endemiskt . Det levande viruset som används i vaccinet kan sällan spridas i avföringen och kan sällan spridas till andra inom ett samhälle. Det levande viruset har också stränga krav på transport och lagring, vilket är ett problem i vissa varma eller avlägsna områden. Som med andra levande virusvacciner är immunitet initierad av OPV troligen livslång.
Den trivalenta (mot vildtyperna 1, 2 och 3) OPV har använts för att nästan utrota polioinfektion över hela världen. Under ledning av Global Polio Eradication Initiative gick 155 länder över till att använda den bivalenta (mot vildtyp 1 och 3) mellan 17 april och 1 maj 2016. Den bivalenta OPV är effektivare mot typ 1 och 3, men täcker inte typ 2. Från och med 2017 fortsätter USA att rekommendera användningen av en trivalent version, men en helt inaktiverad version. Bytet till det bivalenta vaccinet och tillhörande saknad immunitet mot typ 2-stammar ledde bland annat till utbrott av cirkulerande vaccinhärrörande poliovirus typ 2(cVDPV2), som ökade från 2 fall 2016 till 1037 fall 2020. Som ett svar , utvecklades ett nytt oralt poliovaccin typ 2 (nOPV2) med syftet att tillhandahålla en säkrare form av vaccination mot typ 2-stammar med mindre risk att återgå till infektiös polio.
Schema
I länder med endemisk polio eller där risken för importerade fall är hög rekommenderar WHO OPV-vaccin vid födseln följt av en primärserie om tre OPV-doser och minst en IPV-dos som börjar vid 6 veckors ålder, med minst 4 veckor mellan OPV-doser. I länder med >90 % immuniseringstäckning och låg risk för import rekommenderar WHO en eller två IPV-doser som börjar vid 2 månaders ålder följt av minst två OPV-doser, med doserna åtskilda med 4–8 veckor beroende på risken för exponering. I länder med de högsta nivåerna av täckning och de lägsta riskerna för import och överföring rekommenderar WHO en primär serie med tre IPV-injektioner, med en boosterdos efter ett intervall på sex månader eller mer om den första dosen administrerades före 2 månader av ålder.
Bieffekter
De inaktiverade poliovaccinerna är mycket säkra. Mild rodnad eller smärta kan förekomma på injektionsstället. Oralt poliovaccin resulterar i vaccinassocierad paralytisk poliomyelit i cirka tre per miljon doser. De är i allmänhet säkra att ge till de som är gravida och de som har hiv/aids , men som annars mår bra.
Allergisk reaktion på vaccinet
Inaktiverat poliovaccin kan orsaka en allergisk reaktion hos ett fåtal personer eftersom vaccinet innehåller spårmängder av antibiotika, streptomycin, polymyxin B och neomycin. Det ska inte ges till någon som har en allergisk reaktion mot dessa läkemedel. Tecken och symtom på en allergisk reaktion, som vanligtvis uppträder inom några minuter eller några timmar efter att ha fått det injicerade vaccinet, inkluderar andningssvårigheter, svaghet, heshet eller väsande andning, hjärtfrekvensfluktuationer, hudutslag och yrsel.
Vaccininducerad polio
En potentiell, negativ effekt av OPV är dess kända förmåga att rekombinera till en form som orsakar neurologisk infektion och förlamning. Denna genetiska vändning av patogenen till en virulent form tar avsevärd tid (minst 12 månader) och påverkar inte den person som ursprungligen vaccinerades. Det vaccinhärledda försvagade viruset utsöndras normalt från vaccinerade personer under en begränsad period. I områden med dålig sanitet och låg vaccinationstäckning kan således den spontana återgången av det vaccinhärledda viruset till en virulent form och dess spridning i miljön leda till att ovaccinerade människor blir smittade. Klinisk sjukdom, inklusive förlamning, orsakad av vaccin-derived poliovirus (VDPV) kan inte skiljas från den som orsakas av vilda poliovirus. Utbrott av vaccinassocierad paralytisk poliomyelit (VAPP), orsakade av ett cirkulerande vaccinhärlett poliovirus (cVDPV), har rapporterats och tenderar att inträffa i områden med låg täckning av OPV, förmodligen för att OPV i sig själv skyddar mot det relaterade utbrottet anstränga. Med vilda poliofall på rekordlåga nivåer var 2017 det första året där fler fall av cVDPV registrerades än det vilda polioviruset, en trend som förväntas fortsätta.
För att bekämpa detta beslutade WHO 2016 att byta från det trivalenta poliovaccinet till det bivalenta poliovaccinet. Detta vaccin innehåller inte längre poliovirus typ 2 eftersom det utrotades 1999.
Föroreningsproblem
År 1960 fastställdes att rhesusapens njurceller som användes för att förbereda poliovirusvaccinerna var infekterade med simianvirus-40 (SV40), som också upptäcktes 1960 och är ett naturligt förekommande virus som infekterar apor. 1961 visade sig SV40 orsaka tumörer hos gnagare . På senare tid har viruset hittats i vissa former av cancer hos människor, till exempel hjärn- och skelettumörer , pleuralt och peritonealt mesoteliom och vissa typer av non-Hodgkin-lymfom . SV40 har dock inte fastställts för att orsaka dessa cancerformer.
SV40 visade sig finnas i lager av den injicerade formen av IPV som användes mellan 1955 och 1963. Det finns inte i OPV-formen. Över 98 miljoner amerikaner fick en eller flera doser poliovaccin mellan 1955 och 1963 när en del av vaccinet var kontaminerat med SV40; uppskattningsvis 10–30 miljoner amerikaner kan ha fått en dos vaccin kontaminerat med SV40. Senare analyser tydde på att vacciner som producerats av de före detta sovjetblocksländerna fram till 1980 och användes i Sovjetunionen , Kina , Japan och flera afrikanska länder kan ha blivit kontaminerade, vilket betyder att hundratals miljoner fler kan ha exponerats för SV40.
1998 genomförde National Cancer Institute en stor studie med cancerfallsinformation från institutets SEER-databas. De publicerade resultaten från studien visade ingen ökad förekomst av cancer hos personer som kan ha fått vaccin innehållande SV40. En annan stor studie i Sverige undersökte cancerfrekvensen hos 700 000 individer som hade fått potentiellt kontaminerat poliovaccin så sent som 1957; studien visade återigen ingen ökad cancerincidens mellan personer som fick poliovaccin innehållande SV40 och de som inte gjorde det. Frågan om SV40 orsakar cancer hos människor förblir dock kontroversiell, och utvecklingen av förbättrade analyser för detektion av SV40 i mänskliga vävnader kommer att behövas för att lösa kontroversen.

Under kapplöpningen för att utveckla ett oralt poliovaccin genomfördes flera storskaliga försök på människor. År 1958 hade National Institutes of Health bestämt att OPV producerad med Sabin-stammarna var de säkraste. Mellan 1957 och 1960 fortsatte dock Hilary Koprowski att administrera sitt vaccin runt om i världen. I Afrika administrerades vaccinerna till ungefär en miljon människor i de belgiska territorierna (nu Demokratiska republiken Kongo , Rwanda och Burundi ). Resultaten av dessa mänskliga prövningar har varit kontroversiella och ogrundade anklagelser på 1990-talet uppstod om att vaccinet hade skapat de förutsättningar som var nödvändiga för överföring av apimmunbristvirus från schimpanser till människor, vilket orsakade HIV/AIDS . Dessa hypoteser har dock slutgiltigt tillbakavisats . År 2004 hade fall av poliomyelit i Afrika reducerats till bara ett litet antal isolerade regioner i den västra delen av kontinenten, med sporadiska fall på andra håll. Den senaste tidens lokala motstånd mot vaccinationskampanjer har utvecklats på grund av brist på adekvat information, ofta relaterat till rädsla för att vaccinet kan framkalla sterilitet . Sjukdomen har sedan dess återuppstått i Nigeria och i flera andra afrikanska länder utan nödvändig information, vilket epidemiologer tror beror på att vissa lokalbefolkningar vägrat att låta deras barn få poliovaccinet.
Tillverkning
Inaktiverad
Salk-vaccinet, IPV, är baserat på tre vilda, virulenta referensstammar, Mahoney (typ 1 poliovirus), MEF-1 (typ 2 poliovirus) och Saukett (typ 3 poliovirus), odlade i en typ av njurvävnadskultur av apor ( Vero-cellinje ), som sedan inaktiveras med formalin . Det injicerade Salk-vaccinet ger IgG -medierad immunitet i blodomloppet, vilket förhindrar polioinfektion från att utvecklas till viremi och skyddar motorneuronerna , vilket eliminerar risken för bulbar polio och postpoliosyndrom .
I USA administreras vaccin tillsammans med tetanus- , difteri- och acellulär pertussis -vaccin ( DTaP ) och en pediatrisk dos av hepatit B- vaccin. I Storbritannien kombineras IPV med stelkramps-, difteri-, pertussis- och Haemophilus influenzae typ b-vaccin.
Dämpad

OPV är ett försvagat vaccin som produceras genom att viruset passerar genom icke-mänskliga celler vid en subfysiologisk temperatur , vilket producerar spontana mutationer i det virala genomet. Orala poliovaccin utvecklades av flera grupper, varav en leddes av Albert Sabin . Andra grupper, ledda av Hilary Koprowski och HR Cox , utvecklade sina egna försvagade vaccinstammar. År 1958 skapade National Institutes of Health en särskild kommitté för levande poliovacciner. De olika vaccinerna utvärderades noggrant med avseende på deras förmåga att inducera immunitet mot polio, samtidigt som de bibehöll en låg förekomst av neuropatogenicitet hos apor. Storskaliga kliniska prövningar utförda i Sovjetunionen i slutet av 1950-talet till början av 1960-talet av Mikhail Chumakov och hans kollegor visade säkerhet och hög effektivitet av vaccinet. Baserat på dessa resultat valdes Sabin-stammarna för världsomspännande distribution. Femtiosju nukleotidsubstitutioner skiljer den försvagade Sabin 1-stammen från dess virulenta förälder (Mahoney-serotypen), två nukleotidsubstitutioner försvagar Sabin 2-stammen och 10 substitutioner är involverade i attenuera Sabin 3-stammen. Den primära försvagande faktorn som är gemensam för alla tre Sabin-vaccinerna är en mutation belägen i virusets inre ribosominträdesställe, som förändrar stam-loop -strukturer och minskar förmågan hos poliovirus att översätta sin RNA-mall i värdcellen. Det försvagade polioviruset i Sabin-vaccinet replikerar mycket effektivt i tarmen, det primära stället för infektion och replikation, men kan inte replikera effektivt i nervsystemets vävnad. År 1961 licensierades typ 1 och 2 monovalent oralt poliovirusvaccin (MOPV) och 1962 licenserades typ 3 MOPV. 1963 licensierades trivalent OPV (TOPV) och blev det valda vaccinet i USA och de flesta andra länder i världen, och ersatte till stor del det inaktiverade poliovaccinet. En andra våg av massvaccinationer ledde till en ytterligare dramatisk minskning av antalet poliofall. Mellan 1962 och 1965 fick cirka 100 miljoner amerikaner (ungefär 56% av befolkningen vid den tiden) Sabin-vaccinet. Resultatet var en avsevärd minskning av antalet poliomyelitfall, även från de mycket sänkta nivåerna efter införandet av Salk-vaccinet.
OPV tillhandahålls vanligtvis i injektionsflaskor som innehåller 10–20 doser vaccin. En enkel dos av oralt poliovaccin (vanligtvis två droppar) innehåller 1 000 000 smittsamma enheter av Sabin 1 (effektiv mot PV1), 100 000 smittsamma enheter av Sabin 2-stammen och 600 000 smittsamma enheter av Sabin 3. Vaccinet innehåller små spår av antibiotika . neomycin och streptomycin - men innehåller inga konserveringsmedel .
Historia
I en generisk mening fungerar vaccination genom att primera immunsystemet med ett " immunogen ". Stimulering av immunsvar, genom användning av ett smittämne, är känt som immunisering . Utvecklingen av immunitet mot polio blockerar effektivt person-till-person överföring av vilda poliovirus, och skyddar därigenom både enskilda vaccinmottagare och samhället i stort .
Utvecklingen av två poliovacciner ledde till de första moderna massymmpningarna . De sista fallen av paralytisk poliomyelit orsakad av endemisk överföring av vilda virus i USA inträffade 1979, med ett utbrott bland Amish i flera delstater i Mellanvästern .
1930-talet
På 1930-talet upplevdes poliovirus som särskilt skrämmande, eftersom man inte visste hur sjukdomen överfördes eller hur den kunde förebyggas. Detta virus var också anmärkningsvärt för att främst påverka välbärgade barn, vilket gör det till ett främsta mål för vaccinutveckling, trots dess relativt låga dödlighet och sjuklighet. Trots detta har gruppen av forskare på området hittills i stort sett observerat ett informellt moratorium för utveckling av vaccin eftersom det ansågs utgöra en för hög risk för för liten sannolikhet för framgång.
Detta förändrades i början av 1930-talet när amerikanska grupper antog utmaningen: Maurice Brodie ledde ett team från folkhälsolaboratoriet i staden New York och Dr. John A. Kolmer samarbetade med Research Institute of Cutaneous Medicine i Philadelphia. Rivaliteten mellan dessa två forskare gav en rasliknande mentalitet som, i kombination med bristande tillsyn av medicinska studier, återspeglades i metodiken och resultaten av var och en av dessa tidiga vaccinutvecklingssatsningar.
Kolmers levande vaccin
Kolmer började sitt vaccinutvecklingsprojekt 1932 och fokuserade slutligen på att producera ett försvagat eller levande virusvaccin . Inspirerad av framgången med vacciner mot rabies och gula febern hoppades han kunna använda en liknande process för att denaturera polioviruset. För att kunna dämpa sitt poliovaccin förde han upprepade gånger viruset genom apor. Med hjälp av produktionsmetoder som senare beskrevs som "hårresande amatörmässigt, den terapeutiska motsvarigheten till badkarsgin", malde Kolmer ryggmärgen på sina infekterade apor och blötlade dem i en saltlösning. Han filtrerade sedan lösningen genom nät, behandlade den med ricinolat och kylde produkten i 14 dagar för att slutligen skapa vad som senare skulle bli en framträdande kritik som en "veritabel häxbrygd".
I enlighet med tidens normer genomförde Kolmer ett relativt litet djurförsök med 42 apor innan han fortsatte med självexperiment 1934. Han testade sitt vaccin på sig själv, sina två barn och sin assistent. Han gav sitt vaccin till bara 23 fler barn innan han förklarade det säkert och skickade det till läkare och hälsoavdelningar för ett större test av effektivitet. I april 1935 kunde han rapportera att han testat vaccinet på 100 barn utan negativ effekt. Kolmers första formella presentation av resultat skulle inte komma till stånd förrän i november 1935 där han presenterade resultaten av 446 barn och vuxna som han hade vaccinerat med sitt försvagade vaccin. Han rapporterade också att Research Institute of Cutaneous Medicine och Merrell Company of Cincinnati (tillverkaren som innehade patentet för sin ricinoleeringsprocess) tillsammans hade distribuerat 12 000 doser vaccin till cirka 700 läkare över hela USA och Kanada. Kolmer beskrev ingen övervakning av detta experimentella vaccinationsprogram och gav inte heller dessa läkare instruktioner om hur man administrerar vaccinet eller hur man rapporterar biverkningar. Kolmer ägnade huvuddelen av sina publikationer därefter till att förklara vad han trodde var orsaken till de 10+ rapporterade fallen av paralytisk polio efter vaccination, i många fall i städer där inget polioutbrott hade inträffat. Sex av dessa fall hade varit dödliga. Kolmer hade ingen kontrollgrupp men hävdade att många fler barn skulle ha blivit sjuka.
Brodies inaktiverade vaccin
Nästan samtidigt som Kolmers projekt hade Maurice Brodie anslutit sig till immunologen Dr William H. Park vid New York City Health Department där de arbetade tillsammans med poliovirus. Med hjälp av bidragsfinansiering från presidentens födelsedagsbollskommission (en föregångare till vad som skulle bli March of Dimes ) kunde Brodie fortsätta utvecklingen av ett inaktiverat eller "dödat virus"-vaccin. Brodies process började också med att slipa ryggmärgen på infektiösa apor och sedan behandla sladdarna med olika bakteriedödande medel, vilket till slut hittade en lösning av formaldehyd som var den mest effektiva. Den 1 juni 1934 kunde Brodie publicera sin första vetenskapliga artikel som beskrev hans framgångsrika induktion av immunitet hos tre apor med inaktiverat poliovirus. Genom fortsatta studier på ytterligare 26 apor drog Brodie slutsatsen slutsatsen att administrering av levande virusvaccin tenderade att resultera i humoral immunitet medan administrering av dödat virusvaccin tenderade att resultera i vävnadsimmunitet .
Strax efter, efter ett liknande protokoll som Kolmer, fortsatte Brodie med självexperimentering på sig själv och sina medarbetare vid NYC Health Departments laboratorium. Brodies framsteg täcktes ivrigt av populärpressen när allmänheten hoppades på att ett framgångsrikt vaccin skulle bli tillgängligt. Sådan rapportering nämnde inte de 12 barn på ett asyl i New York City som utsattes för tidiga säkerhetsprövningar. Eftersom ingen av försökspersonerna upplevde negativa effekter, förklarade Dr. Park, som av samtida beskrevs som "aldrig en som låter gräs växa under hans fötter", att vaccinet är säkert. När ett allvarligt polioutbrott överväldigade Kern County, Kalifornien , blev det den första testplatsen för det nya vaccinet med mycket kort varsel. Mellan november 1934 - maj 1935 administrerades över 1 500 doser av vaccinet i Kern County. De första resultaten var mycket lovande, men otillräcklig personal och dålig protokolldesign lämnade Brodie öppen för kritik när han publicerade Kaliforniens resultat i augusti 1935. Genom privatläkare genomförde Brodie också en bredare fältstudie, inklusive 9 000 barn som fick vaccinet och 4 500 års ålder. - och platsmatchade kontroller som inte fått något vaccin. Återigen var resultaten lovande. Av dem som fick vaccinet var det bara ett fåtal som utvecklade polio. De flesta hade exponerats före vaccination och ingen hade fått hela serien av vaccindoser som studerades. Dessutom gav en polioepidemi i Raleigh , North Carolina en möjlighet för US Public Health Service att genomföra en mycket strukturerad prövning av Brodie-vaccinet med finansiering från Birthday Ball Commission.
Akademiskt mottagande
Medan deras arbete pågick började den större gruppen av bakteriologer att väcka oro angående säkerheten och effekten av de nya poliovirusvaccinerna. Vid denna tidpunkt fanns det mycket lite tillsyn av medicinska studier, och etisk behandling av studiedeltagare förlitade sig till stor del på moraliskt tryck från akademiska vetenskapsmän. Brodies inaktiverade vacciner fick granskas av många som ansåg att dödade virusvacciner inte kunde vara effektiva. Medan forskare kunde replikera den vävnadsimmunitet han hade producerat i sina djurförsök, var rådande visdom att humoral immunitet var avgörande för ett effektivt vaccin. Kolmer ifrågasatte direkt metoden med dödade virus i vetenskapliga tidskrifter. Kolmers studier hade dock väckt ännu mer oro med ökande rapporter om barn som blivit förlamade efter vaccination med hans levande virusvaccin och framför allt med förlamning som börjar vid armen snarare än foten i många fall. Både Kolmer och Brodie kallades att presentera sin forskning vid American Public Health Associations årliga möte i Milwaukee WI i oktober 1935. Dr. Thomas M. Rivers ombads dessutom att diskutera var och en av de presenterade artiklarna som en framstående kritiker av vaccinutvecklingsinsatser. Detta resulterade i att APHA arrangerade ett symposium om polomyelit som skulle hållas vid årsmötet för deras södra gren följande månad. Det var under diskussionen vid detta möte som Dr. James Leake från US Public Health Service stod för att omedelbart presentera kliniska bevis för att Kolmer-vaccinet hade orsakat flera dödsfall och sedan anklagade Kolmer för att vara en mördare. Som Rivers påminde om i sin muntliga historia, "helvetet bröt lös, och det verkade som om alla försökte prata samtidigt...Jimmy Leake använde det starkaste språk jag någonsin har hört användas vid ett vetenskapligt möte." Som svar på attackerna från alla håll rapporterades Brodie ha stått upp och sagt, "Det ser ut som om, enligt Dr Rivers, mitt vaccin inte är bra, och enligt Dr Leake är Dr Kolmers farligt. " Kolmer svarade helt enkelt genom att säga: "Mine herrar, det här är en gång jag önskar att golvet skulle öppna sig och svälja mig." I slutändan visades Kolmers levande vaccin utan tvekan vara farligt och hade redan dragits tillbaka i september 1935 före mötet i Milwaukee. Medan samförståndet från symposiet till stor del var skeptiskt till effekten av Brodies vaccin, var dess säkerhet inte ifrågasatt och rekommendationen var en mycket större välkontrollerad studie. Men när tre barn blev sjuka i paralytisk polio efter en dos av vaccinet, begärde direktörerna för Warm Springs Foundation i Georgia (som agerar som de primära finansiärerna för projektet) att det skulle dras tillbaka i december 1935. Det observerade moratoriet för utveckling av humant poliomyelitvaccin återupptogs och det skulle inte bli ett nytt försök på nästan 20 år.
Medan Brodie utan tvekan hade gjort störst framsteg i jakten på ett poliovirusvaccin, drabbades han av de mest betydande karriärreaktionerna på grund av sin status som en mindre känd forskare. Moderna forskare inser att Brodie mycket väl kan ha utvecklat ett effektivt poliovaccin, men dåtidens grundläggande vetenskap och teknik var otillräcklig för att förstå och använda detta genombrott. Brodies arbete med att använda formalin-inaktiverat virus skulle senare bli grunden för Salk-vaccinet, men han skulle inte leva för att se denna framgång. Brodie fick sparken från sin tjänst inom tre månader efter att symposiet publicerats. Samtidigt som han kunde hitta en annan laboratorieposition dog han av en hjärtattack bara tre år senare vid 36 års ålder. Däremot kunde Park, som i samhället ansågs nå senilitet vid denna tidpunkt i sin äldre ålder, att avgå från sin position med utmärkelser före sin död 1939. Kolmer, redan en etablerad och väl respekterad forskare, återvände till Temple University som professor i medicin. Kolmer hade en mycket produktiv karriär, fick flera utmärkelser och publicerade otaliga tidningar, artiklar och läroböcker fram till sin pensionering 1957.
1948
Ett genombrott kom 1948 när en forskargrupp ledd av John Enders vid Children's Hospital Boston framgångsrikt odlade polioviruset i mänsklig vävnad i laboratoriet. Denna grupp hade nyligen framgångsrikt odlat påssjuka i cellkultur . I mars 1948 försökte Thomas H. Weller odla varicellavirus i embryonal lungvävnad. Han hade inokulerat det planerade antalet rör när han märkte att det fanns några oanvända rör. Han hämtade ett prov av mushjärna infekterad med poliovirus och lade till det i de återstående provrören, med risken att viruset kunde växa. Varicellakulturerna lyckades inte växa , men poliokulturerna var framgångsrika. Denna utveckling underlättade i hög grad vaccinforskningen och möjliggjorde i slutändan utvecklingen av vacciner mot polio. Enders och hans kollegor, Thomas H. Weller och Frederick C. Robbins , uppmärksammades 1954 för sina ansträngningar med ett Nobelpris i fysiologi eller medicin . Andra viktiga framsteg som ledde till utvecklingen av poliovaccin var: identifieringen av tre poliovirusserotyper ( Poliovirus typ 1 – PV1 eller Mahoney; PV2, Lansing; och PV3, Leon); upptäckten att före förlamning måste viruset finnas i blodet; och demonstrationen att administrering av antikroppar i form av gammaglobulin skyddar mot paralytisk polio.
1950–1955
Under det tidiga 1950-talet var poliofrekvensen i USA över 25 000 per år; 1952 och 1953 upplevde USA ett utbrott av 58 000 respektive 35 000 poliofall, upp från ett typiskt antal på cirka 20 000 per år, med dödsfall under dessa år på 3 200 och 1 400. Mitt i denna amerikanska polioepidemi investerades miljontals dollar i att hitta och marknadsföra ett poliovaccin av kommersiella intressen, inklusive Lederle Laboratories i New York under ledning av HR Cox . På Lederle arbetade också den polskfödda virologen och immunologen Hilary Koprowski från Wistar Institute i Philadelphia, som testade det första framgångsrika poliovaccinet 1950. Men hans vaccin, som är ett levande försvagat virus som tas oralt, var fortfarande på forskningsstadiet och skulle inte vara klar att användas förrän fem år efter att Jonas Salks poliovaccin (ett injicerbart vaccin med döda virus) hade nått marknaden. Koprowskis försvagade vaccin framställdes genom successiva passager genom hjärnan på schweiziska albinomöss. Vid den sjunde passagen kunde vaccinstammarna inte längre infektera nervvävnad eller orsaka förlamning. Efter ytterligare en till tre passager på råttor ansågs vaccinet vara säkert för mänsklig användning. Den 27 februari 1950 testades Koprowskis levande, försvagade vaccin för första gången på en 8-årig pojke som bor i Letchworth Village , en institution för fysiskt och mentalt funktionshindrade i New York. Efter att barnet inte hade några biverkningar utökade Koprowski sitt experiment till att omfatta 19 andra barn.
Jonas Salk


Det första effektiva poliovaccinet utvecklades 1952 av Jonas Salk och ett team vid University of Pittsburgh som inkluderade Julius Youngner , Byron Bennett, L. James Lewis och Lorraine Friedman, vilket krävde flera år av efterföljande tester. Salk gick på CBS radio för att rapportera ett framgångsrikt test på en liten grupp vuxna och barn den 26 mars 1953; två dagar senare publicerades resultaten i JAMA . Leone N. Farrell uppfann en nyckellaboratorieteknik som möjliggjorde massproduktion av vaccinet av ett team som hon ledde i Toronto. Med början den 23 februari 1954 testades vaccinet på Arsenal Elementary School och Watson Home for Children i Pittsburgh, Pennsylvania .
Salks vaccin användes sedan i ett test som kallas Francis Field Trial, ledd av Thomas Francis , det största medicinska experimentet i historien vid den tiden. Testet började med cirka 4 000 barn vid Franklin Sherman Elementary School i McLean, Virginia , och involverade så småningom 1,8 miljoner barn, i 44 delstater från Maine till Kalifornien . När studien avslutades fick ungefär 440 000 en eller flera injektioner av vaccinet, cirka 210 000 barn fick placebo, bestående av ofarliga odlingsmedier , och 1,2 miljoner barn fick ingen vaccination och fungerade som en kontrollgrupp, som sedan skulle observeras. för att se om någon fått polio.
Resultaten av fältförsöket tillkännagavs den 12 april 1955 (tioårsdagen av president Franklin D. Roosevelts död , vars paralytiska sjukdom allmänt troddes ha orsakats av polio). Salk-vaccinet hade varit 60–70 % effektivt mot PV1 (poliovirus typ 1), över 90 % effektivt mot PV2 och PV3 och 94 % effektivt mot utvecklingen av bulbar polio. Strax efter att Salks vaccin licensierades 1955 lanserades barnvaccinationskampanjer. I USA minskade det årliga antalet poliofall från 35 000 år 1953 till 5 600 år 1957 efter en massimmuniseringskampanj som främjades av March of Dimes. År 1961 registrerades endast 161 fall i USA.
En vecka före tillkännagivandet av resultaten från Francis Field Trial i april 1955 hade Pierre Lépine vid Pasteur-institutet i Paris också tillkännagett ett effektivt poliovaccin.
Säkerhetsincidenter
I april 1955, strax efter att massvaccination mot polio började i USA, började kirurgen få rapporter om patienter som drabbats av paralytisk polio ungefär en vecka efter att ha vaccinerats med Salk poliovaccin från läkemedelsföretaget Cutter, med förlamningen som började i extremiteten . vaccinet injicerades i. Cutter-vaccinet hade använts för att vaccinera 409 000 barn i västra och mellanvästra USA. Senare undersökningar visade att Cutter-vaccinet hade orsakat 260 fall av polio och dödat 11. Som svar drog kirurgen bort alla poliovacciner tillverkade av Cutter Laboratories från marknaden, men inte förrän 260 fall av paralytisk sjukdom hade inträffat. Eli Lilly, Parke-Davis, Pitman-Moore och Wyeth poliovacciner rapporterades också ha förlamat många barn. Det upptäcktes snart att en del mängder av Salk poliovaccin tillverkade av Cutter, Wyeth och de andra labben inte hade inaktiverats ordentligt, vilket släppte in levande poliovirus i mer än 100 000 doser vaccin. I maj 1955 inrättade National Institutes of Health and Public Health Services en teknisk kommitté för Poliomyelitvaccin för att testa och granska alla poliovaccinpartier och ge råd till Public Health Service om vilka partier som bör släppas för allmänt bruk. Dessa incidenter minskade allmänhetens förtroende för poliovaccin, vilket ledde till en minskning av vaccinationsfrekvensen.
1961
Samtidigt som Salk testade sitt vaccin fortsatte både Albert Sabin och Hilary Koprowski att arbeta med att utveckla ett vaccin med levande virus. Under ett möte i Stockholm för att diskutera poliovaccin i november 1955, presenterade Sabin resultat som erhållits på en grupp på 80 frivilliga, medan Koprowski läste ett dokument som beskriver resultaten av ett försök med 150 personer. Sabin och Koprowski lyckades båda så småningom utveckla vacciner. På grund av engagemanget för Salk-vaccinet i Amerika gjorde Sabin och Koprowski båda sina tester utanför USA, Sabin i Mexiko och Sovjetunionen, Koprowski i Kongo och Polen. 1957 utvecklade Sabin ett trivalent vaccin innehållande försvagade stammar av alla tre typerna av poliovirus. 1959 fick tio miljoner barn i Sovjetunionen Sabin oralt vaccin. För detta arbete fick Sabin medaljen av Order of Friendship of Peoples, som beskrivs som Sovjetunionens högsta civila ära. Sabins orala vaccin med levande virus kom i kommersiell användning 1961.
När Sabins orala vaccin blev allmänt tillgängligt, ersatte det Salks injicerade vaccin, som enligt allmänhetens åsikt hade fläckats av Cutter-incidenten 1955 , där Salk-vacciner felaktigt preparerade av ett företag ledde till att flera barn dog eller blev förlamade.
1987
En IPV med förstärkt styrka licensierades i USA i november 1987 och är för närvarande det valda vaccinet där. Den första dosen poliovaccin ges strax efter födseln, vanligtvis mellan 1 och 2 månaders ålder, och en andra dos ges vid 4 månaders ålder. Tidpunkten för den tredje dosen beror på vaccinets formulering, men bör ges mellan 6 och 18 månaders ålder. En boostervaccination ges vid 4 till 6 års ålder, totalt fyra doser vid eller före skolstart. I vissa länder ges en femte vaccination under tonåren . Rutinvaccination av vuxna (18 år och äldre) i utvecklade länder är varken nödvändig eller rekommenderad eftersom de flesta vuxna redan är immuna och har en mycket liten risk för exponering för vilda poliovirus i sina hemländer. År 2002 godkändes ett femvärt (femkomponent) kombinationsvaccin (kallat Pediarix) innehållande IPV för användning i USA.
1988
En global ansträngning för att utrota polio, ledd av Världshälsoorganisationen (WHO), UNICEF och Rotary Foundation , började 1988 och har till stor del förlitat sig på det orala poliovaccinet som utvecklats av Albert Sabin och Mikhail Chumakov (Sabin-Chumakov-vaccin) .
Efter 1990
Polio eliminerades i Amerika 1994. Sjukdomen eliminerades officiellt i 36 länder i västra Stilla havet, inklusive Kina och Australien, 2000. Europa förklarades poliofritt 2002. Sedan januari 2011 har inga fall av sjukdomen rapporterats i Indien, därför togs landet i februari 2012 bort från WHO:s lista över polioendemiska länder. I mars 2014 förklarades Indien ett poliofritt land.
Även om överföringen av poliovirus har avbrutits i stora delar av världen, fortsätter överföringen av vilda poliovirus och skapar en pågående risk för import av vilda poliovirus till tidigare poliofria regioner. Om import av poliovirus inträffar kan utbrott av poliomyelit utvecklas, särskilt i områden med låg vaccinationstäckning och dålig sanitet. Som ett resultat måste höga nivåer av vaccinationstäckning upprätthållas. I november 2013 meddelade WHO ett polioutbrott i Syrien. Som svar lade den armeniska regeringen ut ett meddelande där de bad syriska armenier under 15 år att få poliovaccin. Från och med 2014 hade poliovirus spridit sig till 10 länder, främst i Afrika, Asien och Mellanöstern, där Pakistan, Syrien och Kamerun gav råd om vaccinationer till utresande resenärer.
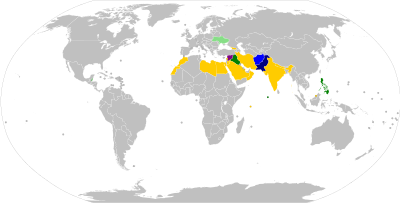
Poliovaccinationsprogram har motståtts av vissa människor i Pakistan, Afghanistan och Nigeria - de tre länderna från och med 2017 med kvarvarande poliofall. Nästan alla muslimska religiösa och politiska ledare har ställt sig bakom vaccinet, men en utkant minoritet tror att vaccinerna i hemlighet används för sterilisering av muslimer. Det faktum att CIA organiserade ett falskt vaccinationsprogram 2011 för att hjälpa till att hitta Usama Bin Laden är ytterligare en orsak till misstro. 2015 tillkännagav WHO ett avtal med talibanerna för att uppmuntra dem att distribuera vaccinet i områden de kontrollerar. De pakistanska talibanerna var dock inte stödjande. Den 11 september 2016 sköt två oidentifierade beväpnade män associerade med pakistanska talibaner, Jamaat-ul-Ahrar, Zakaullah Khan, en läkare som administrerade poliovaccin i Pakistan. Ledaren för Jamaat-ul-Ahrar tog på sig ansvaret för skjutningen och uppgav att gruppen skulle fortsätta denna typ av attack. Sådant motstånd mot och skepsis mot vaccinationer har följaktligen bromsat polioutrotningsprocessen i de två återstående endemiska länderna.
Resekrav
Resenärer som vill resa in i eller lämna vissa länder ska vara vaccinerade mot polio, vanligtvis högst 12 månader och minst 4 veckor innan gränspassering, samt kunna uppvisa vaccinationsjournal/-intyg vid gränskontrollerna. De flesta krav gäller endast för resor till eller från så kallade "polio-endemiska", "poliodrabbade", "polioexporterande", "polioöverförande" eller "högriskländer". Från och med augusti 2020 är Afghanistan och Pakistan de enda polioendemiska länderna i världen (där vild polio ännu inte har utrotats) . Flera länder har ytterligare säkerhetskrav för poliovaccination vid resor, till exempel till och från "viktiga riskländer", som från och med december 2020 inkluderar Kina, Indonesien, Moçambique, Myanmar och Papua Nya Guinea.
| Poliovaccinationskrav för internationella resor | |
|---|---|
| Land | Detaljer |
|
|
Resenärer från polioendemiska länder (Pakistan) behöver Carte Jaune- bevis på poliovaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. Invånare och ALLA resenärer som vistas i Afghanistan längre än 4 veckor behöver bevis på poliovaccination (mottagna mellan 4 veckor och 12 månader före avresa) vid avresa från Afghanistan. |
|
|
Resenärer från Afghanistan och Pakistan behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. Invånare i Belize som reser till länder med bekräftade poliofall behöver också bevis på vaccination. |
|
|
Resenärer från polioexporterande länder behöver Carte Jaune- bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från Afghanistan, Angola, Benin, Kamerun, Centralafrikanska republiken, Kina, Kongo-Kinshasa, Etiopien, Ghana, Indonesien, Kenya, Moçambique, Myanmar, Niger, Nigeria, Pakistan, Papua Nya Guinea, Filippinerna och Somalia behöver Carte Jaune bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från riskländer behöver Carte Jaune- bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. Resenärer utan bevis erbjuds OPV-vaccination vid ankomst. |
|
|
Resenärer från Afghanistan, Kongo-Kinshasa, Etiopien, Kenya, Nigeria, Pakistan, Somalia och Syrien behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresan) vid ankomst. |
|
|
Resenärer från Afghanistan, Pakistan och Nigeria behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. Resenärer utan bevis kommer att vaccineras vid ankomst. |
|
|
Resenärer i åldern 15+ från Afghanistan och Pakistan behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresan) vid ankomsten; barn under 15 år måste ha fått tre doser poliovaccin före resan. Resenärer utan bevis kommer att vaccineras vid ankomst. Resenärer som reser från Irak till Afghanistan och Pakistan måste också uppvisa bevis på vaccination vid avresan. |
|
|
Resenärer från Afghanistan och Pakistan behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från och till poliodrabbade länder behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från Afghanistan och Pakistan behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från och till polioexporterande länder, samt Hajj och Umrah -pilgrimer, behöver Carte Jaune- bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresan) vid ankomst. |
|
|
Resenärer från poliodrabbade länder behöver Carte Jaune- bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från Afghanistan, Kenya, Nigeria, Pakistan och Papua Nya Guinea behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresan) vid ankomst. |
|
|
Resenärer från polioexporterande länder behöver Carte Jaune- bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från ALLA länder som planerar att stanna i Pakistan i mer än 4 veckor behöver Carte Jaune- bevis på OPV-vaccination vid ankomst. Invånare och ALLA resenärer som vistas i Pakistan längre än 4 veckor behöver bevis på OPV-vaccination vid avresa från Pakistan. |
|
|
Resenärer från eller till högriskländer behöver Carte Jaune -bevis på poliovaccination vid ankomst respektive före avresa. På grund av ett pågående lokalt VDPV2-utbrott rekommenderar regeringen alla andra resenärer att överväga att skaffa ett poliovaccin eller boosterdos, beroende på deras situation. |
|
|
Resenärer från polioexporterande länder (identifierade av Qatar som: Afghanistan, Nigeria, Pakistan och Filippinerna) behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från polioendemiska länder som identifierats av WHO (Afghanistan och Pakistan) behöver Carte Jaune- bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresan) vid ankomst. |
|
|
Resenärer från aktiv överföring (inklusive vilda eller vaccin-härledda poliovirus) och riskländer, såväl som alla resenärer från Afghanistan, Kongo-Kinshasa, Moçambique, Myanmar, Niger, Nigeria, Pakistan, Papua Nya Guinea, Somalia, Syrien, och Jemen, behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresa) vid ankomst. Oavsett immuniseringsstatus kommer alla resenärer från Afghanistan, Myanmar, Nigeria, Pakistan, Papua Nya Guinea, Somalia, Syrien och Jemen att få en oral poliovaccindos vid ankomsten. |
|
|
Resenärer från länder med polioutbrott behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagna mellan 4 veckor och 12 månader före avresa) vid ankomst. |
|
|
Resenärer från Kamerun, Ekvatorialguinea och Pakistan behöver Carte Jaune -bevis på OPV- eller IPV-vaccination (mottagen mellan 4 veckor och 12 månader före avresan) vid ankomst. ALLA invånare i Syrien som lämnar Syrien till något land behöver också bevis på vaccination. |
|
|
Långtidsbesökare som reser till stater med vild eller cirkulerande vaccin-härledd poliovirusöverföring bör visa Carte Jaune -bevis på vaccination med minst en dos av bivalent OPV eller IPV (mottagen mellan 4 veckor och 12 månader före avresa). Personer som är skyldiga att genomföra akuta internationella resor måste vaccineras med en engångsdos poliovaccin före avresan. Det finns också risk för överföring av poliovirus i själva Ukraina, och resenärer till Ukraina rekommenderas att vara uppdaterade med sin poliovaccination före inresan. |
Samhälle och kultur
Kosta
Från och med 2015 levererar Global Alliance for Vaccines and Immunization det inaktiverade vaccinet till utvecklingsländer för så lite som 0,75 € (cirka 0,89 USD ) per dos i 10-dosflaskor.
Missuppfattningar
En missuppfattning har funnits i Pakistan att poliovaccinet innehåller haramingredienser och kan orsaka impotens och infertilitet hos manliga barn, vilket leder till att vissa föräldrar inte låter vaccinera sina barn. Denna uppfattning är vanligast i Khyber Pakhtunkhwa- provinsen och FATA -regionen. Attacker mot poliovaccinationsteam har också förekommit, vilket hindrar internationella ansträngningar för att utrota polio i Pakistan och globalt.
Referenser
Vidare läsning
- Ramsay M, red. (2013). "Polio: den gröna boken, kapitel 26" . Immunisering mot infektionssjukdomar . London: Public Health England.
- Hall E, Wodi AP, Hamborsky J, Morelli V, Schillie S, eds. (2021). "Kapitel 18: Poliomyelit" . Epidemiology and Prevention of Vaccine-Preventable Diseases (14:e upplagan). Washington DC: US Centers for Disease Control and Prevention (CDC).
- Routh JA, Oberste MS, Patel M (2018). "Kapitel 12: Poliomyelit" . I Roush SW, Baldy LM, Hall MH (red.). Manual för övervakning av sjukdomar som kan förebyggas med vaccin . Atlanta, Georgia: US Centers for Disease Control and Prevention (CDC).
externa länkar
- "Information om poliovaccin" . Centers for Disease Control and Prevention (CDC) . augusti 2021.
- History of Vaccines Webbplats – History of Polio History of Vaccines, ett projekt från College of Physicians of Philadelphia
- PBS.org – 'People and Discoveries: Salk Produces Polio Vaccine 1952', Public Broadcasting Service (PBS)
- "IPOL – Poliovirusvaccin inaktiverat (monkey Kidney Cell)" . US Food and Drug Administration (FDA) . 11 december 2019. STN: 103930.
- Poliovirusvacciner vid US National Library of Medicine Medical Subject Headings (MeSH)