Lovastatin - Lovastatin
 | |
 | |
| Kliniska data | |
|---|---|
| Handelsnamn | Mevacor, Altocor, andra |
| Andra namn | Monacolin K, Mevinolin |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a688006 |
| Licensdata | |
| Vägar administrering |
Via mun |
| ATC -kod | |
| Rättslig status | |
| Rättslig status | |
| Farmakokinetiska data | |
| Biotillgänglighet | <5% |
| Proteinbindning | > 98% |
| Ämnesomsättning | Lever (CYP3A och CYP2C8 -substrat ) |
| Eliminering halveringstid | 2–5 timmar |
| Exkretion | Avföring (83%), urin (10%) |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.115.931 |
| Kemiska och fysiska data | |
| Formel | C 24 H 36 O 5 |
| Molmassa | 404,547 g · mol −1 |
| 3D -modell ( JSmol ) | |
| |
| |
| (kontrollera) | |
Lovastatin , som bland annat säljs under varumärket Mevacor , är ett statinmedicin för att behandla högt kolesterol i blodet och minska risken för hjärt -kärlsjukdom . Dess användning rekommenderas tillsammans med livsstilsförändringar. Det tas genom munnen.
Vanliga biverkningar inkluderar diarré, förstoppning, huvudvärk, muskelsmärtor, utslag och sömnsvårigheter. Allvarliga biverkningar kan inkludera leverproblem , muskelnedbrytning och njursvikt . Användning under graviditeten kan skada barnet och användning under amning rekommenderas inte. Det fungerar genom att minska leverförmågan att producera kolesterol genom att blockera enzymet HMG-CoA-reduktas .
Lovastatin patenterades 1979 och godkändes för medicinsk användning 1987. Det finns på Världshälsoorganisationens lista över viktiga läkemedel . Det finns som en generisk medicinering . År 2019 var det den 95: e vanligaste förskrivna medicinen i USA, med mer än 8 miljoner recept.
Medicinsk användning
Lovastatin används främst för behandling av dyslipidemi och förebyggande av hjärt -kärlsjukdom . Det rekommenderas att användas endast efter att andra åtgärder, såsom kost, träning och viktminskning, inte har förbättrat kolesterolnivåerna.
Bieffekter
Lovastatin tolereras vanligtvis väl, med de vanligaste biverkningarna i ungefär fallande frekvensordning: förhöjning av kreatinfosfokinas , flatulens , buksmärta, förstoppning, diarré , muskelvärk eller smärta , illamående, matsmältningsbesvär , svaghet, dimsyn, utslag, yrsel och muskelkramper. Som med alla statinläkemedel kan det sällan orsaka myopati , hepatotoxicitet (leverskada), dermatomyosit eller rabdomyolys . Detta kan vara livshotande om det inte känns igen och behandlas i tid, så eventuell oförklarlig muskelsmärta eller svaghet vid behandling med lovastatin bör omedelbart omnämnas till den ordinerande läkaren. Andra ovanliga biverkningar som omedelbart bör nämnas för antingen den ordinerande läkaren eller akutsjukvården inkluderar:
- muskelsmärta, ömhet eller svaghet
- brist på energi
- svaghet
- feber
- mörkfärgad urin
- gulsot : gulning av hud eller ögon
- smärta i övre högra delen av magen
- illamående
- ovanlig blödning eller blåmärken
- aptitlöshet
- influensaliknande symptom
- utslag
- nässelfeber
- klåda
- svårigheter att andas eller svälja
- svullnad i ansikte, hals, tunga, läppar, ögon, händer, fötter, vrister eller underben
- heshet
Dessa mindre allvarliga biverkningar bör fortfarande rapporteras om de kvarstår eller ökar i svårighetsgrad:
- förstoppning
- minnesförlust eller glömska
- förvirring
Kontraindikationer
Kontraindikationer , tillstånd som motiverar att behandlingen med lovastatin upphör, inkluderar graviditet, amning och leversjukdom. Lovastatin är kontraindicerat under graviditet (graviditetskategori X); det kan orsaka fosterskador som skelettdeformiteter eller inlärningssvårigheter. På grund av dess potential att störa lipidmetabolismen hos spädbarn bör lovastatin inte tas under amning. Patienter med leversjukdom ska inte ta lovastatin.
Interaktioner
Liksom med atorvastatin , simvastatin och andra statinläkemedel som metaboliseras via CYP3A4 kan dricka grapefruktjuice under behandling med lovastatin öka risken för biverkningar. Komponenter av grapefruktjuice, flavonoid naringin eller furanokumarin bergamottin hämmar CYP3A4 in vitro och kan bero på in vivo -effekten av grapefruktjuicekoncentrat som minskar metabolisk clearance av lovastatin och ökar dess plasmakoncentrationer.
Handlingsmekanism
Lovastatin är en hämmare av 3-hydroxi-3-metylglutaryl-koenzym A-reduktas (HMG-CoA-reduktas), ett enzym som katalyserar omvandlingen av HMG-CoA till mevalonat. Mevalonate är en nödvändig byggsten för kolesterolbiosyntes och lovastatin stör produktionen genom att fungera som en reversibel konkurrerande hämmare för HMG-CoA, som binder till HMG-CoA-reduktas. Lovastatin är ett prodrug , en inaktiv lakton i sin naturliga form, gamma-lakton-slutna ringformen i vilken den administreras, hydrolyseras in vivo till ß-hydroxisyrans öppna ringform; som är den aktiva formen.
Lovastatin och andra statiner har studerats för deras kemopreventiva och kemoterapeutiska effekter. Inga sådana effekter sågs i de tidiga studierna. Nyare undersökningar avslöjade vissa kemopreventiva och terapeutiska effekter för vissa typer av cancer, särskilt i kombination med statiner med andra cancerläkemedel. Det är troligt att dessa effekter förmedlas av egenskaperna av statiner för att minska proteasom -aktivitet, vilket leder till en ackumulering av cyklin-beroende kinashämmare p21 och p27 , och till efterföljande G 1 -fas stillestånd, såsom ses i celler av olika cancerlinjer.
Historia

Kompaktin och lovastatin, naturliga produkter med en kraftfull hämmande effekt på HMG-CoA-reduktas , upptäcktes på 1970-talet och togs in i klinisk utveckling som potentiella läkemedel för att sänka LDL- kolesterol.
År 1982 genomfördes några småskaliga kliniska undersökningar av lovastatin, en polyketid-härledd naturprodukt isolerad från Aspergillus terreus , hos mycket högriskpatienter, där dramatiska minskningar av LDL-kolesterol observerades, med mycket få negativa effekter. Efter att de ytterligare djursäkerhetsstudierna med lovastatin inte avslöjade någon toxicitet av den typ som antas vara associerad med compactin, fortsatte kliniska studier.
Storskaliga försök bekräftade effektiviteten av lovastatin. Observerad tolerabilitet fortsatte att vara utmärkt, och lovastatin godkändes av amerikanska FDA 1987. Det var det första statinet som godkändes av FDA.
Lovastatin produceras också naturligt av vissa högre svampar , såsom Pleurotus ostreatus (ostronsvamp) och närbesläktade Pleurotus spp. Forskning om effekten av ostronsvamp och dess extrakt på kolesterolnivåerna hos försöksdjur har varit omfattande, även om effekten har visats hos ett mycket begränsat antal människor.
År 1998 förbjöd FDA försäljning av kosttillskott från rött jästris , som naturligt innehåller lovastatin, och hävdade att produkter som innehåller receptbelagda läkemedel kräver godkännande av läkemedel. Domare Dale A. Kimball vid USA: s tingsrätt för District of Utah beviljade en ansökan från Cholestins tillverkare, Pharmanex, om att byråns förbud var olagligt enligt hälso- och utbildningslagen från 1994 för att produkten marknadsfördes som ett kosttillskott , inte ett läkemedel.
Målet är att minska överskottet av kolesterol till en mängd som överensstämmer med upprätthållandet av normal kroppsfunktion. Kolesterol biosyntetiseras i en serie med mer än 25 separata enzymatiska reaktioner som initialt involverar tre successiva kondensationer av acetyl-CoA-enheter för att bilda sexkolföreningen 3-hydroxi-3-metylglutarylkoenzym A (HMG CoA). Detta reduceras till mevalonat och omvandlas sedan i en serie reaktioner till isoprenerna som är byggstenar av squalen , den omedelbara föregångaren till steroler, som cykliserar till lanosterol (en metylerad sterol) och vidare metaboliseras till kolesterol. Ett antal tidiga försök att blockera syntesen av kolesterol resulterade i medel som inhiberade sent i den biosyntetiska vägen mellan lanosterol och kolesterol. Ett stort hastighetsbegränsande steg i vägen är på nivån av det mikrosomala enzymet som katalyserar omvandlingen av HMG CoA till mevalonsyra, och det har ansetts vara ett primärt mål för farmakologisk intervention i flera år.
HMG CoA -reduktas inträffar tidigt i den biosyntetiska vägen och är bland de första åtagandena för kolesterolformulering. Hämning av detta enzym kan leda till ackumulering av HMG CoA, en vattenlöslig mellanprodukt som då lätt kan metaboliseras till enklare molekyler. Denna inhibering av reduktas skulle leda till ackumulering av lipofyliska mellanprodukter med en formell sterolring.
Lovastatin var den första specifika hämmaren av HMG CoA -reduktas som fick godkännande för behandling av hyperkolesterolemi. Det första genombrottet i ansträngningarna att hitta en potent, specifik, konkurrenskraftig hämmare av HMG CoA -reduktas inträffade 1976, då Endo et al. rapporterade upptäckten av mevastatin , en mycket funktionaliserad svampmetabolit, isolerad från kulturer av Penicillium citrium .
Biosyntes
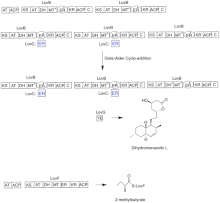
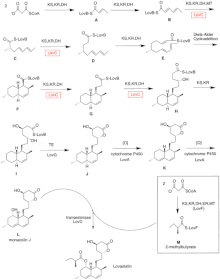
Biosyntesen av lovastatin sker via en iterativ typ I polyketidsyntas (PKS). De sex gener som kodar för enzymer som är väsentliga för biosyntesen av lovastatin är lovB, lovC, lovA, lovD, lovG och lovF. Syntesen av dihydromonakolin L kräver totalt 9-malonyl Coa. Den fortsätter i PKS-vägen tills den når (E) en hexaketide, där den genomgår en Diels-Alder-cykladdition för att bilda de sammansmälta ringarna. Efter cyklisering fortsätter den genom PKS -vägen tills den når (I) en nonaketide, som sedan genomgår frigöring från LovB genom tioesteras som kodas av LovG. Dihydromonacolin L, (J), genomgår sedan oxidation och uttorkning via ett cytokrom P450 oxygenas som kodas av LovA för att erhålla monakolin J, (L) .
MT-domänen från lovB är aktiv vid omvandlingen av ( B) till ( C) när den överför en metylgrupp från S-adenosyl-L-metionin (SAM) till tetraketiden (C) . På grund av att LovB innehåller en inaktiv ER -domän krävs LovC vid specifika steg för att få helt reducerade produkter. Domänorganisationen för LovB, LovC, LovG och LovF visas i figur 2. Den inaktiva ER -domänen för lovB visas med en oval och där LovC verkar i trans till LovB visas med en röd ruta.
I en parallell väg syntetiseras diketidsidokedjan av lovastatin av ett annat mycket reducerande typ I polyketidsyntasenzym som kodas av LovF. Slutligen är sidokedjan, 2-metylbutyrat (M) kovalent bunden till C-8-hydroxigruppen av monakolin J (L) med ett transesteras som kodas av LovD för att bilda lovastatin.
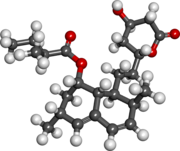
Total syntes
En stor del av arbetet med syntesen av lovastatin utfördes av M. Hirama på 1980 -talet. Hirama syntetiserade compactin och använde en av mellanprodukterna för att följa en annan väg för att komma till lovastatin. Den syntetiska sekvensen visas i scheman nedan. Y-laktonen syntetiserades med användning av Yamada-metodik som började med glutaminsyra. Laktonöppning utfördes med användning av litiummetoxid i metanol och sedan silylering för att ge en separerbar blandning av utgångslaktonen och silyletern . Silyletern vid hydrogenolys följt av Collins oxidation gav aldehyden. Stereoselektiva framställningen av (E, E) -dien åstadkoms genom tillsats av trans-krotyl fenylsulfon anjon, följt av släckning med Ac 2 O och efterföljande reduktiv eliminering av sulfon acetat. Kondensering av detta med litiumanjon av dimetylmetylfosfonat gav förening 1. Förening 2 syntetiserades såsom visas i schemat i det syntetiska förfarandet. Föreningarna 1 och 2 kombinerades sedan med användning av 1,3 ekv natriumhydrid i THF följt av återflöde i klorbensen under 82 timmar under kväve för att få enonen 3.
Enkla organiska reaktioner användes för att komma till lovastatin som visas i schemat.
Samhälle och kultur
Naturliga källor
Lovastatin är en naturligt förekommande förening som finns i låga halter i livsmedel som ostronsvamp , rött jästris och Pu-erh .
Märkesnamn
Mevacor, Advicor (som en kombination med niacin ), Altocor, Altoprev
Andra applikationer
Inom växtfysiologi har lovastatin ibland använts som hämmare av cytokininbiosyntes .
Se även
Referenser
externa länkar
![]() Media relaterade till Lovastatin på Wikimedia Commons
Media relaterade till Lovastatin på Wikimedia Commons
- "Lovastatin" . Läkemedelsinformationsportal . US National Library of Medicine.