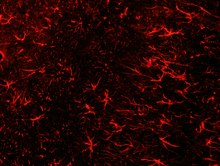
Astroglios - Astrogliosis
| Astroglios | |
|---|---|
 Bildande av reaktiva astrocyter efter skada på centrala nervsystemet (CNS)
| |
| Anatomisk terminologi |
Astroglios (även känd som astrocytosis eller kallad reaktiv astroglios ) är en onormal ökning i antalet astrocyter på grund av förstörelse av närliggande neuroner från centrala nervsystemet (CNS) trauma , infektion , ischemi , stroke , autoimmuna responser eller neurodegenerativ sjukdom . I friska neurala vävnader spelar astrocyter viktiga roller för energiförsörjning, reglering av blodflöde, homeostas av extracellulär vätska, homeostas av joner och sändare, reglering av synapsfunktion och synaptisk ombyggnad. Astroglios förändrar molekylära uttryck och morfologi hos astrocyter, som svar på infektion, till exempel i allvarliga fall som orsakar glialärrbildning som kan hämma axonregenerering .
Orsaker
Reaktiv astroglios är ett spektrum av förändringar i astrocyter som uppstår som svar på alla former av CNS -skada och sjukdom. Förändringar på grund av reaktiv astroglios varierar med svårighetsgraden av CNS -förolämpningen längs ett gradvis kontinuum av progressiva förändringar i molekylärt uttryck, progressiv cellulär hypertrofi , proliferation och ärrbildning.
Förolämpningar av neuroner i centrala nervsystemet orsakade av infektion, trauma, ischemi, stroke, återkommande anfall, autoimmuna svar eller andra neurodegenerativa sjukdomar kan orsaka reaktiva astrocyter.
När astroglios är patologisk i sig, i stället för ett normalt svar på ett patologiskt problem, kallas det astrocytopati .
Funktioner och effekter
Reaktiva astrocyter kan gynna eller skada omgivande neurala och icke-neurala celler. De genomgår en rad förändringar som kan förändra astrocytaktiviteter genom förstärkning eller förlust av funktioner som lånar ut till neuralt skydd och reparation, ärrbildning i glial och reglering av CNS -inflammation .
Neuralt skydd och reparation
Förökning av reaktiva astrocyter är avgörande för ärrbildning och funktion för att minska spridning och uthållighet av inflammatoriska celler , för att upprätthålla reparationen av blod-hjärnbarriären (BBB), för att minska vävnadsskador och lesionsstorlek och för att minska neuronal förlust och demyelinisering.
Reaktiva astrocyter försvarar sig mot oxidativ stress genom glutationproduktion och har ansvaret för att skydda CNS -celler från NH 4 + -toxicitet. De skyddar CNS -celler och vävnad genom olika metoder, såsom upptag av potentiellt excitotoxiskt glutamat , adenosinfrisättning och nedbrytning av amyloid β -peptider . Reparationen av ett avbrott i blodhjärnbarriären underlättas också av reaktiva astrocyter genom deras direkta slutfötter (karaktäristiska strukturer för astrocyter ) interaktion med blodkärlens väggar som inducerar blodhjärnbarriäregenskaper .
De har också visat sig minska vasogent ödem efter trauma, stroke eller obstruktiv hydrocephalus .
Ärrbildning
Förökande reaktiva ärrbildande astrocyter finns konsekvent längs gränserna mellan friska vävnader och fickor av skadad vävnad och inflammatoriska celler. Detta återfinns vanligtvis efter ett snabbt, lokalt utlöst inflammatoriskt svar på akut traumatisk skada i ryggmärgen och hjärnan . I sin extrema form kan reaktiv astroglios leda till uppkomsten av nyförökade astrocyter och ärrbildning som svar på allvarlig vävnadsskada eller inflammation.
Molekylära triggers som leder till denna ärrbildning inkluderar epidermal tillväxtfaktor (EGF), fibroblast tillväxtfaktor (FGF), endotelin 1 och adenosintrifosfat (ATP). Mogna astrocyter kan åter komma in i cellcykeln och föröka sig under ärrbildning. Vissa spridande reaktiva astrocyter kan härledas från NG2 -stamceller i det lokala parenkymet från ependymala cellprogenitorer efter skada eller stroke. Det finns också multipotenta progenitorer i subependymal vävnad som uttrycker glialt fibrillärt surt protein ( GFAP ) och genererar avkommaceller som migrerar mot skador efter trauma eller stroke.
Reglering av inflammation
Reaktiva astrocyter är relaterade till astrocyternas normala funktion. Astrocyter är involverade i den komplexa regleringen av CNS-inflammation som sannolikt är kontextberoende och reglerad av multimodala extra- och intracellulära signalhändelser. De har kapacitet att göra olika typer av molekyler med antingen pro- eller antiinflammatorisk potential som svar på olika typer av stimulering. Astrocyter interagerar mycket med mikroglia och spelar en nyckelroll i CNS -inflammation. Reaktiva astrocyter kan sedan leda till onormal funktion av astrocyter och påverka deras reglering och reaktion på inflammation.
När det gäller antiinflammatoriska effekter hjälper reaktiva ärrbildande astrocyter till att minska spridningen av inflammatoriska celler under lokalt initierade inflammatoriska svar på traumatisk skada eller under periferinitierade adaptiva immunsvar. När det gäller pro-inflammatorisk potential är vissa molekyler i astrocyter associerade med en ökning av inflammation efter traumatisk skada.
I tidiga stadier efter förolämpningar aktiverar astrocyter inte bara inflammation utan bildar också kraftfulla cellmigrationshinder över tid. Dessa barriärer markerar områden där intensiv inflammation behövs och begränsar spridningen av inflammatoriska celler och smittämnen till närliggande frisk vävnad. CNS -skadesvar har gynnat mekanismer som håller små skador oinfekterade. Hämning av migrationen av inflammatoriska celler och infektiösa medel har lett till oavsiktlig biprodukt av axonregenerationshämning, på grund av redundansen mellan migrationssignaler mellan celltyper.
Biologiska mekanismer
Förändringar till följd av astroglios regleras på ett kontextspecifikt sätt av specifika signalhändelser som har potential att ändra både karaktären och graden av dessa förändringar. Under olika stimuleringsförhållanden kan astrocyter producera intercellulära effektormolekyler som förändrar molekylernas uttryck i cellaktiviteter av cellstruktur, energimetabolism, intracellulär signalering och membrantransportörer och pumpar. Reaktiva astrocyter reagerar enligt olika signaler och påverkar neuronal funktion. Molekylära mediatorer frigörs av neuroner , mikroglia , oligodendrocytlinjeceller , endotel , leukocyter och andra astrocyter i CNS -vävnaden som svar på förolämpningar som sträcker sig från subtila cellulära störningar till intensiv vävnadsskada. De resulterande effekterna kan sträcka sig från blodflödesreglering till energiförsörjning till synaptisk funktion och neural plasticitet .
Signalmolekyler
Få av de kända signalmolekylerna och deras effekter förstås i samband med reaktiva astrocyter som reagerar på olika grader av förolämpning.
Uppreglering av GFAP , som induceras av FGF , TGFB och ciliär neurotrofisk faktor (CNTF), är en klassisk markör för reaktiv glios. Axonregenerering sker inte i områden med en ökning av GFAP och vimentin . Paradoxalt nog är en ökning av GFAP -produktionen också specifik för minimering av lesionsstorleken och minskning av risken för autoimmun encefalomyelit och stroke .
Transportörer och kanaler
Närvaron av astrocyternas glutamat transportörer är associerad med en reducerad antal kramper och minskad neurodegeneration medan astrocyt gap junction-protein Cx43 bidrar till den neuroprotektiva effekten av prekonditionering till hypoxi . Dessutom spelar AQP4 , en astrocytvattenkanal, en avgörande roll vid cytotoxiskt ödem och förvärrar resultatet efter stroke .
Neurologiska patologier
Förlust eller störning av funktioner som normalt utförs av astrocyter eller reaktiva astrocyter under processen med reaktiv astroglios har potential att ligga till grund för neural dysfunktion och patologi under olika tillstånd, inklusive trauma , stroke , multipel skleros och andra. Några av exemplen är följande:
- Autoimmun förstörelse av astrocytändfötter som kontaktar och omsluter blodkärl är associerad med inflammation i CNS och en form av multipel skleros
- Rasmussens syndrom förstörelse av astrocyter orsakar anfall
- I Alexander sjukdom , är en dominant, förstärknings-of-funktion mutation av den gen som kodar GFAP associerad med makro encefalopati , kramper , psykomotoriska störningar, och för tidig död.
- I en familjär form av amyotropisk lateral skleros ( ALS ) leder en dominerande gain-of-function-mutation av genen som kodar för superoxiddismutas (SOD) till produktion av reaktiva astrocyter av molekyler som är giftiga för motorneuroner.
Reaktiva astrocyter kan också stimuleras av specifika signalkaskader för att få skadliga effekter såsom följande:
- Försämring av inflammation via cytokin produktion
- Produktion och frisättning av neurotoxiska nivåer av reaktiva syrearter
- Frisättning av potentiellt excitotoxiskt glutamat
- Den potentiella bidrag till beslag genesis
- Kompromiss med blod-hjärnbarriärfunktionen till följd av produktion av vaskulära endotelväxtfaktorer
- Cytotoxiskt ödem under trauma och stroke genom överaktivitet AQP4
- Potential för kronisk cytokinaktivering av astrocyter för att bidra till kronisk smärta
Reaktiva astrocyter har potential att främja neuraltoxicitet via de cytotoxiska molekylerna som kväveoxidradikaler och andra reaktiva syrearter , som kan skada närliggande neuroner. Reaktiva astrocyter kan också främja sekundär degeneration efter CNS -skada.
Nya terapeutiska tekniker
På grund av de destruktiva effekterna av astroglios, som inkluderar förändrat molekylärt uttryck, frisättning av inflammatoriska faktorer, astrocytproliferation och neuronal dysfunktion, letar forskare för närvarande efter nya sätt att behandla astroglios och neurodegenerativa sjukdomar. Olika studier har visat astrocyters roll vid sjukdomar som Alzheimers , amyotrofisk lateral skleros ( ALS ), Parkinsons och Huntingtons . Inflammationen som orsakas av reaktiv astroglios förstärker många av dessa neurologiska sjukdomar. Aktuella studier undersöker möjliga fördelar med att hämma inflammationen orsakad av reaktiv glios för att minska dess neurotoxiska effekter.
Neurotrofiner forskas för närvarande som möjliga läkemedel för neuronskydd, eftersom de har visat sig återställa neuronal funktion. Till exempel har några studier använt nervtillväxtfaktorer för att återfå viss kolinerg funktion hos patienter med Alzheimers .
Anti-glios-funktion hos BB14
En specifik läkemedelskandidat är BB14, som är en nervtillväxtfaktorliknande peptid som fungerar som en TrkA- agonist . BB14 visade sig minska reaktiv astroglios efter perifera nervskador hos råttor genom att verka på DRG- och PC12 -celldifferentiering. Även om ytterligare forskning behövs, har BB14 potential att behandla en mängd olika neurologiska sjukdomar. Ytterligare forskning av neurotrofiner kan potentiellt leda till utvecklingen av en mycket selektiv, potent och liten neurotrofin som riktar sig mot reaktiv glios för att lindra vissa neurodegenerativa sjukdomar.
Reglerande funktion för TGFB
TGFB är en reglerande molekyl som är involverad i proteoglykanproduktion . Denna produktion ökar i närvaro av bFGF eller Interleukin 1 . En anti-TGFβ-antikropp kan potentiellt minska GFAP- uppreglering efter CNS-skador, vilket främjar axonal regenerering.
Etidiumbromidbehandling
Injektion av etidiumbromid dödar alla CNS -glia ( oligodendrocyter och astrocyter ), men lämnar axoner, blodkärl och makrofager opåverkade. Detta ger en miljö som bidrar till axonal regenerering i cirka fyra dagar. Efter fyra dagar återinvinner CNS glia området för injektion och axonal regenerering hämmas följaktligen. Denna metod har visat sig minska ärrbildning av glialer efter trauma i CNS.
Metalloprotineasaktivitet
Oligodendrocytprekursorceller och C6 -gliomceller producerar metalloproteinas , vilket visar sig inaktivera en typ av hämmande proteoglykan som utsöndras av Schwann -celler . Följaktligen kan ökat metalloproteinas i miljön runt axoner underlätta axonal regenerering via nedbrytning av hämmande molekyler på grund av ökad proteolytisk aktivitet.