Angiotensin -konverterande enzym - Angiotensin-converting enzyme
| Angiotensin-konverterande enzym | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifierare | |||||||||
| EG -nr. | 3.4.15.1 | ||||||||
| CAS -nr. | 9015-82-1 | ||||||||
| Databaser | |||||||||
| IntEnz | IntEnz -vy | ||||||||
| BRENDA | BRENDA -inträde | ||||||||
| ExPASy | NiceZyme -vy | ||||||||
| KEGG | KEGG -post | ||||||||
| MetaCyc | Metabolisk väg | ||||||||
| PRIAM | profil | ||||||||
| PDB -strukturer | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
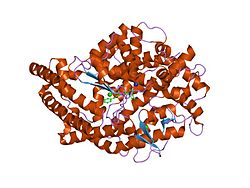
Angiotensin-konverterande enzym ( EC 3.4.15.1 ), eller ACE , är en central komponent i renin-angiotensinsystemet (RAS), som styr blodtrycket genom att reglera vätskevolymen i kroppen. Det omvandlar hormonet angiotensin I till det aktiva vasokonstriktorn angiotensin II . Därför ökar ACE indirekt blodtrycket genom att få blodkärlen att dras ihop. ACE -hämmare används ofta som läkemedel för behandling av hjärt -kärlsjukdomar .
Enzymet upptäcktes av Leonard T. Skeggs Jr. 1956. Den första kristallstrukturen för mänskliga testiklar ACE löstes år 2002 av R. Natesh i laboratoriet av K. Ravi Acharya och arbetet publicerades i tidskriften Nature in Januari 2003. Det ligger huvudsakligen i lungornas kapillärer men kan också hittas i endotel- och njurepitelceller .
Andra mindre kända funktioner för ACE är nedbrytning av bradykinin , substans P och amyloid beta-protein .
Nomenklatur
ACE är också känt under följande namn:
- dipeptidylkarboxipeptidas I
- peptidas P
- dipeptidhydrolas
- peptidyldipeptidas
- angiotensinkonverterande enzym
- kininas II
- angiotensin I-konverterande enzym
- karboxikatepsin
- dipeptidylkarboxipeptidas
- "hypertensinkonverterande enzym" peptidyldipeptidas I
- peptidyldipeptidhydrolas
- peptidyldipeptidhydrolas
- endotelcellpeptidyldipeptidas
- peptidyldipeptidas-4
- PDH
- peptidyldipeptidhydrolas
- DCP
- CD143
Fungera
ACE hydrolyserar peptider genom avlägsnande av en dipeptid från C-terminalen. På samma sätt omvandlar den den inaktiva decapeptiden angiotensin I till octapeptiden angiotensin II genom att avlägsna dipeptiden His-Leu.
ACE är en central komponent i renin -angiotensinsystemet (RAS), som styr blodtrycket genom att reglera vätskevolymen i kroppen.

Angiotensin II är en potent vasokonstriktor på ett substratkoncentrationsberoende sätt. Angiotensin II binder till typ 1 angiotensin II -receptorn (AT1) , vilket utlöser ett antal åtgärder som resulterar i vasokonstriktion och därför ökat blodtryck.
ACE är också en del av kinin-kallikreinsystemet där det bryter ned bradykinin , en kraftig vasodilatator och andra vasoaktiva peptider.
Kininas II är detsamma som angiotensinkonverterande enzym. Således slipper samma enzym (ACE) som genererar en vasokonstriktor (ANG II) också vasodilatatorer (bradykinin).
Mekanism
ACE är ett zinkmetalloproteinas . Zinkjonen är avgörande för dess aktivitet, eftersom den direkt deltar i katalysen av peptidhydrolysen. Därför kan ACE hämmas av metallkelaterande medel.

E384 -resten visade sig ha en dubbel funktion. Först fungerar det som en allmän bas för att aktivera vatten som en nukleofil. Då fungerar det som en allmän syra för att klyva CN -bindningen.
Kloridjonens funktion är mycket komplex och debatteras mycket. Anjonaktiveringen med klorid är ett karakteristiskt drag hos ACE. Det bestämdes experimentellt att aktiveringen av hydrolys med klorid är starkt beroende av substratet. Även om det ökar hydrolyshastigheterna för t.ex. Hip-His-Leu hämmar det hydrolys av andra substrat som Hip-Ala-Pro. Under fysiologiska förhållanden når enzymet cirka 60% av sin maximala aktivitet mot angiotensin I medan det når sin fulla aktivitet mot bradykinin. Det antas därför att anjonaktiveringens funktion i ACE ger hög substratspecificitet. Andra teorier säger att kloriden helt enkelt kan stabilisera enzymets övergripande struktur.
Genetik
ACE -genen, ACE , kodar för två isozymer . Det somatiska isozymet uttrycks i många vävnader, huvudsakligen i lungan, inklusive vaskulära endotelceller , epiteliala njurceller och testikulära Leydig -celler , medan germinalen endast uttrycks i spermier . Hjärnvävnad har ACE -enzym, som deltar i lokal RAS och omvandlar Aβ42 (som aggregerar till plack) till Aβ40 (som man tror är mindre giftigt) former av beta -amyloid . Det senare är övervägande en funktion av N -domändelen på ACE -enzymet. ACE-hämmare som passerar blod-hjärnbarriären och som företrädesvis har vald N-terminal aktivitet kan därför orsaka ackumulering av Aβ42 och progression av demens.
Sjukdomsrelevans
ACE -hämmare används i stor utsträckning som farmaceutiska läkemedel vid behandling av tillstånd som högt blodtryck , hjärtsvikt , diabetisk nefropati och typ 2 -diabetes mellitus .
ACE -hämmare hämmar ACE konkurrenskraftigt. Det resulterar i minskad bildning av angiotensin II och minskad metabolism av bradykinin , vilket leder till systematisk utvidgning av artärer och vener och en minskning av arteriellt blodtryck. Dessutom minskar angiotensin II-bildning av angiotensin II-medierad aldosteronsekretion från binjurebarken , vilket leder till en minskning av vatten- och natriumreabsorption och en minskning av extracellulär volym.
ACE: s effekt på Alzheimers sjukdom är fortfarande mycket debatterad. Alzheimers patienter visar vanligtvis högre ACE -nivåer i hjärnan. Vissa studier tyder på att ACE-hämmare som kan passera blod-hjärnbarriären (BBB) kan öka aktiviteten hos stora amyloid-beta-peptidnedbrytande enzymer som neprilysin i hjärnan vilket resulterar i en långsammare utveckling av Alzheimers sjukdom. Nyare forskning tyder på att ACE-hämmare kan minska risken för Alzheimers sjukdom i frånvaro av apolipoprotein E4-alleler (ApoE4) , men har ingen effekt hos ApoE4-bärare. En annan nyare hypotes är att högre nivåer av ACE kan förhindra Alzheimers. Det antas att ACE kan bryta ned beta-amyloid i hjärnans blodkärl och därför hjälpa till att förhindra sjukdomens utveckling.
En negativ korrelation mellan ACE1 D-allelen frekvens och förekomsten och mortaliteten i COVID-19 har fastställts.
Patologi
- Förhöjda nivåer av ACE finns också vid sarkoidos och används för att diagnostisera och övervaka denna sjukdom. Förhöjda nivåer av ACE finns också vid spetälska , hypertyreoidism , akut hepatit , primär gallcirros , diabetes mellitus , multipelt myelom , artros , amyloidos , Gauchers sjukdom , pneumokonios , histoplasmos och miliär tuberkulos . Det noteras också hos vissa patienter med omfattande plackpsoriasis.
- Serumnivåerna minskar vid njursjukdom , obstruktiv lungsjukdom och hypotyreos .
Påverkan på atletisk prestation
Den angiotensinomvandlande enzymgenen har mer än 160 polymorfismer beskrivna från och med 2018.
Studier har visat att olika genotyper av angiotensinkonverterande enzym kan leda till varierande inflytande på atletisk prestanda.
Rs1799752 I/D polymorfism består antingen av en insättning (I) eller frånvaro (D) av en 287 baspar alaninsekvens i intron 16 i genen. DD -genotypen associeras med högre plasmanivåer av ACE -proteinet, DI -genotypen med mellanliggande nivåer och II med lägre nivåer. Under fysisk träning, på grund av högre nivåer av ACE för D-allelbärare, därmed högre kapacitet att producera angiotensin II, kommer blodtrycket att öka snabbare än för I-allelbärare. Detta resulterar i en lägre maximal puls och lägre maximal syreupptagning (VO 2max ). Därför har D-allelbärare en 10% ökad risk för hjärt-kärlsjukdomar. Vidare är D-allelen associerad med en större ökning av vänster kammartillväxt som svar på träning jämfört med I-allelen. Å andra sidan uppvisar I-allelbärare vanligtvis en ökad maximal puls på grund av lägre ACE-nivåer, högre maximalt syreupptag och visar därför en förbättrad uthållighetsprestanda. I -allelen återfinns med ökad frekvens hos elitdistanslöpare, roddare och cyklister. Kortdistanssimmare visar en ökad frekvens av D-allelen, eftersom deras disciplin är mer beroende av styrka än uthållighet.
Se även
- ACE -hämmare
- Angiotensin-konverterande enzym 2 (ACE2)
- Hypotensiv transfusionsreaktion
- Renin -angiotensinsystem
Referenser
Vidare läsning
- Niu T, Chen X, Xu X (2002). "Angiotensin -konverterande enzymgeninsättning/deletionspolymorfism och kardiovaskulär sjukdom: terapeutiska konsekvenser". Droger . 62 (7): 977–93. doi : 10.2165/00003495-200262070-00001 . PMID 11985486 . S2CID 46986772 .
- Roĭtberg GE, Tikhonravov AV, Dorosh ZV (2004). "[Rollen av angiotensin-konverterande enzymgenpolymorfism i utvecklingen av metaboliskt syndrom]". Terapevticheskiĭ Arkhiv . 75 (12): 72–7. PMID 14959477 .
- Vynohradova SV (2005). "[Rollen av angiotensin-konverterande enzymgen I/D-polymorfism vid utveckling av metaboliska störningar hos patienter med kardiovaskulär patologi]". T︠S︡itologii︠a︡ I Genetika . 39 (1): 63–70. PMID 16018179 .
- König S, Luger TA, Scholzen TE (okt 2006). "Övervakning av neuropeptidspecifika proteaser: behandling av proopiomelanokortinpeptiderna adrenokortikotropin och alfa-melanocytstimulerande hormon i huden" . Experimentell dermatologi . 15 (10): 751–61. doi : 10.1111/j.1600-0625.2006.00472.x . PMID 16984256 . S2CID 32034934 .
- Sabbagh AS, Otrock ZK, Mahfoud ZR, Zaatari GS, Mahfouz RA, et al. (Mars 2007). "Angiotensin-konverterande enzymgenpolymorfism och allelfrekvenser i den libanesiska befolkningen: prevalens och granskning av litteraturen". Molekylärbiologiska rapporter . 34 (1): 47–52. doi : 10.1007/s11033-006-9013-y . PMID 17103020 . S2CID 9939390 .
- Castellon R, Hamdi HK (2007). "Demystifiering av ACE -polymorfismen: från genetik till biologi". Nuvarande läkemedelsdesign . 13 (12): 1191–8. doi : 10.2174/138161207780618902 . PMID 17504229 .
- Lazartigues E, Feng Y, Lavoie JL (2007). "De två ansiktena i vävnaden renin -angiotensinsystem: implikation vid hjärt -kärlsjukdomar". Nuvarande läkemedelsdesign . 13 (12): 1231–45. doi : 10.2174/138161207780618911 . PMID 17504232 .
externa länkar
- Proteopedia Angiotensin-converting_enzyme- den angiotensin-konverterande enzymstrukturen i interaktiv 3D
- Angiotensin+omvandling+enzym vid US National Library of Medicine Medical Subject Headings (MeSH)
- Plats för mänsklig ACE -genom och ACE -geninformation i UCSC -genomsökaren .