Aluminiumhydroxid - Aluminium hydroxide
|
|

|
|
| Namn | |
|---|---|
|
Föredraget IUPAC -namn
Aluminiumhydroxid |
|
|
Systematiskt IUPAC -namn
Aluminium (3+) trioxidanid |
|
| Andra namn
Alumininsyra
Aluminiumhydroxid |
|
| Identifierare | |
|
3D -modell ( JSmol )
|
|
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.040.433 |
| KEGG | |
|
PubChem CID
|
|
| RTECS -nummer | |
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
| Egenskaper | |
| Al (OH) 3 | |
| Molmassa | 78,00 g/mol |
| Utseende | Vitt amorft pulver |
| Densitet | 2,42 g / cm 3 , fast substans |
| Smältpunkt | 300 ° C (572 ° F; 573 K) |
| 0,0001 g/100 ml | |
|
Löslighetsprodukt ( K sp )
|
3 × 10 −34 |
| Löslighet | löslig i syror och alkalier |
| Surhet (p K a ) | > 7 |
| Isoelektrisk punkt | 7.7 |
| Termokemi | |
|
Std entalpi för
bildning (Δ f H ⦵ 298 ) |
−1277 kJ · mol −1 |
| Farmakologi | |
| A02AB01 ( WHO ) | |
| Faror | |
| Säkerhetsdatablad | Extern datablad |
| GHS -piktogram |

|
| H319 , H335 | |
| P264 , P261 , P280 , P271 , P312 , P304+340 , P305+351+338 , P337+313 | |
| NFPA 704 (eldiamant) | |
| Flampunkt | Ej brandfarligt |
| Dödlig dos eller koncentration (LD, LC): | |
|
LD 50 ( median dos )
|
> 5000 mg/kg (råtta, oral) |
| Relaterade föreningar | |
|
Andra anjoner
|
Ingen |
|
Relaterade föreningar
|
Natriumoxid , aluminiumoxidhydroxid |
|
Om inte annat anges, ges data för material i deras standardtillstånd (vid 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referenser | |
Aluminiumhydroxid , Al (OH) 3 , finns i naturen som mineralen gibbsit (även känd som hydrargillit) och dess tre mycket sällsyntare polymorfer : bayerit, doyleit och nordstrandit. Aluminiumhydroxid är amfoter , det vill säga har både basiska och sura egenskaper. Nära besläktade är aluminiumoxid-hydroxid , AIO (OH), och aluminiumoxid eller aluminiumoxid (Al 2 O 3 ), varav den senare är också amfotera. Dessa föreningar tillsammans är huvudkomponenterna i aluminiummalm bauxit .
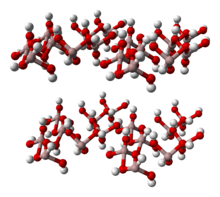
Strukturera
Al (OH) 3 är uppbyggt av dubbla lager av hydroxylgrupper med aluminiumjoner som upptar två tredjedelar av de oktaedriska hålen mellan de två lagren. Fyra polymorfer känns igen. Alla har lager av oktaedriska aluminiumhydroxid -enheter, med vätebindningar mellan lagren. Polymorferna skiljer sig åt när det gäller stapling av skikten. Alla former av Al (OH) 3 -kristaller är sexkantiga:
- gibbsite är också känd som γ-Al (OH) 3 eller α-Al (OH) 3
- bayerit är också känt som a-Al (OH) 3 eller β-aluminiumoxid-trihydrat
- nordstrandite är också känd som Al (OH) 3
- doyleit
Hydrargillit , en gång tänkt att vara aluminiumhydroxid, är ett aluminiumfosfat . Ändå hänvisar både gibbsit och hydrargillit till samma polymorfism av aluminiumhydroxid, med gibbsit som oftast används i USA och hydrargillit som används oftare i Europa. Hydrargillit är uppkallat efter de grekiska orden för vatten ( hydra ) och lera ( argyller ).
Egenskaper
Aluminiumhydroxid är amfotärt . I syra fungerar det som en Brønsted – Lowry -bas . Det neutraliserar syran och ger ett salt:
- 3 HCl + Al (OH) 3 → AlCl 3 + 3 H 2 O
I baser fungerar den som en Lewis -syra genom att binda hydroxidjoner:
- Al (OH) 3 + OH - → Al (OH) 4 -
Produktion

Nästan all aluminiumhydroxid som används kommersiellt tillverkas med Bayer -processen, vilket innebär att bauxit löses i natriumhydroxid vid temperaturer upp till 270 ° C (518 ° F). Det fasta avfallet, bauxitutmatningar , avlägsnas och aluminiumhydroxid fälls ut från den återstående lösningen av natriumaluminat . Denna aluminiumhydroxid kan omvandlas till aluminiumoxid eller aluminiumoxid genom kalcinering .
Återstoden eller bauxitutsläpp , som mestadels är järnoxid, är mycket frätande på grund av kvarvarande natriumhydroxid. Det lagrades historiskt i laguner; detta ledde till Ajka -aluminiumoxidfabrikolyckan 2010 i Ungern, där en damm sprack ledde till att nio personer drunknade. Ytterligare 122 sökte behandling för kemiska brännskador. Leran förorenade 40 kvadratkilometer mark och nådde Donau . Medan leran ansågs giftfri på grund av låga halter av tungmetaller, hade den tillhörande uppslamningen ett pH på 13.
Användningsområden
Brandskyddsmedel
Aluminiumhydroxid kan också användas som brandhämmande fyllmedel för polymerapplikationer. Det är valt för dessa applikationer eftersom det är färglöst (som de flesta polymerer), billigt och har bra brandhämmande egenskaper. Magnesiumhydroxid och blandningar av huntit och hydromagnesit används på samma sätt. Det sönderdelas vid cirka 180 ° C (356 ° F), absorberar en betydande mängd värme i processen och avger vattenånga. Förutom att bete sig som en brandskyddsmedel är den mycket effektiv som rökdämpare i ett stort antal polymerer, särskilt i polyestrar, akryl, etylenvinylacetat, epoxier, PVC och gummi.
Föregångare till Al -föreningar
Aluminiumhydroxid är ett matarmaterial för framställning av andra aluminiumföreningar: specialitet kalcinerade aluminiumoxider, aluminiumsulfat , polyaluminiumklorid, aluminiumklorid , zeoliter , natrium-aluminat , aktiverad aluminiumoxid, och aluminiumnitrat .
Nyutfälld aluminiumhydroxid bildar geler , som är grunden för applicering av aluminiumsalter som flockmedel vid vattenrening. Denna gel kristalliserar med tiden. Aluminiumhydroxidgeler kan dehydreras (t.ex. med hjälp av vattenblandbara icke-vattenhaltiga lösningsmedel som etanol ) för att bilda ett amorft aluminiumhydroxidpulver som är lättlösligt i syror. Uppvärmning omvandlar det till aktiverade aluminiumoxider, som används som torkmedel , adsorberande vid gasrening och katalysatorstöd .
Farmaceutisk
Under det generiska namnet "algeldrat" används aluminiumhydroxid som antacida hos människor och djur (främst katter och hundar). Det är att föredra framför andra alternativ såsom natriumbikarbonat eftersom Al (OH) 3 , som är olösligt, inte ökar pH i magen över 7 och därför inte utlöser utsöndring av överskott av syra i magen. Varumärken inkluderar Alu-Cap, Aludrox, Gaviscon eller Pepsamar. Det reagerar med överskott av syra i magen, vilket minskar surheten i maginnehållet, vilket kan lindra symtomen på sår , halsbränna eller dyspepsi . Sådana produkter kan orsaka förstoppning , eftersom aluminiumjonerna hämmar sammandragningar av glatta muskelceller i mag -tarmkanalen, saktar ner peristaltiken och förlänger den tid som krävs för avföring att passera genom tjocktarmen . Vissa sådana produkter är formulerade för att minimera sådana effekter genom att inkludera lika stora koncentrationer av magnesiumhydroxid eller magnesiumkarbonat , som har motviktande laxerande effekter.
Denna förening används också för att kontrollera hyperfosfatemi (förhöjda fosfat- eller fosforhalter i blodet) hos människor och djur som lider av njursvikt. Normalt filtrerar njurarna överflödigt fosfat ur blodet, men njursvikt kan orsaka att fosfat ackumuleras. Aluminiumsaltet vid förtäring binder till fosfat i tarmarna och minskar mängden fosfor som kan absorberas.
Utfälld aluminiumhydroxid ingår som adjuvans i vissa vacciner (t.ex. mjältbrandvaccin ). Ett av de välkända varumärkena för aluminiumhydroxidadjuvans är Alhydrogel, tillverkat av Brenntag Biosector. Eftersom det absorberar protein bra fungerar det också för att stabilisera vacciner genom att förhindra att proteinerna i vaccinet faller ut eller fastnar på behållarens väggar under lagring. Aluminiumhydroxid kallas ibland " alun ", en term som i allmänhet är reserverad för ett av flera sulfater.
Vaccinformuleringar som innehåller aluminiumhydroxid stimulerar immunsystemet genom att inducera frisättning av urinsyra , en immunologisk farosignal . Detta lockar starkt vissa typer av monocyter som differentieras till dendritiska celler . De dendritiska cellerna tar upp antigenet, bär det till lymfkörtlar och stimulerar T -celler och B -celler . Det verkar bidra till induktion av ett bra Th2 -svar, så det är användbart för att immunisera mot patogener som blockeras av antikroppar. Det har dock liten förmåga att stimulera cell (Th1) immunsvar, som är viktiga för skydd mot många patogener, och inte heller är det bra när antigenet är peptid baserad.
Säkerhet
På 1960- och 1970 -talen spekulerades det i att aluminium var relaterat till olika neurologiska störningar , inklusive Alzheimers sjukdom . Sedan dess har flera epidemiologiska studier inte funnit någon koppling mellan exponering för miljö eller svalt aluminium och neurologiska störningar, även om injicerat aluminium inte tittades på i dessa studier.
Referenser
externa länkar
- Internationellt kemikaliesäkerhetskort 0373
- "Vissa egenskaper hos aluminiumhydroxid utfälldes i närvaro av leror", Soil Research Institute, RC Turner, Department of Agriculture, Ottawa
- Effekt av åldrande på egenskaper hos polynukleära hydroxialuminiumkatjoner
- En andra art av polynukleär hydroxialuminiumkatjon, dess bildning och några av dess egenskaper

