Fenylgrupp - Phenyl group
I organisk kemi , den fenylgrupp , eller fenylring , är en cyklisk grupp av atomer med formeln C 6 H 5 . Fenylgrupper är nära besläktade med bensen och kan ses som en bensenring, minus ett väte, som kan ersättas med något annat element eller förening för att fungera som en funktionell grupp . Fenylgrupper har sex kolatomer bundna samman i en sexkantig plan ring, varav fem är bundna till enskilda väteatomer, med det återstående kolet bundet till en substituent . Fenylgrupper är vanliga inom organisk kemi . Även om de ofta avbildas med alternerande dubbel- och enkelbindningar, är fenylgrupper kemiskt aromatiska och har lika bindningslängder mellan kolatomer i ringen.
Nomenklatur
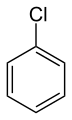
Vanligtvis är en "fenylgrupp" synonymt med C 6 H 5 - och representeras av symbolen Ph eller, archaically, Φ . Bensen betecknas ibland som PhH. Fenylgrupper är i allmänhet bundna till andra atomer eller grupper. Exempelvis trifenylmetan (Ph 3 CH) har tre fenylgrupper bundna till samma kol centrum. Många eller till och med de flesta fenylföreningar beskrivs inte med termen "fenyl". Exempelvis klorderivatet C 6 H 5 är Cl normalt kallas klorbensen , även om det skulle kunna kallas fenyl klorid. I särskilda (och sällsynta) fall, är isolerade fenylgrupper upptäckt: fenyl- anjon (C 6 H 5 - ), fenylen katjonen (C 6 H 5 + ) och fenyl -radikal (C 6 H 5 • ).
Fastän Ph och fenyl unikt betecknar C 6 H 5 , även substituerade derivat beskrivs som använder fenyl-terminologi. Till exempel, O 2 NC 6 H 4 är nitrofenyl, och F 5 C 6 är pentafluorfenyl. Monosubstituerade fenylgrupper (det vill säga disubstituerade bensener) är associerade med elektrofila aromatiska substitutionsreaktioner och produkterna följer arensubstitutionsmönstret . Så, en given substituerad fenylförening har tre isomerer, orto (1,2-disubstitution), meta (1,3-disubstitution) och para (1,4-disubstitution). En disubstituerad fenylförening (trisubstituerad bensen) kan exempelvis vara 1,3,5-trisubstituerad eller 1,2,3-trisubstituerad. Högre substitutionsgrader, av vilka pentafluorfenylgruppen är ett exempel, existerar och namnges enligt IUPAC-nomenklaturen.
Etymologi
Fenyl härrör från det franska ordet phényle , som i sin tur härstammar från grekiska φαίνω ( phaino ), "glänsande", eftersom de första namngivna fenylföreningarna var biprodukter för framställning och raffinering av olika gaser som användes för belysning . Enligt McMurry, "Ordet härstammar från den grekiska feno (" Jag bär ljus "), till minne av upptäckten av bensen av Michael Faraday 1825 från den oljiga återstoden som lämnats av den lysande gas som används i Londons gatlyktor."
Struktur, bindning och karakterisering
Fenylföreningar är härledda från bensen (C 6 H 6 ), åtminstone begreppsmässigt och ofta i termer av deras produktion. När det gäller dess elektroniska egenskaper är fenylgruppen relaterad till en vinylgrupp . Det anses allmänt vara en induktivt tillbakadragande grupp (- I ) på grund av den högre elektronegativiteten hos sp 2 kolatomer, och en resonansgivande grupp (+ M ), på grund av dess π-systemets förmåga att donera elektrontäthet när konjugering är möjlig . Fenylgruppen är hydrofob . Fenylgrupper tenderar att motstå oxidation och reduktion. Fenylgrupper (som alla aromatiska föreningar) har förbättrad stabilitet jämfört med ekvivalent bindning i alifatiska (icke-aromatiska) grupper. Denna ökade stabilitet beror på de unika egenskaperna hos aromatiska molekylära orbitaler .
Bindningslängderna mellan kolatomer i en fenylgrupp är ungefär 1,4 Å .
I en H- NMR -spektroskopi, protoner i en fenylgrupp har typiskt kemiska skift runt 7,27 ppm. Dessa kemiska förändringar påverkas av aromatisk ringström och kan förändras beroende på substituenter.
Förberedelse, förekomst och applikationer
Fenylgrupper introduceras vanligtvis med användning av reagens som beter sig som källor till fenylanjonen eller fenylkatjonen. Representativa reagens innefattar fenyllitium (C 6 H 5 Li) och fenylmagnesiumbromid (C 6 H 5 MgBr). Elektrofiler attackerar bensen för att ge fenylderivat:
- C 6 H 6 + E + → C 6 H 5 E + H +
där E + (de "elektrofil") = Cl + , NO 2 + , SO 3 . Dessa reaktioner kallas elektrofila aromatiska substitutioner .
- Representativa föreningar innehållande fenylgrupper
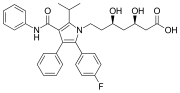
Atorvastatin (Lipitor) , ett blockbuster-läkemedel med två fenyl- och en p- fluorfenylgrupper. Det används för att sänka kolesterol hos personer med hyperkolesterolemi .
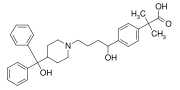
Fexofenadin (Allegra, Telfast) , en annan blockbuster läkemedel, som har en difenylmetylgrupp samt en p - fenylen- (Ci- 6 H 4 ) grupp. Det är en antihistamin som används för att behandla allergier .
Fenylalanin , en vanlig aminosyra.
Bifenyl , bestående av två fenylgrupper. De två ringarna brukar inte vara i samma plan.
Klorbensen (eller fenylklorid), ett lösningsmedel.
Fenylgrupper finns i många organiska föreningar, både naturliga och syntetiska (se figur). Vanligast bland naturliga produkter är aminosyran fenylalanin , som innehåller en fenylgrupp. En viktig produkt från den petrokemiska industrin är " BTX " bestående av bensen, toluen och xylen - som alla utgör byggstenar för fenylföreningar. Den polymer polystyren är härledd från en fenyl-innehållande monomer och owes dess egenskaper till den styvhet och hydrofobicitet av fenylgrupperna. Många läkemedel och många föroreningar innehåller fenylringar. En av de enklaste fenyl-innehållande föreningar är fenol , C 6 H 5 OH. Det sägs ofta att resonansstabiliteten av fenol gör den till en starkare syra än den av alifatiska alkoholer såsom etanol ( p K a = 10 vs. 16-18). Emellertid, är ett betydande bidrag desto större elektronegativitet av sp två alfa-kolet i fenol jämfört med sp tre alfa-kolet i alifatiska alkoholer.
Referenser
externa länkar
-
 Media relaterade till Phenyl-gruppen på Wikimedia Commons
Media relaterade till Phenyl-gruppen på Wikimedia Commons