Paramyxoviridae -Paramyxoviridae
| Paramyxoviridae | |
|---|---|

|
|
| CD- virusvirus och organisation av genomet | |
|
Virusklassificering |
|
| (oklassificerad): | Virus |
| Rike : | Riboviria |
| Rike: | Orthornavirae |
| Provins: | Negarnaviricota |
| Klass: | Monjiviricetes |
| Ordning: | Mononegavirales |
| Familj: | Paramyxoviridae |
| Underfamiljer | |
Paramyxoviridae (från grekiska para- "vid sidan av" och myxa " slem ") är en familj av negativsträngade RNA-virus i ordningen Mononegavirales . Ryggradsdjur fungerar som naturliga värdar. Sjukdomar i samband med denna familj inkluderar mässling , påssjuka och luftvägsinfektioner . Familjen har fyra underfamiljer, 17 släktingar och 78 arter, varav tre släktingar inte tilldelats en underfamilj.
Strukturera
Virioner är omslutna och kan vara sfäriska eller pleomorfa och kunna producera trådformiga virioner. Diametern är cirka 150 nm. Genomerna är linjära, cirka 15 kb långa. Fusionsproteiner och fästproteiner visas som spikar på virionsytan. Matrixproteiner inuti kuvertet stabiliserar virusstrukturen. Nukleokapsidkärnan består av genomiskt RNA, nukleokapsidproteiner, fosfoproteiner och polymerasproteiner.
Genom
Den genomet är nonsegmented, negativ-sense-RNA, 15-19 kilobaser i längd, och innehåller sex till 10 gener. Extracistronic (icke-kodande) regioner inkluderar:
- En 3'-ledarsekvens, 50 nukleotider lång, som fungerar som en transkriptionspromotor .
- En 5'-trailersekvens, 50–161 nukleotider lång
- Intergenomiska regioner mellan varje gen , som är tre nukleotider långa för morbillivirus, respirovirus och henipavirus, och variabel längd (en-56 nukleotider) för rubulavirus.
Varje gen innehåller transkriptionsstart / stoppsignaler i början och slutet, som transkriberas som en del av genen.
Gensekvensen i genomet bevaras över hela familjen på grund av ett fenomen som kallas transkriptionell polaritet (se Mononegavirales ) där gener närmast 3'-änden av genomet transkriberas i större överflöd än de mot 5'-änden. Detta är ett resultat av genomets struktur. Efter att varje gen har transkriberats pausar det RNA-beroende RNA-polymeraset för att frigöra det nya mRNA när det möter en intergen sekvens. När RNA-polymeras pausas finns det en chans att det kommer att dissocieras från RNA-genomet. Om den dissocieras måste den komma in igen genomet i ledarsekvensen snarare än att fortsätta att transkribera genomets längd. Resultatet är att ju längre nedströms generna kommer från ledarsekvensen, desto mindre transkriberas de av RNA-polymeras.
Bevis för en enda promotormodell verifierades när virus exponerades för UV-ljus. UV-strålning kan orsaka dimerisering av RNA, vilket förhindrar transkription av RNA-polymeras. Om virusgenomet följer en multipel promotormodell bör nivån inhibering av transkription korrelera med längden på RNA-genen. Genomet beskrivs emellertid bäst av en enda promotormodell. När paramyxovirusgenomet exponerades för UV-ljus var nivån av hämning av transkription proportionell mot avståndet från ledarsekvensen. Det vill säga ju längre genen är från ledarsekvensen, desto större är chansen att RNA-dimerisering hämmar RNA-polymeras.
Viruset utnyttjar den enda promotormodellen genom att generna ordnas i relativ proteinordning som behövs för framgångsrik infektion. Exempelvis behövs nukleokapsidprotein, N, i större mängder än RNA-polymeras, L.
Virus i Paramyxoviridae- familjen är också antigeniskt stabila, vilket innebär att glykoproteinerna på virusen överensstämmer mellan olika stammar av samma typ. Två orsaker till detta fenomen framställs: Den första är att genomet är icke-segmenterat och kan således inte genomgå genetisk omklassificering . För att denna process ska inträffa krävs segment som omplacering när segment från olika stammar blandas för att skapa en ny stam. Utan några segment kan ingenting blandas med varandra, så ingen antigenförskjutning sker. Den andra anledningen avser tanken på antigen drift . Eftersom RNA-beroende RNA-polymeras inte har en felkontrollfunktion, görs många mutationer när RNA behandlas. Dessa mutationer byggs upp och så småningom skapas nya stammar. På grund av detta koncept skulle man förvänta sig att paramyxovirus inte borde vara antigeniskt stabila; emellertid ses motsatsen vara sant. Huvudhypotesen bakom varför virusen är antigeniskt stabila är att varje protein och aminosyra har en viktig funktion. Således skulle varje mutation leda till en minskning eller total förlust av funktion, vilket i sin tur skulle få det nya viruset att vara mindre effektivt. Dessa virus skulle inte kunna överleva så länge jämfört med de mer virulenta stammarna, och så skulle de dö ut.
Många paramyxovirusgenom följer "regeln om sex" . Den totala längden på genomet är nästan alltid en multipel av sex. Detta beror troligen på fördelen med att allt RNA är bundet av N-protein (eftersom N binder hexamerer av RNA). Om RNA lämnas exponerat replikeras inte viruset effektivt. Gensekvensen är:
- Nukleokapsid - fosfoprotein - matris - fusion - bindning - stort (polymeras)
Proteiner
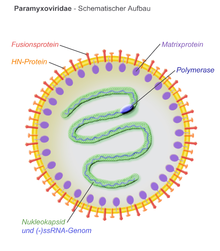
- N - nukleokapsidproteinet associeras med genomiskt RNA (en molekyl per hexamer) och skyddar RNA från nukleasdigerering
- P - fosfoproteinet binder till N- och L-proteinerna och utgör en del av RNA-polymeraskomplexet
- M - matrisproteinet samlas mellan höljet och nukleokapsidkärnan, det organiserar och upprätthåller virionsstrukturen
- F - fusionsproteinet skjuter ut från kuvertytan som en trimer och förmedlar cellinträde genom att inducera fusion mellan viralhöljet och cellmembranet genom klass I-fusion. En av de definierande egenskaperna hos familjemedlemmarna Paramyxoviridae är kravet på ett neutralt pH för fusogen aktivitet.
- H / HN / G - cellbindningsproteinerna spänner över viralhöljet och skjuter ut från ytan som spikar. De binder till proteiner på ytan av målceller för att underlätta cellinträde. Proteiner betecknas H ( hemagglutinin ) för morbillivirus eftersom de har hemagglutinationsaktivitet , observerade som en förmåga att få röda blodkroppar att klumpa sig i laboratorietester. HN ( hemagglutinin-neuraminidas ) fästproteiner förekommer i respirovirus, rubulavirus och avulavirus. Dessa har både hemagglutination och neuraminidasaktivitet , som klyver sialinsyra på cellytan, vilket förhindrar viruspartiklar från att återfästas till tidigare infekterade celler. Fästproteiner med varken hemagglutination eller neuraminidasaktivitet betecknas G ( glykoprotein ). Dessa förekommer i henipavirus.
- L - det stora proteinet är den katalytiska underenheten av RNA-beroende RNA-polymeras (RDRP)
- Tillbehörsproteiner - en mekanism som kallas RNA-redigering (se Mononegavirales ) gör att flera proteiner kan produceras från P-genen. Dessa är inte nödvändiga för replikering men kan hjälpa till att överleva in vitro eller kan vara inblandade i att reglera övergången från mRNA-syntes till antigenomsyntes .
Livscykel

Viral replikation är cytoplasmatisk . Inträde i värdcellen uppnås genom viral bindning till värdcellen. Replikering följer den negativsträngade RNA-virusreplikationsmodellen. Transkription av negativsträngat RNA-virus, med användning av polymerasstammning, är transkriptionsmetoden. Översättningen sker genom läckande scanning, ribosomal shunting och RNA-terminering-återinitiering. Viruset lämnar värdcellen genom att spira. Mänskliga, ryggradsdjur och fåglar fungerar som de naturliga värdarna. Överföringsvägen är luftburna partiklar.
Den Paramyxoviridae kan undergå mRNA redigering, som producerar olika proteiner från samma mRNA-transkript genom att halka tillbaka en bas för att läsa av i en annan öppen läsram ( ORF ) på grund av närvaron av sekundära strukturer såsom pseudoknut. Paramyxoviridae genomgår också translationell stamning för att producera poly (A) svansen i slutet av mRNA-transkript genom att upprepade gånger flytta tillbaka en nukleotid i taget i slutet av RNA-mallen.
Taxonomi
Familj: Paramyxoviridae
- Underfamilj: Avulavirinae , som innehåller tre släkt och 22 arter
- Underfamilj: Metaparamyxovirinae , som innehåller ett släkt och en art
- Underfamilj: Orthoparamyxovirinae , som innehåller åtta släkt och 34 arter
- Underfamilj: Rubulavirinae , som innehåller två släkt och 18 arter
- Otilldelade släkter:
Patogena paramyxovirus
Ett antal viktiga sjukdomar hos människor orsakas av paramyxovirus. Dessa inkluderar påssjuka och mässling som orsakade cirka 733 000 dödsfall år 2000.
De humana parainfluensavirusen (HPIV) är de näst vanligaste orsakerna till luftvägssjukdom hos spädbarn och barn. Det finns fyra typer av HPIV, kända som HPIV-1, HPIV-2, HPIV-3 och HPIV-4. HPIV-1 och HPIV-2 kan orsaka förkylningsliknande symtom, tillsammans med kryp hos barn. HPIV-3 är associerad med bronkiolit , bronkit och lunginflammation . HPIV-4 är mindre vanligt än de andra typerna och är känt för att orsaka mild till svår luftvägssjukdom.
Paramyxovirus är också ansvariga för en rad sjukdomar hos andra djurarter, till exempel hundsjuka virus ( hundar ), phocine distemper virus ( sälar ), cetacean morbillivirus ( delfiner och tumlare ), Newcastlesjuka virus ( fåglar ) och rinderpestvirus ( nötkreatur) ). Vissa paramyxovirus, såsom henipavirus, är zoonotiska patogener, som förekommer naturligt hos en djurvärd, men som också kan infektera människor.
Hendra virus (HEV) och Nipah virus (NIV) i släktet Henipavirus har dykt upp hos människor och boskap i Australien och sydöstra Asien . Båda virusen är smittsamma , mycket virulenta och kan infektera ett antal däggdjursarter och orsaka potentiellt dödlig sjukdom. På grund av avsaknaden av ett licensierat vaccin eller antivirala terapier betecknas HeV och NiV som biosäkerhetsnivå (BSL) 4- medel. Den genomiska strukturen för båda virusen är den för ett typiskt paramyxovirus.
Mångfald och evolution
Under de senaste decennierna har paramyxovirus upptäckts från mark-, volant- och vattenlevande djur, vilket visar ett stort värdområde och stor viral genetisk mångfald. I takt med att molekylär teknik utvecklas och virusövervakningsprogram implementeras ökar upptäckten av nya virus i denna grupp.
Utvecklingen av paramyxovirus diskuteras fortfarande. Med hjälp av pneumovirus (mononegaviral familj Pneumoviridae ) som en utgrupp kan paramyxovirus delas in i två klader: en bestående av avulavirus och rubulavirus och en bestående av respirovirus, henipavirus och morbillivirus. Inom den andra kladen verkar respirovirusen vara basalgruppen. Respirovirus-henipavirus-morbillivirus-kladen kan vara basal till avulavirus-rubulavirus-kladen.
Se även
Referenser
externa länkar
- ICTV-rapport: Paramyxoviridae
- Paramyxovirus (1998) - morfologi, genom, replikering, patogenes (särskild åtkomst krävs)
- "Hendra-viruset har ett växande släktträd" . CSIRO Paramyxovirus pressmeddelande . 2001. Arkiverat från originalet 2007-08-04.
- Djurvirus
- Paramyxoviridae Genomes Viral Bioinformatics Resource Center
- Viralzone : Paramyxoviridae
- Viruspatogendatabas och analysresurs (ViPR): Paramyxoviridae


