Tymocyt - Thymocyte
En tymocyt är en immuncell som finns i tymusen innan den genomgår omvandling till en T -cell . Thymocyter produceras som stamceller i benmärgen och når tymus via blodet . Thymopoiesis beskriver processen som gör tymocyter till mogna T -celler enligt antingen negativt eller positivt urval. Denna urvalsprocess är mycket viktig för att forma populationen av tymocyter till en perifer pool av T -celler som kan reagera på främmande patogener men förblir toleranta mot kroppens egna antigener. Positivt urval väljer celler som kan binda MHC klass I eller II molekyler med åtminstone en svag affinitet. Detta eliminerar (genom en process som kallas "död genom försummelse") de T-celler som skulle vara icke-funktionella på grund av oförmåga att binda MHC. Negativ selektion förstör tymocyter med hög affinitet för självpeptider eller MHC. Detta eliminerar celler som skulle rikta immunsvar mot självproteiner i periferin. Negativt urval är inte 100% effektivt, och vissa autoreaktiva T -celler flyr och släpps ut i cirkulationen. Ytterligare mekanismer för perifer tolerans finns för att tysta dessa celler, men om dessa misslyckas kan autoimmunitet uppstå.
Mognadsstadier
Tymocyter klassificeras i ett antal distinkta mognadsstadier baserade på uttryck av cellytamarkörer. Det tidigaste tymocytstadiet är det dubbla negativa steget (negativt för både CD4 och CD8), som på senare tid har beskrivits bättre som Lineage-negativt, och som kan delas in i fyra delsteg. Nästa stora etapp är det dubbla positiva steget (positivt för både CD4 och CD8). Det sista steget i mognad är det enda positiva steget (positivt för antingen CD4 eller CD8).
Hos möss
| Skede | Definierar ytmarkörer | Plats | Betydande händelser |
| Dubbel negativ 1 eller ETP (Early T lineage Progenitor) | Lineage- CD44 + CD25 - CD117 + | bark | Spridning, förlust av B och myeloida potentialer |
| Dubbel negativ 2 | Lineage-CD44+CD25+CD117+ | bark | - |
| Dubbel negativ 3 | Lineage-CD44-CD25+ | bark | TCR-beta-omorganisation, betaval |
| Dubbel negativ 4 | Lineage-CD44-CD25- | bark | - |
| Dubbel positivt | CD4 + CD8 + | bark | TCR-alfa-omorganisation, positivt urval, negativt urval |
| Singel positiv | CD4+CD8- eller CD4-CD8+ | märg | Negativt urval |
I människor
Hos människor finns cirkulerande CD34+ hematopoetiska stamceller ( HSC ) i benmärgen. De producerar föregångare till T -lymfocyter, som fröer thymus (därmed blir tymocyter) och differentieras under påverkan av Notch och dess ligander.
Tidiga, dubbla negativa tymocyter uttrycker (och kan identifieras med) CD2 , CD5 och CD7 . Under det dubbla negativa steget stannar CD34 -uttrycket och CD1 uttrycks. Uttryck av både CD4 och CD8 gör dem dubbla positiva och mognar till antingen CD4+ eller CD8+ celler.
Händelser under mognad
| typ: | funktionell (betaval) | funktionellt (positivt urval) | autoreaktiv (negativt urval) |
| plats: | bark | bark | cortex/medulla |
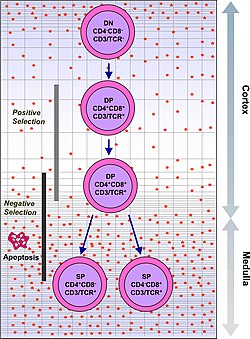 |
För att passera β-urvalskontrollen måste β-kedjan hos T-cellreceptorn som omordnas av tymocyten behålla de strukturella egenskaperna så att den kan presenteras på ytan av tymocyten med pre-TCRα. Detta eliminerar tymocyter med grova defekter som införs i T -cellreceptorn genom genarrangemang. |
För att bli positivt utvalda måste tymocyter interagera med flera cellytmolekyler, MHC , för att säkerställa reaktivitet och specificitet. Positivt urval väljer celler med en T -cellreceptor som kan binda MHC klass I eller II molekyler med åtminstone en svag affinitet. Detta eliminerar (genom en process som kallas "död genom försummelse") de T-celler som skulle vara icke-funktionella på grund av oförmåga att binda MHC. |
Negativt urval är den aktiva induktionen av apoptos i tymocyter med hög affinitet för självpeptider eller MHC. Detta eliminerar celler som skulle rikta immunsvar mot självproteiner i periferin. Negativt urval är inte 100% effektivt, vissa autoreaktiva T -celler slipper tymisk censur och släpps ut i cirkulationen. Ytterligare mekanismer för tolerans som är aktiva i periferin finns för att tysta dessa celler såsom anergi , borttagning och regulatoriska T -celler . Om dessa perifera toleransmekanismer också misslyckas kan autoimmunitet uppstå. |
Thymus bosätter sig
Thymocyter härstammar slutligen från hematopoetiska stamceller från benmärgen [se hematopoetisk stamcell , hematopoiesis ] som når tymus genom cirkulationen. Antalet förfäder som kommer in i thymus varje dag anses vara extremt litet. Vilka stamfäder som koloniserar thymus är därför okända. För närvarande föreslås Early Lymphoid Progenitors (ELP) att lösa thymus och är troligen föregångare till åtminstone några tymocyter. ELP är Lineage-CD44+ CD25-CD117+ och liknar därmed mycket ETP, de tidigaste föregångarna i thymus. Prekursorer går in i thymus vid kortikom-medullär korsning. Molekyler som är kända för att vara viktiga för tymusinträde inkluderar P- selectin (CD62P) och kemokinreceptorerna CCR7 och CCR9 .
Efter tymusinträde förökar sig stamfäder för att generera ETP -populationen. Detta steg följs av generering av DN2-tymocyter som migrerar från kortikomedullärkorsningen mot tymuskapseln. DN3 -tymocyter genereras vid den subkapselformiga zonen.
Förutom spridning sker differentiering och T -släktengagemang inom DN -tymocytpopulationen. Engagemang eller förlust av alternativa släktpotentialer (såsom myeloid-, B- och NK -släktpotentialer) är beroende av Notch -signalering och slutförs i DN3 -steget. Efter T-släktingens åtagande genomgår DN3-tymocyter β-selektion.
β-urval
T -cellers förmåga att känna igen främmande antigener medieras av T -cellreceptorn (TCR), som är ett ytprotein som kan känna igen korta proteinsekvenser ( peptider ) som presenteras på MHC . Syftet med tymocytutveckling är att producera mogna T -celler med en mängd olika funktionella T -cellreceptorer, genom processen för TCR -genarrangemang.
Till skillnad från de flesta gener, som har en stabil sekvens i varje cell som uttrycker dem, består T -cellreceptorn av en serie alternativa genfragment. För att skapa en funktionell T-cellreceptor använder de dubbla negativa tymocyterna en serie DNA-interagerande enzymer för att klippa DNA och föra samman separata genfragment. Resultatet av denna process är att varje T -cellreceptor har en annan sekvens på grund av olika val av genfragment och de fel som infördes under skärnings- och sammanfogningsprocessen (se avsnittet om V (D) J -rekombination för mer information om TCR -omläggning) . Den evolutionära fördelen med att ha ett stort antal unika T -cellreceptorer är att varje T -cell kan känna igen en annan peptid, vilket ger ett försvar mot snabbt utvecklande patogener.
TCR -omorganisation sker i två steg. Först omorganiseras TCRp -kedjan vid DN3 -steget i T -cellutvecklingen. TCRp-kedjan är ihopkopplad med pre-Tα för att generera pre-TCR. Den cellulära nackdelen i omorganisationsprocessen är att många av kombinationerna av T-cellreceptorgengenfragmenten är icke-funktionella. För att eliminera tymocyter som har gjort en icke-funktionell T-cellreceptor får endast celler som framgångsrikt har omorganiserat betakedjan för att producera en funktionell pre-TCR utvecklas bortom DN3-steget. Celler som misslyckas med att producera en funktionell pre-TCR elimineras genom apoptos . Denna process kallas beta-urvalskontrollpunkten. Framgångsrikt beta-urval kräver att TCRβ produceras, TCRβ kan para ihop med pre-Tα för att generera pre-TCR och att pre-TCR kan interagera på cellytan med TCR-signalproteinerna.
I p-selektionsstadiet på samma sätt som det mogna TCR, bildar pre-TCR också en immunologisk synaps. Även om pre-TCR och den peptidbundna MHC-interaktionen inte är nödvändiga för T-cellutveckling, spelar den en kritisk roll för att uppmuntra den förmånliga spridningen av celler vars pre-TCR kan binda själv-MHC.
Efter β-selektion tymocyter genererar CD4+ CD8+ dubbla positiva celler, som sedan genomgår TCRα omorganisation, vilket resulterar i fullständigt sammansatt TCR.
Positivt urval och släktengagemang
Tymocyter som passerar β-selektion uttrycker en T-cellreceptor som kan samlas på ytan. Många av dessa T-cellreceptorer kommer dock fortfarande att vara icke-funktionella på grund av oförmåga att binda MHC . Nästa stora steg i tymocytutvecklingen är positivt urval, för att bara behålla de tymocyter som har en T -cellreceptor som kan binda MHC. T -cellreceptorn kräver CD8 som en coreceptor för att binda till MHC klass I och CD4 som en coreceptor för att binda MHC klass II. I detta skede uppregulerar tymocyter både CD4 och CD8 och blir till dubbla positiva celler.
Dubbla positiva tymocyter som har en T -cellreceptor som kan binda MHC klass I eller klass II (även med svag affinitet) mottar signalering genom T -cellreceptorn. Tymocyter som har en T -cellreceptor som inte kan binda MHC klass I eller klass II genomgår apoptos . Vissa tymocyter kan rädda misslyckat positivt urval genom receptorredigering (omorganisation av den andra T -cellreceptorallelen för att producera en ny T -cellreceptor).
De dubbla positiva tymocyterna genomgår släktengagemang, mognar till en CD8+ T -cell (känner igen MHC klass I) eller en CD4+ T -cell (känner igen MHC klass II). Linjeåtagande sker i det sena stadiet av positivt urval och fungerar genom nedreglering av både CD4 och CD8 (reducerar signalen från T -cellreceptorn) och sedan endast uppreglering av CD4. Tymocyter som börjar ta emot signal igen är de som känner igen MHC klass II, och de blir CD4+ T -celler. Tymocyter som inte börjar ta emot signal igen är de som känner igen MHC klass I, och de nedreglerar CD4 och uppreglerar CD8 för att bli CD8+ T -celler. Båda dessa tymocyttyper är kända som enstaka positiva tymocyter.
Negativt urval
Framgång med positivt urval gör att tymocyten kan genomgå ett antal mognadsförändringar under övergången till en enda positiv T -cell. De enda positiva T -cellerna uppreglerar kemokinreceptorn CCR7, vilket orsakar migration från cortex till medulla. I detta skede involverar nyckelmognadsprocessen negativt urval, eliminering av autoreaktiva tymocyter.
Den viktigaste nackdelen med en genomläggningsprocess för T-cellreceptorer är att av en slump kommer vissa arrangemang av genfragment att skapa en T-cellreceptor som kan binda självpeptider presenterade på MHC klass I eller MHC klass II. Om T -celler som bär dessa T -cellreceptorer skulle komma in i periferin skulle de kunna aktivera ett immunsvar mot mig själv, vilket resulterar i autoimmunitet . Negativt urval är den process som utvecklats för att minska denna risk. Under negativ selektion induceras alla tymocyter med hög affinitet för bindning av självpeptider presenterade på MHC klass I eller klass II att uppreglera BCL2L11 , ett protein som driver apoptos. Celler som inte har hög affinitet för självantigener överlever negativt urval. I detta skede väljs också vissa celler ut för att bli regulatoriska T-celler , vanligtvis celler som har en mellanliggande affinitet för självpeptid.
Negativt urval kan inträffa i det dubbla positiva stadiet i cortex. Repertoaren av peptider i cortex är emellertid begränsad till de som uttrycks av epitelceller, och dubbla positiva celler är dåliga på att genomgå negativ selektion. Därför är den viktigaste platsen för negativt urval medulla, när cellerna är i det enda positiva stadiet. För att avlägsna tymocyter som är reaktiva mot perifera organ driver transkriptionsfaktorerna Aire och Fezf2 uttrycket av flera perifera antigener, såsom insulin, vilket resulterar i borttagning av celler specifika för dessa antigener. Detta gör att enstaka positiva tymocyter kan exponeras för en mer komplex uppsättning självantigener än vad som finns i cortex och tar därför bort mer effektivt de T-celler som är autoreaktiva.
Enstaka positiva tymocyter finns kvar i medulla i 1-2 veckor och undersöker självantigener för att testa för autoreaktivitet. Under denna tid genomgår de slutliga mognadsförändringar och lämnar sedan thymus med S1P och CCR7. Vid inträde i det perifera blodomloppet anses cellerna mogna T -celler, och inte tymocyter.
Negativt urval är inte 100% effektivt, vissa autoreaktiva T -celler slipper tymisk censur och släpps ut i cirkulationen. Ytterligare mekanismer för perifer tolerans som är aktiva i periferin finns för att tysta dessa celler såsom anergi , deletion och regulatoriska T -celler . Om dessa perifera toleransmekanismer också misslyckas kan autoimmunitet uppstå.
Thymustransplantation resulterar i att T-celler lärs att undvika att reagera med donatorantigener istället, och kan fortfarande reagera med många självantigener i kroppen. Autoimmun sjukdom är en frekvent komplikation efter tymustransplantation, som finns hos 42% av patienterna över 1 år efter transplantation. Detta förklaras dock delvis av att indikationen i sig, det vill säga fullständigt DiGeorge -syndrom (frånvaro av tymus), ökar risken för autoimmun sjukdom.
Cancer
Tymocyter som får onkogena mutationer som tillåter okontrollerad spridning kan bli tymiska lymfom .
Alternativa släktlinjer
Förutom klassiska αβ T -celler (vars utveckling är skisserad ovan) utvecklas ett antal andra T -linjer i thymus, inklusive γδ T -celler och Natural Killer T (NKT) -celler. Dessutom kan andra icke-T hematopoetiska linjer utvecklas i thymus, inklusive B-lymfocyter (B-celler), Natural Killer-lymfocyter (NK-celler).), Myeloidceller och dendritiska celler. Thymus är dock inte en källa till B-, NKC- eller myeloidutveckling (detta påstående är inte sant för alla B-celler eller NKC). Utvecklingen av dessa celler i thymus speglar den multi-potenta naturen hos hematopoetiska stamfäder som fröer thymus. Mogna B-celler och andra APC kan också hittas i medulla som bidrar till negativa selektionsprocesser.