Schwann cell - Schwann cell
| Schwann cell | |
|---|---|
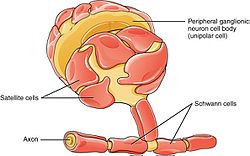 PNS har satellitceller och Schwann -celler.
| |
| Identifierare | |
| Maska | D012583 |
| FMA | 62121 |
| Anatomiska termer för neuroanatomi | |
Schwann -celler eller neurolemmocyter (uppkallad efter den tyska fysiologen Theodor Schwann ) är det huvudsakliga glia i det perifera nervsystemet (PNS). Glialceller fungerar för att stödja neuroner och i PNS, inkluderar också satellitceller , luktceller , enterisk glia och glia som finns vid sensoriska nervändar, såsom Pacinian corpuscle . De två typerna av Schwann -celler är myeliniserande och icke -myeliniserande. Myeliniserande schwannceller linda runt axoner av motoriska och sensoriska neuroner för att bilda myelinskidan. Schwann -cellpromotorn är närvarande i nedströmsregion av den humana dystrofingenen som ger förkortat transkript som återigen syntetiseras på ett vävnadsspecifikt sätt.
Under utvecklingen av PNS styrs myeliniseringens regleringsmekanismer genom feedforward -växelverkan mellan specifika gener, som påverkar transkriptionella kaskader och formar de myeliniserade nervfibrernas morfologi.
Schwann-celler är involverade i många viktiga aspekter av perifer nerv biologi-ledning av nervimpulser längs axoner , nervutveckling och regenerering , trofiska stöd för neuroner , produktion av nerven extracellulär matris, modulering av neuromuskulär synaptisk aktivitet, och presentation av antigener till T -lymfocyter .
Charcot – Marie – Tooth sjukdom , Guillain – Barré syndrom (akut inflammatorisk demyeliniserande polyradikulopati typ), schwannomatos , kronisk inflammatorisk demyeliniserande polyneuropati och spetälska är alla neuropatier som involverar Schwann -celler.
Strukturera
| Schwann -celler lindade runt en axon |
|---|
Schwann -celler är en mängd olika glialceller som håller perifera nervfibrer (både myeliniserade och ommyeliniserade) vid liv. I myeliniserade axoner, Schwann-celler bildar myelinskidan. Höljet är inte kontinuerligt. Individuella myeliniserande Schwann-celler täcker cirka 1 mm av en axon-vilket motsvarar cirka 1000 Schwann-celler längs en 1 m längd av axonen. Klyftorna mellan intilliggande Schwann -celler kallas Ranviers noder .
9-O-Acetyl GD3 gangliosid är en acetylerad glykolipid som finns i cellmembranen i många typer av ryggradsdjurceller. Under perifer nervregenerering uttrycks 9-O-acetyl GD3 av Schwann-celler.
Fungera
Den vertebrat nervsystemet beroende av myelinskidan för isolering och som en metod för att minska membran kapacitans i axonet. Den aktionspotentialen hoppar från nod till nod, i en process som kallas saltatory ledning , vilket kan öka ledningshastighet upp till 10 gånger, utan en ökning av axonal diameter. I denna mening, Schwann-celler är de PNS s analoger av det centrala nervsystemet är oligodendrocyter . Men till skillnad från oligodendrocyter ger varje myeliniserande Schwann -cell isolering till endast en axon (se bild). Detta arrangemang tillåter saltatorisk ledning av åtgärdspotentialer med repropagation vid Ranviers noder. På detta sätt ökar myeliniseringen kraftigt ledningshastigheten och sparar energi.
Icke -myeliniserande Schwann -celler är involverade i underhåll av axoner och är avgörande för neuronal överlevnad. Vissa grupperar runt mindre axoner ( Extern bild här ) och bildar Remak -buntar .
Myeliniserande Schwann -celler börjar bilda myelinhöljet hos däggdjur under fosterutveckling och fungerar genom att spiralera runt axonen, ibland med så många som 100 varv. En välutvecklad Schwann-cell är formad som ett hoprullat pappersark med myelinlager mellan varje spole. Omslagets inre lager, som huvudsakligen är membranmaterial , bildar myelinhöljet, medan det yttersta lagret av kärnbildad cytoplasma bildar neurilemma . Endast en liten volym kvarvarande cytoplasma möjliggör kommunikation mellan de inre och yttre skikten. Detta ses histologiskt som Schmidt-Lantermann-inkreationen .
Regeneration
Schwann -celler är kända för sina roller för att stödja nervregenerering . Nerver i PNS består av många axoner myeliniserade av Schwann -celler. Om skador uppstår på en nerv hjälper Schwann -cellerna till matsmältningen av dess axoner ( fagocytos ). Efter denna process kan Schwann -cellerna styra regenerering genom att bilda en typ av tunnel som leder mot målneuronerna. Denna tunnel är känd som band av Büngner , ett styrspår för de regenererande axonerna, som beter sig som ett endoneuralt rör. Stubben på den skadade axonen kan gro, och de groddar som växer genom Schwann-cellens "tunnel" gör det med en hastighet av cirka 1 mm/dag under bra förhållanden. Hastigheten för regenerering minskar med tiden. Framgångsrika axoner kan därför återansluta till musklerna eller organen som de tidigare kontrollerade med hjälp av Schwann -celler, men specificiteten bibehålls inte och fel är vanliga, särskilt när långa avstånd är inblandade. På grund av deras förmåga att påverka regenerering av axoner har Schwann -celler också kopplats till förmånsmotorisk reinnervation . Om Schwann -celler hindras från att associera med axoner, dör axonerna. Regenererande axoner når inte något mål om inte Schwann -celler är där för att stödja dem och vägleda dem. De har visat sig ligga före tillväxtkottarna .
Schwann -celler är viktiga för upprätthållandet av friska axoner. De producerar en mängd olika faktorer, inklusive neurotrofiner , och överför också viktiga molekyler över till axoner.
Genetik
Schwann cellbildning
Sox10
SOX10 är en transkriptionsfaktor aktiv under embryonisk utveckling och rikligt med bevis tyder på att det är avgörande för generering av gliallinjer från stamcellceller. När SOX10 inaktiveras hos möss, utvecklas inte satellitglia och Schwann -cellprekursorer, även om neuroner genereras normalt utan problem. I avsaknad av SOX10 överlever neurala toppceller och är fria att generera neuroner, men glialspecifikationen blockeras. SOX10 kan påverka tidiga glialprekursorer att reagera på neuregulin 1 (se nedan).
Neuregulin 1
Neuregulin 1 (NRG1) verkar på ett antal sätt för att både främja bildandet och säkerställa överlevnad av omogna Schwann -celler. Under embryonal utveckling hämmar NRG1 bildandet av neuroner från neurala kamceller, i stället bidrar det till att neurala crestceller leds ner en väg till gliogenes. NRG1 -signalering är emellertid inte nödvändig för differentiering av glial från neuralkammen.
NRG1 spelar viktiga roller i utvecklingen av neurala vapenderivat. Det krävs för att neurala toppceller ska migrera förbi platsen för dorsala rotganglier för att hitta de ventrala regionerna för sympatisk gangliogenes. Det är också en väsentlig axon-härledd överlevnadsfaktor och en mitogen för Schwann-cellprekursorer. Det finns i dorsala rotganglion och motorneuroner vid den tidpunkt då Schwann -cellprekursorer börjar fylla ryggradsnerver och påverkar därför Schwann -cellens överlevnad. I embryonala nerver är transmembran III -isoform troligen den primära varianten av NRG1 som är ansvarig för överlevnadssignaler. Hos möss som saknar transmembran III -isoform elimineras så småningom Schwann -cellprekursorer från spinalnerver.
Bildning av myelinhölje
P0
Myelinprotein noll (P0) är en celladhesionsmolekyl som tillhör immunglobulinsuperfamiljen och är huvudkomponenten i perifert myelin och utgör över 50% av det totala proteinet i höljet. P0 har visat sig vara avgörande för bildandet av kompakt myelin, eftersom P0-nullmutanta (P0-) möss visade allvarligt avvikande perifer myelinisering. Även om myelinisering av stora kaliberaxoner initierades i P0-möss, var de resulterande myelinskikten mycket tunna och dåligt komprimerade. Oväntat visade P0-möss också degenerering av båda axonerna och deras myelinhöljen, vilket tyder på att P0 spelar en roll för att upprätthålla den strukturella integriteten för både myelinbildning och axon som det är associerat med. P0-möss utvecklade beteendemässiga underskott runt 2 veckors ålder när möss började visa tecken på lätt skakningar. Grov inkoordination uppstod också när djuren utvecklades, medan darrningar blev svårare och några äldre möss utvecklade krampaktiga beteenden. Trots mängden nedsatt motorbeteende sågs ingen förlamning hos dessa djur. P0 är också en viktig gen som uttrycks tidigt inom Schwann -celllinjen, uttryckt i Schwann -cellprekursorer efter att ha differentierats från migrerande neurala crestceller i det utvecklande embryot.
Krox-20
Flera viktiga transkriptionsfaktorer uttrycks och involveras också i olika utvecklingsstadier och förändrar funktionerna på Schwann -cellerna från ett omoget till moget tillstånd. En oumbärlig transkriptionsfaktor uttryckt under myeliniseringsprocessen är Krox-20. Det är en allmän zink-finger-transkriptionsfaktor och uttrycks i rombomererna 3 och 5.
Krox-20 anses vara en av huvudregulatorerna för PNS-myelinisering och är viktig för att driva transkription av specifika strukturproteiner i myelinet. Det har visat sig kontrollera en uppsättning gener som är ansvariga för att störa denna funktion i axonet som ändrar det från ett pro-myeliniserande till myeliniserande tillstånd. På detta sätt har det i Krox-20 dubbla knock-out-möss registrerats att segmentering av bakhjärnan påverkas liksom myelinisering av Schwann-cellassocierade axoner. Faktum är att hos dessa möss kan Schwann -cellerna inte utföra sin myelinisering ordentligt eftersom de bara sveper sina cytoplasmatiska processer ett och ett halvt varv runt axonen och trots att de fortfarande uttrycker den tidiga myelinmarkören saknas sena myelingenprodukter . Dessutom har nya studier också bevisat vikten av denna transkriptionsfaktor för att upprätthålla myeliniseringsfenotypen (och kräver samuttryck av Sox 10) eftersom dess inaktivering leder till dedifferentiering av Schwann-cellerna.
Klinisk signifikans
Charcot – Marie – Tooth sjukdom (CMT), Guillain – Barré syndrom (GBS, akut inflammatorisk demyeliniserande polyradikulopati typ), schwannomatos och kronisk inflammatorisk demyeliniserande polyneuropati (CIDP), spetälska och Zika Virus är alla neuropatier som involverar Schwann -celler.
Transplantation
Ett antal experimentella studier sedan 2001 har implanterat Schwann-celler i ett försök att inducera remyelinisering i multipelskleros -afflicted patienter. Under de senaste två decennierna har många studier visat positiva resultat och potential för Schwann -celltransplantation som en behandling för ryggmärgsskada, både för att underlätta återväxt och myelinisering av skadade CNS -axoner. Schwann celltransplantationer i kombination med andra terapier som kondroitinas ABC har också visat sig vara effektiva vid funktionell återhämtning från ryggmärgsskada.
Se även
- Elektrofysiologi
- Hodgkin – Huxley modell
- Mesaxon
- Neurotransmission
- Luktfrämjande cell
- Schwannoma
- Lista över mänskliga celltyper härledda från groddskikten
Referenser
externa länkar
- Diagram på clc.uc.edu
- Histologibild: 21301loa - Histology Learning System vid Boston University - "Cellens ultrastruktur: myeliniserad axon och Schwann -cell"
- Cellcentrerad databas - Schwann -cell


