Hemolytisk sjukdom hos nyfödda - Hemolytic disease of the newborn
| Hemolytisk sjukdom hos nyfödda | |
|---|---|
| Andra namn | HDN |
 | |
| Specialitet |
Pediatri , immunhematologi |
| Komplikationer | hjärtsvikt , splenomegali |
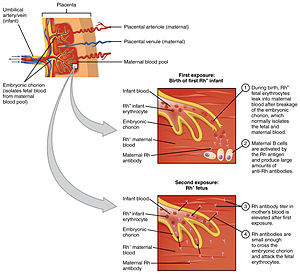
Hemolytisk sjukdom hos nyfödda , även känd som hemolytisk sjukdom hos foster och nyfödda , HDN , HDFN eller erytroblastos foetalis , är ett alloimmunt tillstånd som utvecklas hos ett foster vid eller runt födseln, när IgG -molekylerna (en av de fem huvudtyperna av antikroppar ) som produceras av modern passerar genom moderkakan . Bland dessa antikroppar finns några som angriper antigener på de röda blodkropparna i fostrets cirkulation , bryter ner och förstör cellerna . Fostret kan utveckla retikulocytos och anemi . Intensiteten hos denna fostersjukdom sträcker sig från mild till mycket svår, och fosterdöd från hjärtsvikt ( hydrops fetalis ) kan uppstå. När sjukdomen är måttlig eller svår finns många erytroblaster (omogna röda blodkroppar) i fosterblodet, vilket ger dessa former av sjukdomen namnet erythroblastosis fetalis (brittisk engelska: erythroblastosis foetalis ).
HDFN representerar ett brott mot immunprivilegierna för fostret eller någon annan form av försämring av immuntoleransen under graviditeten . Olika typer av HDFN klassificeras enligt vilka alloantigen framkallar svaret. Typerna inkluderar kombinationer av ABO , anti-RhD , anti-RhE , anti-Rhc , anti-Rhe, anti-RhC, multiantigen och anti-Kell . Även om globala prevalensstudier av differentialbidrag från dessa typer saknas, har regionala befolkningsstudier visat att anti-RhD-typen är den vanligaste orsaken till HDFN, följt av anti-RhE, anti-RhC och anti-Rhc.
tecken och symtom
Tecken på hemolytisk sjukdom hos den nyfödda inkluderar ett positivt direkt Coombs -test (även kallat direkt agglutinationstest), förhöjda navelbilirubinnivåer och hemolytisk anemi . Det är möjligt för en nyfödd med denna sjukdom att ha neutropeni och neonatal alloimmun trombocytopeni också. Hemolys leder till förhöjda bilirubinnivåer . Efter förlossningen rensas bilirubin inte längre (via moderkakan) från det nyfödda blodet och symtomen på gulsot (gulaktig hud och gul missfärgning av ögonvitorna eller ikterus ) ökar inom 24 timmar efter födseln. Liksom andra former av svår neonatal gulsot finns det möjlighet att det nyfödda barnet utvecklas akut eller kronisk kernicterus , men risken för kernicterus i HDN är högre på grund av den snabba och massiva förstörelsen av blodkroppar. Det är viktigt att notera att isoimmunisering är en riskfaktor för neurotoxicitet och sänker nivån vid vilken kernicterus kan uppstå. Obehandlad djup anemi kan orsaka hjärtsvikt med hög effekt , med blekhet , förstorad lever och/eller mjälte , generaliserad svullnad och andningssvårigheter .
HDN kan vara orsaken till hydrops fetalis , en ofta allvarlig form av prenatal hjärtsvikt som orsakar fosterödem .
Komplikationer
Komplikationer av HDN kan inkludera kernicterus , hepatosplenomegali , inspicerat (förtjockat eller torkat) gallsyndrom och/eller grönaktig färgning av tänderna , hemolytisk anemi och leverskada på grund av överskott av bilirubin. Tillstånd som kan orsaka liknande symtom under den nyfödda perioden inkluderar: förvärvad hemolytisk anemi , medfödd toxoplasma , medfödd syfilisinfektion , medfödd obstruktion av gallgången och cytomegalovirus (CMV) infektion.
- Hög vid födseln eller snabbt stigande bilirubin
- Långvarig hyperbilirubinemi
- Bilirubininducerad neurologisk dysfunktion
- Cerebral pares
- Kernicterus
- Neutropeni
- Trombocytopeni
- Hemolytisk anemi - FÅR INTE behandlas med järn
- Anemi sent - får INTE behandlas med järn. Kan bestå upp till 12 veckor efter födseln.
Patofysiologi
Antikroppar produceras när kroppen utsätts för ett antigen som är främmande för kroppens sammansättning. Om en mamma utsätts för ett främmande antigen och producerar IgG (i motsats till IgM som inte passerar moderkakan), kommer IgG att rikta sig mot antigenet, om det finns i fostret, och kan påverka det i livmodern och kvarstå efter förlossningen. De tre vanligaste modellerna där en kvinna blir sensibiliserad mot (dvs producerar IgG -antikroppar mot) ett visst antigen är blödning, blodtransfusion och ABO -inkompatibilitet.
Foster-maternell blödning , som är rörelsen av fostrets blodkroppar över moderkakan, kan uppstå under abort , ektopisk graviditet , förlossning , bristningar i moderkakan under graviditeten (ofta orsakad av trauma) eller medicinska ingrepp som utförs under graviditeten som bryter mot livmodervägg. Vid efterföljande graviditeter, om det finns en liknande inkompatibilitet hos fostret, kan dessa antikroppar sedan passera moderkakan in i fostrets blodomlopp för att fästa vid de röda blodkropparna och orsaka deras förstörelse ( hemolys ). Detta är en viktig orsak till HDN, eftersom 75% av graviditeterna resulterar i viss kontakt mellan foster- och moderblod, och 15–50% av graviditeterna har blödningar med risk för immunsensibilisering. Mängden fosterblod som behövs för att orsaka sensibilisering hos mamman beror på individens immunsystem och sträcker sig från 0,1 ml till 30 ml.
Kvinnan kan ha fått en terapeutisk blodtransfusion . ABO -blodgruppssystem och D -antigenet i Rhesus (Rh) blodgruppssystemtypning är rutin före transfusion. Förslag har gjorts att kvinnor i fertil ålder eller unga flickor inte ska ges en transfusion med Rhc-positivt blod eller Kell 1- positivt blod för att undvika eventuell sensibilisering, men detta skulle påverka resurserna för blodtransfusionstjänster, och det är anses för närvarande oekonomiskt att screena för dessa blodgrupper. HDFN kan också orsakas av antikroppar mot en mängd andra blodgruppssystemantigener , men Kell och Rh är de vanligaste.
Den tredje sensibiliseringsmodellen kan förekomma hos kvinnor av blodtyp O. Immunsvaret mot A- och B-antigener, som är utbredda i miljön, leder vanligtvis till produktion av IgM- eller IgG-anti-A- och anti-B-antikroppar tidigt i livet. Kvinnor av blodtyp O är mer benägna än kvinnor av typ A och B att göra IgG anti-A och anti-B antikroppar, och dessa IgG-antikroppar kan passera moderkakan. Av okända skäl är förekomsten av moderantikroppar mot typ A- och B -antigener av IgG -typen som potentiellt kan orsaka hemolytisk sjukdom hos det nyfödda större än den observerade förekomsten av "ABO -sjukdom". Cirka 15% av graviditeterna involverar en typ O -mamma och ett typ A eller typ B -barn; endast 3% av dessa graviditeter resulterar i hemolytisk sjukdom på grund av A/B/O -inkompatibilitet. Till skillnad från antikroppar mot A- och B -antigener verkar produktion av Rhesus -antikroppar vid exponering för miljöantigener variera betydligt mellan individer. I de fall där det finns ABO-inkompatibilitet och Rh-inkompatibilitet minskar risken för alloimmunisering eftersom fostrets röda blodkroppar avlägsnas från moderns cirkulation på grund av anti-ABO-antikroppar innan de kan utlösa ett anti-Rh-svar.
Serologiska typer
HDN klassificeras efter vilken typ av antigener som är inblandade. Huvudtyperna är ABO HDN, Rhesus HDN, Kell HDN och andra antikroppar. Kombinationer av antikroppar (till exempel anti-Rhc och anti-RhE som förekommer tillsammans) kan vara särskilt allvarliga.
ABO hemolytisk sjukdom hos nyfödda kan variera från mild till svår, men i allmänhet är det en mild sjukdom. Det kan orsakas av anti-A och anti-B antikroppar.
Rhesus D hemolytisk sjukdom hos nyfödda (kallas ofta Rh -sjukdom) är den vanligaste och enda förebyggbara formen av allvarlig HDN. Sedan introduktionen av Rho-D-immunglobulin, ( Rhogam , 1968, som förhindrar produktion av moderna Rho-D-antikroppar, har förekomsten av anti-D HDN minskat dramatiskt.
Rhesus c HDFN kan sträcka sig från en mild till svår sjukdom och är den tredje vanligaste formen av svår HDN. Rhesus e och rhesus C hemolytisk sjukdom hos nyfödda är sällsynta. Anti-C och anti-c kan båda visa en negativ DAT men fortfarande ha ett hårt drabbat spädbarn. En indirekt Coombs måste också köras.
Anti-Kell hemolytisk sjukdom hos nyfödda orsakas oftast av anti-K 1- antikroppar, den näst vanligaste formen av allvarlig HDN. Över hälften av fallen av anti-K 1- relaterad HDN orsakas av flera blodtransfusioner. Antikroppar mot de andra Kell -antigenerna är sällsynta. Anti-Kell kan orsaka allvarlig anemi oavsett titer. Det undertrycker benmärgen genom att hämma erytroida stamceller.
Anti-M rekommenderar också antigentestning för att utesluta förekomst av HDN eftersom de direkta coombarna kan komma tillbaka negativa hos ett svårt drabbat spädbarn.
Kidd -antigener finns också på njurarnas endotelceller.
En studie säger att det vore oklokt att rutinmässigt avfärda anti-E som liten klinisk konsekvens. Den fann också att det allvarligaste fallet av anti-E HDFN inträffade med titrarna 1: 2 och drog slutsatsen att titrar inte är tillförlitliga för diagnosen av anti-E-typen.
Diagnos
Den diagnos av HDN bygger på historia och laboratorieresultat:
Blodprov på det nyfödda barnet
- Biokemiska tester för gulsot inklusive totala och direkta bilirubinnivåer .
- Komplett blodantal ( CBC ) som kan visa ett minskat hemoglobin och hematokrit på grund av förstörelse av röda blodkroppar
- Antalet retikulocyter som vanligtvis kommer att öka när benmärgen gör nya röda blodkroppar för att ersätta de som förstörs och ett perifert blodprov för att titta på cellmorfologi . I närvaro av signifikant hemolys visar utstrykningen schistocyter (fragmenterade röda blodkroppar), retikulocytos och i allvarliga fall Erythroblaster (även kända som kärnbildade röda blodkroppar).
- Positivt direkt Coombs -test (kan vara negativt efter fetalt interuterint blodtransfusion)
Blodprov gjorda på modern
- Positivt indirekt Coombs -test
Blodprov på pappan (behövs sällan)
- Erytrocytantigenstatus
Förebyggande
Vid Rho (D) inkompatibilitet ges Rho (D) immunglobulin för att förhindra sensibilisering. Det finns dock ingen jämförbar immunterapi tillgänglig för andra inkompatibiliteter i blodgruppen.
Tidig graviditet
- IVIG - IVIG står för Intravenous Immunoglobulin. Det används i fall av tidigare förlust, höga maternella titrar, kända aggressiva antikroppar och i fall där religion förhindrar blodtransfusion. IVIG kan vara mer effektivt än enbart IUT. Fosterdödligheten minskade med 36% i IVIG- och IUT -gruppen än endast i IUT -gruppen. IVIG och plasmaferes tillsammans kan minska eller eliminera behovet av en IUT.
- Plasmaferes - Plasmaferes syftar till att minska moderns titer genom direkt plasmaersättning och fysiskt avlägsnande av antikropp. Plasmaferes och IVIG tillsammans kan till och med användas på kvinnor med tidigare hydropiska foster och fosterskador.
Mellan till sen graviditet
- IUT - Intrauterin transfusion (IUT) görs antingen genom intraperitoneal transfusion (IPT) eller intravenös transfusion (IVT). IVT är att föredra framför IPT. IUT görs bara fram till 35 veckor. Därefter är risken för IUT större än risken vid transfusion efter födseln.
- Steroider - Steroider ges ibland till modern före IUT och tidig förlossning för att mogna fostrets lungor.
- Fenobarbital - Fenobarbital ges ibland till modern för att hjälpa mogna fostrets lever och minska hyperbilirubinemi.
- Tidig leverans - Leverans kan ske när som helst efter lönsamhetsåldern. Nödleverans på grund av misslyckad IUT är möjlig, tillsammans med arbetskraftsinduktion vid 35–38 veckor.
Rhesus-negativa mödrar som är gravida med ett rhesus-positivt spädbarn erbjuds Rho (D) immunglobulin (RhIG eller RhoGam) 28 veckor under graviditeten, vid 34 veckor och inom 48 timmar efter förlossningen för att förhindra sensibilisering för D-antigenet . Det fungerar genom att binda alla fostrets röda blodkroppar med D-antigenet innan modern kan producera ett immunsvar och bilda anti-D IgG. En nackdel med pre-partum administrering av RhIG är att det orsakar en positiv antikroppsskärm när mamman testas, vilket kan vara svårt att skilja från naturliga immunologiska svar som resulterar i antikroppsproduktion. Utan Rho (D) immunglobulin är risken för isoimmunisering cirka 17%; med korrekt administration minskar risken till mindre än 0,1–0,2%.
Efter födelsetest
- Coombs - i vissa fall (när det finns oro för blodgruppens inkompatibilitet mellan mor och barn till exempel), efter en födelse kommer ett barn att få en direkt Coombs -testkörning för att bekräfta antikropparna som är fästa vid spädbarnets röda blodkroppar. Detta test körs på spädbarnets navelsträngsblod.
I vissa fall kommer de direkta Coombs att vara negativa men allvarliga, även dödliga HDN kan uppstå. En indirekt Coombs måste köras i fall av anti-C, anti-c och anti-M. Spädbarn med Anti-M rekommenderas också att få antigenprovning för att utesluta förekomsten av HDN. Nedanstående tester är ofta användbara vid hemolytisk sjukdom hos nyfödda men krävs inte för behandling av alla nyfödda.
- Hgb - spädbarnets hemoglobin ska testas från navelsträngsblod.
- Antal retikulocyter - Retikulocyter ökar när barnet producerar fler röda blodkroppar som svar på anemi. En ökning av antalet retiska kan innebära att ett spädbarn kanske inte behöver ytterligare transfusioner. Låg retik observeras hos spädbarn som behandlats med IUT och hos barn med HDN från anti-Kell.
- Neutrofiler - eftersom neutropeni är en av komplikationerna med HDN, bör antalet neutrofiler kontrolleras.
- Trombocyter - eftersom trombocytopeni är en av komplikationerna med HDN, bör trombocyttalet kontrolleras.
- Bilirubin ska testas från navelsträngsblod.
- Ferritin - eftersom de flesta spädbarn som drabbas av HDN har järnöverbelastning måste ett ferritin köras innan barnet får ytterligare järn.
- Nyfödda screeningtester - Transfusion med donatorblod under graviditeten eller strax efter födseln kan påverka resultaten av de nyfödda screeningtesterna. Det rekommenderas att vänta och testa igen 10–12 månader efter senaste transfusionen. I vissa fall kan DNA -testning från saliv användas för att utesluta vissa tillstånd.
Behandling
Efter födseln beror behandlingen på tillståndets svårighetsgrad, men kan innefatta temperaturstabilisering och övervakning, fototerapi , transfusion med kompatibelt packat rött blod, utbytstransfusion , natriumbikarbonat för korrigering av acidos och/eller assisterad ventilation.
- Fototerapi - Exponering för ultraviolett ljus (fototerapi) rekommenderas när bilirubin från kabeln är 3 eller högre. Vissa läkare använder det på lägre nivåer i väntan på laboratorieresultat. Detta omvandlar okonjugerat bilirubin till en konjugerad form som är lättare för barnet att rensa.
- IVIG - IVIG har använts för att framgångsrikt behandla många fall av HDN. Det har använts inte bara på anti-D, utan också på anti-E. <IVIG kan användas för att minska behovet av växlingstransfusion och för att förkorta fototerapilängden. AAP rekommenderar "Vid isoimmun hemolytisk sjukdom rekommenderas administrering av intravenös y-globulin (0,5-1 g/kg över 2 timmar) om TSB (totalt serumbilirubin) stiger trots intensiv fototerapi eller TSB-nivån ligger inom 2 till 3 mg /dL (34–51 μmol/L) av utbytesnivån. Vid behov kan denna dos upprepas på 12 timmar (beviskvalitet B: fördelar överstiger skador). Intravenös γ-globulin har visat sig minska behovet av utbytestransfusioner i Rh och ABO hemolytisk sjukdom. "
- Bytransfusion - Bytransfusion används när bilirubin når antingen de höga eller medellånga risklinjerna på nonogrammet från American Academy of Pediatrics (Figur 4). Sladdbilirubin> 4 är också ett tecken på behovet av utbytestransfusion.
Transfusionsreaktioner
När en kvinna har antikroppar löper hon stor risk för en framtida transfusionsreaktion om hon behöver blodtransfusion. Av denna anledning måste hon alltid ha ett medicinskt varningskort och informera alla läkare och akutpersonal om hennes antikroppsstatus. Frånvaron av antikroppar hindrar dock inte en kvinna från att ha en transfusionsreaktion:
"Akuta hemolytiska transfusionsreaktioner kan vara antingen immunförmedlade eller icke-immunförmedlade. Immunförmedlade hemolytiska transfusionsreaktioner orsakade av immunglobulin M (IgM) anti-A, anti-B eller anti-A, B resulterar vanligtvis i allvarliga, potentiellt dödliga komplementförmedlad intravaskulär hemolys. Immunförmedlade hemolytiska reaktioner orsakade av IgG-, Rh-, Kell-, Duffy- eller andra icke-ABO-antikroppar resulterar vanligtvis i extravaskulär sekvestrering, förkortad överlevnad av transfusionerade röda blodkroppar och relativt milda kliniska reaktioner Akuta hemolytiska transfusionsreaktioner på grund av immunhemolys kan förekomma hos patienter som inte har några antikroppar som kan detekteras genom rutinmässiga laboratorieprocedurer. "
För en sammanfattning av transfusionsreaktioner i USA, se referens.
Epidemiologi
År 2003 var förekomsten av Rh (D) sensibilisering i USA 6,8 per 1000 levande födda; 0,27% av kvinnorna med ett Rh -inkompatibelt foster upplever alloimmunisering.
Andra djur
Hemolytisk sjukdom hos den nyfödda ses oftast hos kattungar (där det är känt som "blekande kattens syndrom") och föl. Det har också rapporterats hos valpar .
Se även
- Bytransfusion
- Rh -sjukdom
- Alloimmunisering
- Hemolytisk sjukdom hos nyfödda (anti-Kell)
- Hemolytisk sjukdom hos nyfödda (anti-Rhc)
- Hemolytisk sjukdom hos nyfödda (anti-RhE)
- Hemolytisk sjukdom hos nyfödda (ABO)
- Neonatal röda blodkroppar
Referenser
Vidare läsning
- Geifman-Holtzman O, Wojtowycz M, Kosmas E, Artal R (februari 1997). "Kvinnlig alloimmunisering med antikroppar som är kända för att orsaka hemolytisk sjukdom". Obstetrik och gynekologi . 89 (2): 272–5. doi : 10.1016/S0029-7844 (96) 00434-6 . PMID 9015034 . S2CID 36953155 .
- Mollison PL, Engelfriet CP, Contreras M (1997). Blodtransfusion i klinisk medicin (10: e upplagan). Oxford, Storbritannien: Blackwell Science. ISBN 978-0-86542-881-2.
- Dean L (2005). "Hemolytisk sjukdom hos nyfödda" . Blodgrupper och röda blodkroppsantigener . Nationellt centrum för bioteknikinformation.
externa länkar
| Klassificering | |
|---|---|
| Externa resurser |
