Acetal - Acetal
En acetal är en funktionell grupp med anslutbarheten R 2 C (OR ') 2 ). Här kan R -grupperna vara organiska fragment (en kolatom, med godtyckliga andra atomer kopplade till det) eller väte , medan R' -grupperna måste vara organiska fragment inte väte. De två R' -grupperna kan vara ekvivalenta med varandra (en "symmetrisk acetal") eller inte (en "blandad acetal"). Acetaler bildas från och konverteras till aldehyder eller ketoner och har samma oxidationstillstånd vid det centrala kolet, men har väsentligen olika kemisk stabilitet och reaktivitet jämfört med de analoga karbonylföreningarna . Den centrala kolatomen har fyra bindningar till den och är därför mättad och har tetraedral geometri .
Uttrycket ketal används ibland för att identifiera strukturer associerade med ketoner (båda R-grupperna organiska fragment snarare än väte) snarare än aldehyder och historiskt användes termen acetal specifikt för aldehydrelaterade fall (med minst ett väte istället för ett R på det centrala kolet). IUPAC upphävde ursprungligen användningen av ordet ketal helt och hållet, men har sedan ändrat sitt beslut. Till skillnad från historisk användning är emellertid ketaler nu en delmängd av acetaler, en term som nu omfattar både aldehyd- och keton-härledda strukturer.
Om en av R-grupperna har ett syre som den första atomen (det vill säga att det finns mer än två oxygens enkelbundna till det centrala kolet), är den funktionella gruppen istället en ortoester . Till skillnad från variationer av R är båda R' -grupperna organiska fragment. Om en R 'är ett väte är den funktionella gruppen istället ett hemiacetal , medan om båda är H är den funktionella gruppen ett ketonhydrat eller aldehydhydrat.
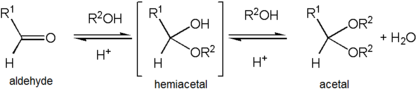
Bildning av en acetal uppstår när hydroxylgruppen i ett hemiacetal blir protonerad och går förlorad som vatten. Den karbokatjon som produceras sedan snabbt attackeras av en molekyl av alkohol . Förlust av protonen från den bifogade alkoholen ger acetalen.
Acetaler är stabila jämfört med hemiacetaler men deras bildning är en reversibel jämvikt som med estrar . När en reaktion för att skapa en acetal fortskrider måste vatten avlägsnas från reaktionsblandningen, till exempel med en Dean – Stark -apparat , så att den inte hydrolyserar produkten tillbaka till hemiacetalen. Bildandet av acetaler minskar det totala antalet närvarande molekyler (karbonyl + 2 alkohol → acetal + vatten) och är därför i allmänhet inte gynnsamt med avseende på entropi . En situation där det inte är entropiskt ogynnsamt är när en enda diolmolekyl används snarare än två separata alkoholmolekyler (karbonyl + diol → acetal + vatten). Ett annat sätt att undvika den entropiska kostnaden är att utföra syntesen genom acetalbyte, med hjälp av ett redan existerande acetaltypsreagens som OR'-gruppgivare snarare än enkel tillsats av alkoholer själva. En typ av reagens som används för denna metod är en ortoester. I detta fall förstörs vatten som produceras tillsammans med acetalprodukten när det hydrolyserar kvarvarande ortoestermolekyler, och denna sidoreaktion ger också mer alkohol som ska användas i huvudreaktionen.
Acetaler används som skyddsgrupper för karbonylgrupper vid organisk syntes eftersom de är stabila med avseende på hydrolys med baser och med avseende på många oxidations- och reduktionsmedel. De kan antingen skydda karbonylen i en molekyl (genom att reagera den tillfälligt med en alkohol) eller en diol (genom att reagera den tillfälligt med en karbonyl). Det vill säga antingen karbonyl eller alkoholer, eller båda kan vara en del av molekylen vars reaktivitet ska kontrolleras.
Olika specifika karbonylföreningar har speciella namn för sina acetalformer. Till exempel kallas en acetal bildad av formaldehyd (två väten fästa vid det centrala kolet) ibland en formell eller metylendioxigrupp . Acetalen som bildas av aceton kallas ibland en acetonid .
Används i en mer allmän bemärkelse, termen X , Y - acetal hänvisar också till vilken som helst funktionell grupp som består av en kolatom som uppbär två heteroatomer X och Y . Till exempel hänvisar N , O -acetal till föreningar av typ R 1 R 2 C (OR) (NR ' 2 ) (R, R' ≠ H) även känd som en hemiaminal eter ) och S , S -acetal avser föreningar av typ R 1 R 2 C (SR) (SR ') (R, R' ≠ H, även känd som en tioacetal ).
Acetalisering
Acetalisering är den organiska reaktionen som involverar bildandet av en acetal (eller ketaler). Ett sätt att bilda acetal är den nukleofila tillsatsen av en alkohol till en keton eller en aldehyd. Acetalisering används ofta i organisk syntes för att skapa en skyddsgrupp eftersom det är en reversibel reaktion.
Acetalisering är syra katalyserad med eliminering av vatten; acetaler gör inte bildas under basiska förhållanden. Reaktionen kan drivas till acetalen när vatten avlägsnas från reaktionssystemet antingen genom azeotrop destillation eller genom att fånga vatten med molekylsilar eller aluminiumoxid .
Karbonylgruppen i 1 tar en proton från hydronium . Den protonerade karbonylgruppen 2 aktiveras för nukleofil tillsats av alkoholen. Strukturerna 2a och 2b är mesomerer . Efter deprotonering av 3 med vatten bildas hemiacetal eller hemiketal 4 . Hydroxylgruppen i 4 är protonerad vilket leder till oxoniumjonen 6 som accepterar en andra alkoholgrupp till 7 med en slutlig deprotonering till acetalen 8 . Omvänd reaktion sker genom tillsats av vatten i samma sura medium. Acetaler är stabila mot grundläggande medier. Vid en transacetalisering eller crossacetalisering reagerar en diol med en acetal eller två olika acetaler reagerar med varandra. Återigen är detta möjligt eftersom alla reaktionsstegen är jämvikt.
Exempel
- Bensylidenacetal , en skyddande grupp
- Dimetoximetan , ett lösningsmedel, aka metylal, aka formellt [tvetydigt]
- Dioxolan
- Metalldehyd
- Paraldehyd
- 1,3,5-Trioxan
- Fenylsulfonyletyliden (PSE) acetal är ett exempel på arylsulfonylacetal som har atypiska egenskaper, som resistens mot syrahydrolys, vilket leder till selektiv introduktion och avlägsnande av den skyddande gruppen.
- De flesta glykosidbindningar i kolhydrater och andra polysackarider är acetalbindningar.
- Cellulosa är ett allestädes närvarande exempel på en polyacetal.
Även om många föreningar innehåller en funktionell acetalgrupp, kallas minst två acetalföreningar "acetal" i korthet:
- Polyoximetylen (POM) plast, även känd som "acetal" eller "polyacetal", är en polyacetal (och en polyeter) och en polymer av formaldehyd .
- 1,1-dietoxietan (acetaldehyddietylacetal), ibland kallat helt enkelt "acetal", är en viktig smakämne i destillerade drycker .
Se även
- Aminal , aka aminoacetal
- Hemiaminal
- Orthoformate
- Tioacetal
- Tioketal
Referenser
- ^ IUPAC , Compendium of Chemical Terminology , andra upplagan. ("Guldboken") (1997). Onlinekorrigerad version: (2006–) " ketaler ". doi : 10.1351/goldbook.K03376
- ^ Morrison, Robert T. och Boyd, Robert N., "Organisk kemi (6: e upplagan)". p683. Prentice-Hall Inc (1992).
- ^ Chéry, Florens; Rollin, Patrick; De Lucchi, Ottorino; Cossu, Sergio (2000). "Fenylsulfonyletyliden (PSE) acetaler som atypiska kolhydratskyddande grupper". Tetrahedron bokstäver . 41 (14): 2357–2360. doi : 10.1016/s0040-4039 (00) 00199-4 . ISSN 0040-4039 .
- ^ IUPAC , Compendium of Chemical Terminology , andra upplagan. ("Guldboken") (1997). Onlinekorrigerad version: (2006–) " glykosider ". doi : 10.1351/goldbook.G02661
- ^ Flyktiga föreningar i livsmedel och drycker, ISBN 0-8247-8390-5 , https://books.google.com/books?id=_OvXjhLUz-oC , s.554