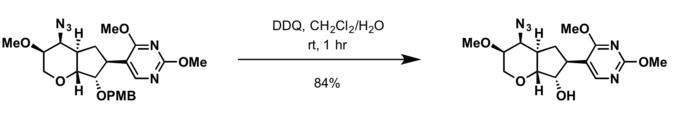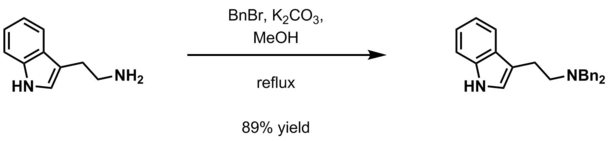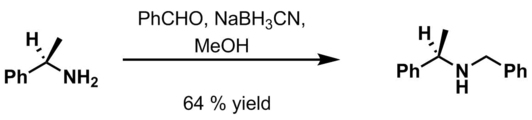Bensylgrupp - Benzyl group
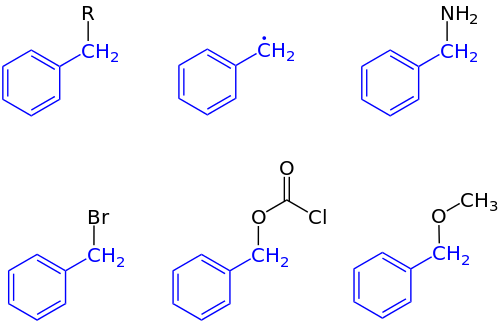
I organisk kemi , bensyl är den substituent eller molekylfragment som har strukturen C 6 H 5 CH 2 -. Bensyl har en bensenring fäst vid en CH 2- grupp.
Nomenklatur
I lUPAC-nomenklatur prefixet bensyl avser en C 6 H 5 CH 2 substituent, exempelvis bensylklorid eller bensylbensoat . Bensyl är att inte förväxlas med fenyl med formeln C 6 H 5 . Uttrycket bensyl används för att beskriva positionen för det första kolet bundet till en bensen eller annan aromatisk ring. Exempelvis (C 6 H 5 ) (CH 3 ) 2 C + benämnes en "bensylisk" karbokatjon. Den bensylfria radikalen har formeln C
6 H
5 CH •
2 . Bensylkatjonen eller fenylkarbeniumjonen är karbocentrationen med formel C
6 H
5 CH +
2 ; bensylanjonen eller fenylmetaniden är karbanjonen med formeln C
6 H
5 CH -
2 . Ingen av dessa arter kan bildas i betydande mängder i lösningsfasen under normala förhållanden, men de är användbara referenser för diskussion av reaktionsmekanismer och kan existera som reaktiva mellanprodukter.
Förkortningar
Förkortningen "Bn" betecknar bensyl. Exempelvis kan bensylalkohol representeras som BnOH. Denna förkortning är ej att förväxla med "Bz", som är en förkortning för bensoyl grupp C 6 H 5 C (O) -, eller fenylgruppen C 6 H 5 , förkortat "Ph". Förvirrande, i gammal litteratur, användes "Bz" också för bensyl.
Reaktivitet hos bensylcentra
Den förbättrade reaktiviteten för bensylpositioner tillskrivs den låga bindningsdissociationsenergin för bensyliska C-H-bindningar. Specifikt bindningen C 6 H 5 CH 2 -H är ca 10-15% svagare än andra typer av CH-bindningar. Den angränsande aromatiska ringen stabiliserar bensylradikaler. Uppgifterna i tabellen nedan jämför bensyliska C-H-bindningar med relaterade C-H-bindningsstyrkor.
| Obligation | Obligation | Bond-dissociationsenergi | Kommentar | |
|---|---|---|---|---|
| (kcal / mol) | (kJ / mol) | |||
| C 6 H 5 CH 2 −H | bensylisk C-H-bindning | 90 | 377 | besläktad med allyliska C-H- bindningar visar sådana bindningar förbättrad reaktivitet |
| H 3 C − H | metyl C-H-bindning | 105 | 439 | en av de starkaste alifatiska C-H-bindningarna |
| C 2 H 5 −H | etyl- C-H-bindning | 101 | 423 | något svagare än H 3 C − H |
| C 6 H 5 −H | fenyl C-H-bindning | 113 | 473 | jämförbar med vinylradikal, sällsynt |
| CH 2 = CHCH 2 -H | allylisk C – H-bindning | 89 | 372 | liknar bensylisk CH |
| (C 6 H 4 ) 2 CH − H | fluorenyl C-H-bindning | 80 | mer aktiverad vs difenylmetyl ( pKa = 22,6) | |
| (C 6 H 5 ) 2 CH − H | difenylmetyl C-H-bindning | 82 | "dubbelt bensylisk" ( pKa = 32,2) | |
| (C 6 H 5 ) 3 C − H | trityl C – H-bindning | 81 | 339 | "triply bensylisk" |
C-H-bindningens svaghet återspeglar stabiliteten hos bensylradikalen. Av besläktade skäl uppvisar bensylsubstituenter förbättrad reaktivitet, såsom vid oxidation , halogenering av fria radikaler eller hydrogenolys . Som ett praktiskt exempel, i närvaro av lämpliga katalysatorer, p - xylen oxiderar exklusivt på de bensyliska positioner för att ge tereftalsyra :
- CH 3 C 6 H 4 CH 3 + 3 O 2 → HO 2 CC 6 H 4 CO 2 H ^ 2 H 2 O.
Miljontals ton tereftalsyra produceras årligen med denna metod.
Funktionalisering vid bensylposition
I några få fall inträffar dessa bensyltransformationer under betingelser som är lämpliga för laboratoriesyntes. Den Wohl-Ziegler reaktion kommer bromera en bensylisk C-H-bindning: (ArCHR 2 → ArCBrR 2 ). Någon icke-tertiär bensylisk alkylgrupp kommer att oxideras till en karboxylgrupp genom vattenhaltig kaliumpermanganat (KMnO 4 ) eller koncentrerad salpetersyra (HNO 3 ): (ArCHR 2 → ArCOOH). Slutligen, komplexet av kromtrioxid och 3,5-dimetylpyrazol (CrOs 3 -dmpyz) kommer selektivt oxidera en bensylisk metylengrupp till en karbonylgrupp: (ArCH 2 R → ArC (O) R). 2-jodoxibensoesyra i DMSO fungerar lika.
Som en skyddsgrupp
Bensylgrupper används ibland som skyddsgrupper vid organisk syntes. Deras installation och särskilt avlägsnande av dem kräver relativt hårda förhållanden, så bensyl är vanligtvis inte att föredra för skydd.
Alkoholskydd
Bensyl används ofta i organisk syntes som en robust skyddsgrupp för alkoholer och karboxylsyror .
- Behandling av alkohol med en stark bas såsom pulveriserad kaliumhydroxid eller natriumhydrid och bensylhalogenid ( BnCl eller BnBr )
- Monobenzylation av dioler kan uppnås med användning Ag 2 O i dimetylformamid (DMF) vid omgivande till förhöjda temperaturer
- Primära alkoholer kan selektivt bensyleras i närvaro av fenolfunktionella grupper med användning av Cu (acac) 2
Avskyddande metoder
Bensyletrar kan avlägsnas under reduktiva förhållanden , oxidativa förhållanden och med användning av Lewis-syror .
- Borttagen med hydrogenolys
- Enda elektronprocess med Na / NH 3 eller Li / NH 3
- Bensylskyddsgrupper kan avlägsnas med ett brett spektrum av oxidationsmedel, inklusive:
- CrO 3 / ättiksyra vid omgivande temperatur
- Ozon
- N- bromsuccinimid (NBS)
- N- jodosuccinimid (NIS)
- Trimetylsilyl -jodid (Me 3 SII) i diklormetan vid omgivningstemperatur (selektivitet kan uppnås under vissa villkor)
Den p -metoxibensyl skyddande grupp
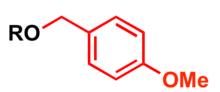
p- Metoxibensyl ( PMB ) används som en skyddsgrupp för alkoholer i organisk syntes ( 4-metoxibensyltiol används för att skydda tioler).
- Stark bas såsom pulveriserad kaliumhydroxid eller natriumhydrid och p- metoxibensylhalogenid (klorid eller bromid)
- 4-metoxibensyl-2,2,2-trikloracetimidat kan användas för att installera PMB-gruppen i närvaro av:
- Scandium (III) triflat (Sc (OTf) 3 ) i toluen vid 0 ° C
-
Trifluormetansulfonsyra (TfOH) i diklormetan vid 0 ° C
Avskyddande metoder
- 2,3-diklor-5,6-dicyano- p- bensokinon (DDQ)
- Villkor för avskyddande av bensylgruppen är tillämpliga för klyvning av PMB-skyddsgruppen
Aminskydd
Bensylgruppen används ibland som en skyddsgrupp för aminer i organisk syntes . Det finns andra metoder.
- Vattenhaltigt kaliumkarbonat och bensylhalogenid ( BnCl , BnBr ) i metanol
-
Bensaldehyd , 6 M HCl och NaBH 3 CN i metanol
Avskyddande metoder
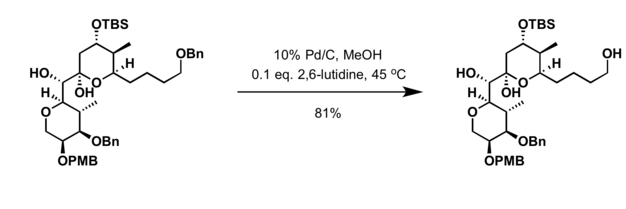
- Hydrogenering i närvaro av palladiumkatalysator
Se även
Referenser
externa länkar
-
 Kemiportal
Kemiportal
-
 Citat relaterade till Benzyl-gruppen på Wikiquote
Citat relaterade till Benzyl-gruppen på Wikiquote