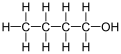
1 -Butanol - 1-Butanol
|
|
|||
|
|||
| Namn | |||
|---|---|---|---|
|
Föredraget IUPAC -namn
Butan-1-ol |
|||
| Andra namn
n -Butanol
n -Butylalkohol n -Butylhydroxid n -Propylkarbinol n -Propylmetanol 1 -Hydroxibutan Metylolpropan |
|||
| Identifierare | |||
|
3D -modell ( JSmol )
|
|||
| 3DMet | |||
| 969148 | |||
| ChEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.000.683 |
||
| EG -nummer | |||
| 25753 | |||
| KEGG | |||
| Maska | 1-Butanol | ||
|
PubChem CID
|
|||
| RTECS -nummer | |||
| UNII | |||
| FN -nummer | 1120 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C 4 H 10 O | |||
| Molmassa | 74,123 g · mol −1 | ||
| Utseende | Färglös, brytande vätska | ||
| Odör | bananliknande , hård, alkoholhaltig och söt | ||
| Densitet | 0,81 g / cm 3 | ||
| Smältpunkt | −89,8 ° C (−129,6 ° F; 183,3 K) | ||
| Kokpunkt | 117,7 ° C (243,9 ° F; 390,8 K) | ||
| 73 g/L vid 25 ° C | |||
| Löslighet | mycket löslig i aceton blandbar med etanol , etyleter |
||
| logg P | 0,839 | ||
| Ångtryck | 0,58 kPa (20 ° C) ILO International Chemical Safety Cards (ICSC) | ||
| Surhet (p K a ) | 16.10 | ||
| −56.536 · 10 −6 cm 3 /mol | |||
|
Brytningsindex ( n D )
|
1.3993 (20 ° C) | ||
| Viskositet | 2,573 mPa · s (vid 25 ° C) | ||
| 1,66 D | |||
| Termokemi | |||
|
Std molar
entropi ( S |
225,7 J/(K · mol) | ||
|
Std entalpi för
bildning (Δ f H ⦵ 298 ) |
−328 (4) kJ/mol | ||
|
Std entalpin för
förbränning (Δ c H ⦵ 298 ) |
−2670 (20) kJ/mol | ||
| Faror | |||
| Säkerhetsdatablad | ICSC 0111 | ||
| GHS -piktogram |
  
|
||
| NFPA 704 (eldiamant) | |||
| Flampunkt | 35 ° C (95 ° F; 308 K) | ||
| 343 ° C (649 ° F; 616 K) | |||
| Explosiva gränser | 1,45–11,25% | ||
| Dödlig dos eller koncentration (LD, LC): | |||
|
LD 50 ( median dos )
|
790 mg/kg (råtta, oral) | ||
|
LD Lo ( lägst publicerad )
|
3484 mg/kg (kanin, oral) 790 mg/kg (råtta, oral) 1700 mg/kg (hund, oral) |
||
|
LC 50 ( mediankoncentration )
|
9221 ppm (däggdjur) 8000 ppm (råtta, 4 h ) |
||
| NIOSH (amerikanska hälsoexponeringsgränser): | |||
|
PEL (tillåtet)
|
TWA 100 ppm (300 mg/m 3 ) | ||
|
REL (rekommenderas)
|
C 50 ppm (150 mg/m 3 ) [hud] | ||
|
IDLH (Omedelbar fara)
|
1400 sid / min | ||
| Relaterade föreningar | |||
|
Relaterade föreningar
|
Butantiol n -butylamin Dietyleter Pentan |
||
|
Om inte annat anges, ges data för material i deras standardtillstånd (vid 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infobox -referenser | |||
Butan-1-ol , även känd som n-butanol är en primär alkohol med den kemiska formeln C 4 H 9 OH och en linjär struktur. Isomerer av butan-1-ol är isobutanol , butan-2-ol och tert- butanol . Den omodifierade termen butanol hänvisar vanligtvis till isomer med rak kedja.
1-Butanol förekommer naturligt som en mindre produkt av etanoljäsningen av sockerarter och andra sackarider och finns i många livsmedel och drycker. Det är också ett tillåtet artificiellt smakämne i USA, som används i smör, grädde, frukt, rom, whisky, glass och is, godis, bakverk och godis. Det används också i ett brett utbud av konsumentprodukter.
Den största användningen av 1-butanol är som en industriell mellanprodukt, särskilt för tillverkning av butylacetat (i sig ett artificiellt smakämne och industriellt lösningsmedel). Det är en petrokemikalie som härrör från propylen . Uppskattade produktionssiffror för 1997 är: USA 784 000 ton; Västeuropa 575 000 ton; Japan 225 000 ton.
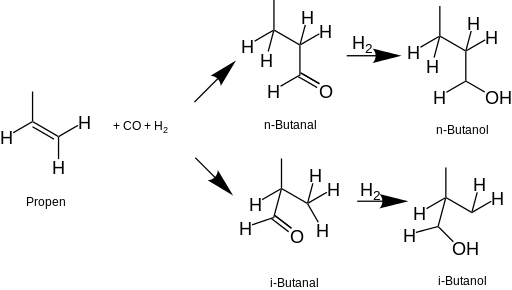
Produktion
Sedan 1950-talet produceras mest 1-butanol genom hydroformylering av propen (oxoprocess) för att företrädesvis bilda butyraldehyd- n-butanal. Typiska katalysatorer är baserade på kobolt och rodium. Butyraldehyd därefter hydreras för att producera butanol.
En andra metod för att producera butanol involverar Reppe -reaktionen av propen med CO och vatten:
- CH 3 CH = CH 2 + H 2 O + 2 CO → CH 3 CH 2 CH 2 CH 2 OH + CO 2
Tidigare framställdes butanol av krotonaldehyd , som kan erhållas från acetaldehyd .
Butanol kan också produceras genom jäsning av biomassa av bakterier. Före 1950 -talet användes Clostridium acetobutylicum vid industriell jäsning för att producera butanol. Forskning under de senaste decennierna visade resultat av andra mikroorganismer som kan producera butanol genom jäsning.
Industriell användning
1-butanol utgör 85% av dess användning och används främst vid tillverkning av lacker . Det är ett populärt lösningsmedel, t.ex. för nitrocellulosa . En mängd butylestrar används som lösningsmedel, t.ex. butoxietanol . Många mjukningsmedel är baserade på butylestrar, t.ex. dibutylftalat . Den monomer butylakrylat används för att producera polymerer. Det är föregångaren till n-butylaminer .
Biobränsle
1-Butanol har föreslagits som ett substitut för dieselbränsle och bensin . Den produceras i små mängder i nästan alla jäsningar (se fuselolja ). Clostridium ger mycket högre utbyten av butanol. Forskning pågår för att öka biobutanolutbytet från biomassa .
Butanol anses vara ett potentiellt biobränsle ( butanolbränsle ). Butanol med 85 procents styrka kan användas i bilar som är konstruerade för bensin utan förändring av motorn (till skillnad från 85% etanol), och det ger mer energi för en given volym än etanol, på grund av butanols lägre syrehalt, och nästan lika mycket som bensin. Därför skulle ett fordon som använder butanol returnera bränsleförbrukningen mer jämförbar med bensin än etanol. Butanol kan också tillsättas diesel för att minska sotutsläpp.
Framställning av, eller i vissa fall, användning av följande ämnen kan resultera i exponering för 1-butanol: konstläder , butylestrar , gummicement , färgämnen, fruktessenser, lacker, film och fotografiska filmer, regnrockar, parfymer, pyroxylinplaster , rayon , säkerhetsglas, skalellack och vattentät trasa.
Förekomst i naturen
Butan-1-ol förekommer naturligt som ett resultat av kolhydratjäsning i ett antal alkoholhaltiga drycker, inklusive öl, druvbrännvin, vin och whisky. Det har upptäckts i flyktiga ämnen humle, jackfrukt, värmebehandlad mjölk, myskmelon, ost, södra ärtfrön och kokt ris. 1-Butanol bildas också vid fritering av majsolja, bomullsfröolja, trilinolein och triolein.
Butan-1-ol är en av " fuselalkoholerna " (från tyska för "dålig sprit"), som inkluderar alkoholer som har mer än två kolatomer och har betydande löslighet i vatten. Det är en naturlig komponent i många alkoholhaltiga drycker, om än i låga och varierande koncentrationer. Det (tillsammans med liknande fuselalkoholer) är ansett att vara ansvarigt för allvarliga baksmälla , även om experiment i djurmodeller inte visar några bevis för detta.
1-Butanol används som ingrediens i bearbetade och artificiella smakämnen, och för extraktion av lipidfritt protein från äggula, naturliga smakämnen och vegetabiliska oljor, tillverkning av humleextrakt för ölproduktion och som lösningsmedel för att avlägsna pigment från fuktig ostmassa bladproteinkoncentrat .
Metabolism och toxicitet
Den akuta toxiciteten för 1-butanol är relativt låg, med orala LD 50- värden på 790–4 360 mg/kg (råtta; jämförbara värden för etanol är 7 000–15 000 mg/kg). Det metaboliseras fullständigt i ryggradsdjur på ett sätt som liknar etanol : alkoholdehydrogenas omvandlar 1-butanol till butyraldehyd ; detta omvandlas därefter till smörsyra av aldehyddehydrogenas . Smörsyra kan fullständigt metaboliseras till koldioxid och vatten genom β-oxidationsvägen . Hos råtta utsöndrades endast 0,03% av en oral dos på 2000 mg/kg i urinen. Vid sub-dödliga doser fungerar 1-butanol som ett depressiv medel i centrala nervsystemet , liknande etanol: en studie på råttor indikerade att den berusande styrkan hos 1-butanol är cirka 6 gånger högre än för etanol, möjligen på grund av dess långsammare transformation med alkoholdehydrogenas.
Andra faror
Flytande 1-butanol, som är vanligt med de flesta organiska lösningsmedel, är extremt irriterande för ögonen; upprepad kontakt med huden kan också orsaka irritation. Detta antas vara en generisk effekt av "avfettning". Ingen hudsensibilisering har observerats. Irritation av andningsvägarna uppträder endast vid mycket höga koncentrationer (> 2400 ppm).
Med en flampunkt på 35 ° C utgör 1-butanol en måttlig brandrisk: den är något mer brandfarlig än fotogen eller dieselbränsle men mindre brandfarlig än många andra vanliga organiska lösningsmedel. Den dämpande effekten på centrala nervsystemet (liknande etanolförgiftning) är en potentiell fara vid arbete med 1-butanol i slutna utrymmen, även om luktgränsen (0,2–30 ppm) ligger långt under den koncentration som skulle ha någon neurologisk effekt.
Se även
externa länkar
- Internationellt kemikaliesäkerhetskort 0111
- NIOSH fickguide för kemiska faror. "#0076" . National Institute for Occupational Safety and Health (NIOSH).
- SIDS Initial Assessment Report för n -Butanol från Organisationen för ekonomiskt samarbete och utveckling (OECD)
- IPCS Environmental Health Criteria 65: Butanoler: fyra isomerer
- IPCS Health and Safety Guide 3: 1-Butanol