Viskositet -Viscosity
| Viskositet | |
|---|---|
 En simulering av vätskor med olika viskositeter. Vätskan till vänster har lägre viskositet än vätskan till höger.
| |
Vanliga symboler |
η , μ |
Härledningar från andra kvantiteter |
μ = G · t |
| Del av en serie om |
| Kontinuummekanik |
|---|
Viskositeten hos en vätska är ett mått på dess motstånd mot deformation vid en given hastighet. För vätskor motsvarar det det informella konceptet "tjocklek": till exempel har sirap en högre viskositet än vatten .
Viskositeten kvantifierar den inre friktionskraften mellan intilliggande lager av vätska som är i relativ rörelse. Till exempel, när en viskös vätska tvingas genom ett rör, flyter den snabbare nära rörets axel än nära dess väggar. Experiment visar att viss stress (såsom en tryckskillnad mellan de två ändarna av röret) behövs för att upprätthålla flödet. Detta beror på att en kraft krävs för att övervinna friktionen mellan skikten av vätskan som är i relativ rörelse. För ett rör med konstant flödeshastighet är styrkan på kompensationskraften proportionell mot vätskans viskositet.
I allmänhet beror viskositeten på en vätskas tillstånd, såsom dess temperatur, tryck och deformationshastighet. Beroendet av vissa av dessa fastigheter är dock försumbart i vissa fall. Till exempel varierar inte viskositeten hos en newtonsk vätska nämnvärt med deformationshastigheten. Nollviskositet (ingen motståndskraft mot skjuvspänning ) observeras endast vid mycket låga temperaturer i superfluids ; annars kräver termodynamikens andra lag att alla vätskor har positiv viskositet. En vätska som har noll viskositet kallas ideal eller inviscid .
Etymologi
Ordet "viskositet" kommer från latinets viscum (" mistel "). Viscum hänvisade också till ett trögflytande lim som härrör från mistelbär.
Definition
Dynamisk viskositet
Inom materialvetenskap och ingenjörsvetenskap är man ofta intresserad av att förstå krafterna eller påfrestningarna som är involverade i deformationen av ett material. Till exempel, om materialet var en enkel fjäder, skulle svaret ges av Hookes lag , som säger att kraften som upplevs av en fjäder är proportionell mot avståndet som förskjuts från jämvikt. Spänningar som kan hänföras till deformation av ett material från något viloläge kallas elastiska spänningar. I andra material förekommer spänningar som kan hänföras till förändringshastigheten av deformationen över tiden. Dessa kallas viskösa spänningar. Till exempel, i en vätska såsom vatten beror spänningarna som uppstår vid skjuvning av vätskan inte på avståndet som vätskan har skjuvats; snarare beror de på hur snabbt klippningen sker.
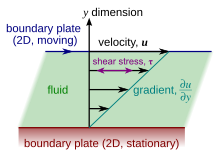
Viskositet är den materialegenskap som relaterar de viskösa spänningarna i ett material till förändringshastigheten för en deformation (töjningshastigheten). Även om det gäller allmänna flöden är det lätt att visualisera och definiera i ett enkelt skjuvflöde, till exempel ett plant Couette-flöde .
I Couette-flödet fångas en vätska mellan två oändligt stora plattor, en fast och en i parallell rörelse med konstant hastighet (se bilden till höger). Om hastigheten på toppplattan är tillräckligt låg (för att undvika turbulens) så rör sig vätskepartiklarna parallellt med den i ett stabilt tillstånd och deras hastighet varierar från botten till toppen. Varje lager av vätska rör sig snabbare än det precis under det, och friktion mellan dem ger upphov till en kraft som motstår deras relativa rörelse. Speciellt anbringar vätskan på toppplattan en kraft i motsatt riktning mot dess rörelse och en lika stor men motsatt kraft på bottenplattan. En extern kraft krävs därför för att hålla toppplattan i rörelse med konstant hastighet.
I många vätskor observeras flödeshastigheten att variera linjärt från noll i botten till toppen. Dessutom visar sig storleken på kraften, som verkar på toppplattan, vara proportionell mot hastigheten och arean för varje platta, och omvänt proportionell mot deras separation :
Proportionalitetsfaktorn är vätskans dynamiska viskositet , ofta helt enkelt kallad viskositeten . Det betecknas med den grekiska bokstaven mu ( μ ). Den dynamiska viskositeten har dimensionerna , vilket resulterar i SI-enheterna och de härledda enheterna :
Det tidigare nämnda förhållandet kallas hastigheten för skjuvdeformation eller skjuvhastighet och är derivatan av vätskehastigheten i riktningen vinkelrät mot plattornas normalvektor (se bilderna till höger). Om hastigheten inte varierar linjärt med , då är den lämpliga generaliseringen:
där , och är den lokala skjuvhastigheten. Detta uttryck kallas Newtons viskositetslag. I skjuvflöden med plan symmetri är det vad som definierar . Det är ett specialfall av den allmänna definitionen av viskositet (se nedan), som kan uttryckas i koordinatfri form.
Användning av den grekiska bokstaven mu ( ) för den dynamiska viskositeten (kallas ibland även den absoluta viskositeten ) är vanligt bland mekaniska och kemiingenjörer , såväl som matematiker och fysiker. Den grekiska bokstaven eta ( ) används dock också av kemister, fysiker och IUPAC . Viskositeten kallas ibland även för skjuvviskositeten . Men åtminstone en författare avråder från användningen av denna terminologi, och noterar att den kan förekomma i icke-skjuvande flöden utöver skjuvningsflöden.
Kinematisk viskositet
Inom vätskedynamik är det ibland mer lämpligt att arbeta i termer av kinematisk viskositet (ibland även kallad momentumdiffusivitet ), definierad som förhållandet mellan den dynamiska viskositeten ( μ ) och vätskans densitet ( ρ ). Det betecknas vanligtvis med den grekiska bokstaven nu ( ν ):
och har dimensionerna , vilket resulterar i SI-enheterna och de härledda enheterna :
- specifik energi multiplicerad med tid .
Allmän definition
I mycket allmänna termer definieras de viskösa spänningarna i en vätska som de som härrör från den relativa hastigheten för olika vätskepartiklar. Som sådan måste de viskösa spänningarna bero på rumsliga gradienter av flödeshastigheten. Om hastighetsgradienterna är små beror till en första approximation de viskösa spänningarna endast på de första derivatorna av hastigheten. (För newtonska vätskor är detta också ett linjärt beroende.) I kartesiska koordinater kan det allmänna sambandet då skrivas som
var är en viskositetstensor som kartlägger hastighetsgradienttensorn på den viskösa spänningstensorn . Eftersom indexen i detta uttryck kan variera från 1 till 3 finns det totalt 81 "viskositetskoefficienter" . Men om man antar att viskositetsrank-4-tensorn är isotrop reducerar dessa 81 koefficienter till tre oberoende parametrar , , :
och vidare antas det att inga viskösa krafter kan uppstå när vätskan genomgår enkel rotation av stelkroppen, vilket således endast lämnar två oberoende parametrar. Den vanligaste nedbrytningen är i termer av standardviskositeten (skalär) och bulkviskositeten så att och . I vektornotation ser detta ut som:
var är enhetens tensor, och dolken anger transponeringen . Denna ekvation kan ses som en generaliserad form av Newtons viskositetslag.
Bulkviskositeten (även kallad volymviskositet) uttrycker en typ av inre friktion som motstår skjuvlös kompression eller expansion av en vätska. Kunskap om är ofta inte nödvändigt i flödesdynamikproblem. Till exempel uppfyller en inkompressibel vätska och så faller termen innehållande ut. Dessutom antas ofta vara försumbar för gaser eftersom det är i en monoatomisk idealgas . En situation som kan vara viktig är beräkningen av energiförlust i ljud- och stötvågor , beskriven av Stokes lag om ljuddämpning , eftersom dessa fenomen involverar snabba expansioner och kompressioner.
De definierande ekvationerna för viskositet är inte grundläggande naturlagar, så deras användbarhet, såväl som metoder för att mäta eller beräkna viskositeten, måste fastställas med hjälp av separata metoder. En potentiell fråga är att viskositeten i princip beror på vätskans fullständiga mikroskopiska tillstånd, vilket omfattar positionerna och momenten för varje partikel i systemet. Sådan mycket detaljerad information är vanligtvis inte tillgänglig i realistiska system. Men under vissa förhållanden kan det mesta av denna information visas vara försumbar. Speciellt för newtonska vätskor nära jämvikt och långt från gränser (bulktillstånd), beror viskositeten endast på rymd- och tidsberoende makroskopiska fält (såsom temperatur och densitet) som definierar lokal jämvikt.
Icke desto mindre kan viskositeten fortfarande ha ett icke försumbart beroende av flera systemegenskaper, såsom temperatur, tryck och amplituden och frekvensen av eventuell extern forcering. Därför definieras precisionsmätningar av viskositet endast med avseende på ett specifikt vätsketillstånd. För att standardisera jämförelser mellan experiment och teoretiska modeller extrapoleras viskositetsdata ibland till idealiska begränsningsfall, såsom nollskjuvgränsen eller (för gaser) nolldensitetsgränsen .
Momentum transport
Transportteori ger en alternativ tolkning av viskositet i termer av rörelsemängdstransport: viskositet är den materialegenskap som kännetecknar rörelsemängdstransport inom en vätska, precis som värmeledningsförmåga kännetecknar värmetransport , och (mass) diffusion kännetecknar masstransport. Detta perspektiv är implicit i Newtons viskositetslag, eftersom skjuvspänningen har enheter som motsvarar ett momentumflöde , dvs momentum per tidsenhet och areaenhet. Kan således tolkas som att specificera flödet av momentum i riktningen från ett vätskeskikt till nästa. Enligt Newtons viskositetslag sker detta momentumflöde över en hastighetsgradient, och storleken på motsvarande momentumflöde bestäms av viskositeten.
Analogin med värme- och massöverföring kan göras explicit. Precis som värme strömmar från hög temperatur till låg temperatur och massa strömmar från hög densitet till låg densitet, flyter momentum från hög hastighet till låg hastighet. Dessa beteenden beskrivs alla av kompakta uttryck, kallade konstitutiva relationer , vars endimensionella former ges här:
var är densiteten, och är massan och värmeflödena, och och är massans diffusivitet och värmeledningsförmåga. Det faktum att mass-, momentum- och energi(värme)transport är bland de mest relevanta processerna inom kontinuummekaniken är inte en slump: dessa är bland de få fysikaliska storheter som bevaras på mikroskopisk nivå vid interpartikelkollisioner. Sålunda, snarare än att dikteras av den snabba och komplexa mikroskopiska interaktionens tidsskala, sker deras dynamik på makroskopiska tidsskalor, som beskrivs av de olika ekvationerna för transportteori och hydrodynamik.
Newtonska och icke-newtonska vätskor
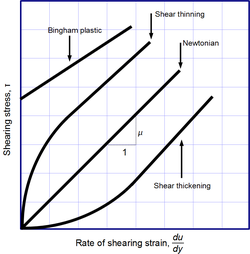
Newtons viskositetslag är inte en grundläggande naturlag, utan snarare en konstitutiv ekvation (som Hookes lag , Ficks lag och Ohms lag ) som tjänar till att definiera viskositeten . Dess form är motiverad av experiment som visar att det för ett brett spektrum av vätskor är oberoende av töjningshastigheten. Sådana vätskor kallas Newtonska . Gaser , vatten och många vanliga vätskor kan betraktas som newtonska i vanliga förhållanden och sammanhang. Det finns dock många icke-newtonska vätskor som väsentligt avviker från detta beteende. Till exempel:
- Skjuvförtjockande (dilatant) vätskor, vars viskositet ökar med hastigheten på skjuvtöjningen.
- Skjuvförtunnande vätskor, vars viskositet minskar med hastigheten på skjuvtöjningen.
- Tixotropa vätskor, som blir mindre trögflytande med tiden när de skakas, skakas eller på annat sätt stressas.
- Reopektiska vätskor, som blir mer trögflytande med tiden när de skakas, upprörda eller på annat sätt stressade.
- Binghamplaster som beter sig som ett fast ämne vid låga spänningar men flyter som en trögflytande vätska vid höga spänningar.
Troutons förhållande är förhållandet mellan extensionsviskositet och skjuvviskositet . För en Newtonsk vätska är Trouton-förhållandet 3. Skjuvförtunnande vätskor är mycket vanliga, men missvisande, beskrivna som tixotropa.
Även för en newtonsk vätska beror viskositeten vanligtvis på dess sammansättning och temperatur. För gaser och andra komprimerbara vätskor beror det på temperaturen och varierar mycket långsamt med trycket. Viskositeten hos vissa vätskor kan bero på andra faktorer. En magnetoreologisk vätska , till exempel, blir tjockare när den utsätts för ett magnetfält , möjligen till den grad att den beter sig som ett fast ämne.
I fasta ämnen
De viskösa krafterna som uppstår under vätskeflöde skiljer sig från de elastiska krafterna som uppstår i ett fast ämne som svar på skjuv-, kompressions- eller töjspänningar. Medan spänningen i den senare är proportionell mot mängden skjuvdeformation, är den i en vätska proportionell mot deformationshastigheten över tiden. Av denna anledning använde Maxwell termen flyktig elasticitet för vätskeviskositet.
Men många vätskor (inklusive vatten) reagerar kort som elastiska fasta ämnen när de utsätts för plötslig påfrestning. Omvänt kommer många "fasta ämnen" (även granit ) att flyta som vätskor, om än mycket långsamt, även under godtyckligt liten belastning. Sådana material beskrivs bäst som viskoelastiska - det vill säga besitter både elasticitet (reaktion på deformation) och viskositet (reaktion på deformationshastighet).
Viskoelastiska fasta ämnen kan uppvisa både skjuvviskositet och bulkviskositet. Extensionsviskositeten är en linjär kombination av skjuv- och bulkviskositeten som beskriver reaktionen mellan ett fast elastiskt material och förlängning. Det används ofta för att karakterisera polymerer.
Inom geologi kallas jordmaterial som uppvisar viskös deformation som är minst tre storleksordningar större än deras elastiska deformation ibland rheids .
Mått
Viskositeten mäts med olika typer av viskometer och reometrar . En reometer används för vätskor som inte kan definieras av ett enda viskositetsvärde och därför kräver att fler parametrar ställs in och mäts än vad som är fallet för en viskosimeter. Noggrann temperaturkontroll av vätskan är avgörande för att få exakta mätningar, särskilt i material som smörjmedel, vars viskositet kan fördubblas med en förändring på endast 5 °C.
För vissa vätskor är viskositeten konstant över ett brett spektrum av skjuvhastigheter ( Newtonska vätskor ). Vätskorna utan konstant viskositet ( icke-newtonska vätskor ) kan inte beskrivas med ett enda tal. Icke-newtonska vätskor uppvisar en mängd olika korrelationer mellan skjuvspänning och skjuvhastighet.
Ett av de vanligaste instrumenten för att mäta kinematisk viskositet är glaskapillärviskosimetern.
I beläggningsindustrier kan viskositeten mätas med en kopp i vilken utflödestiden mäts. Det finns flera typer av koppar – som Zahn-koppen och Fords viskositetskopp – där användningen av varje typ varierar huvudsakligen beroende på branschen.
En Stormer viskosimeter används också i beläggningar och använder belastningsbaserad rotation för att bestämma viskositeten. Viskositeten redovisas i Krebs-enheter (KU), som är unika för Stormer viskometrar.
Vibrerande viskosimeter kan också användas för att mäta viskositet. Resonans- eller vibrationsviskometer fungerar genom att skapa skjuvvågor i vätskan. I denna metod är sensorn nedsänkt i vätskan och får resonans vid en specifik frekvens. När sensorns yta skär genom vätskan går energi förlorad på grund av dess viskositet. Denna förbrukade energi mäts sedan och omvandlas till en viskositetsavläsning. En högre viskositet orsakar en större energiförlust.
Extensionsviskositet kan mätas med olika reometrar som applicerar extensionsspänning .
Volymviskositeten kan mätas med en akustisk reometer .
Skenbar viskositet är en beräkning härledd från tester utförda på borrvätska som används i olje- eller gasbrunnar. Dessa beräkningar och tester hjälper ingenjörer att utveckla och underhålla egenskaperna hos borrvätskan enligt de specifikationer som krävs.
Nanoviskositet (viskositet avkänd av nanoprober) kan mätas med fluorescenskorrelationsspektroskopi .
Enheter
SI - enheten för dynamisk viskositet är newton -sekund per kvadratmeter (N·s/m 2 ), också ofta uttryckt i ekvivalenta former pascal - sekund (Pa·s), kilogram per meter per sekund (kg·m −1 ·s −1 ) och Poiseuilli (Pl). CGS - enheten är poisen ( P, eller g·cm −1 ·s −1 = 0,1 Pa·s), uppkallad efter Jean Léonard Marie Poiseuille . Det uttrycks vanligtvis, särskilt i ASTM - standarder, som centipoise (cP). Centipoise är bekvämt eftersom viskositeten för vatten vid 20 °C är cirka 1 cP, och en centipoise är lika med SI millipascal sekund (mPa·s).
SI-enheten för kinematisk viskositet är kvadratmeter per sekund (m 2 /s), medan CGS-enheten för kinematisk viskositet är stokes (St, eller cm 2 ·s −1 = 0,0001 m 2 ·s −1 ), uppkallad efter Sir George Gabriel Stokes . I amerikansk användning används stoke ibland som singularis. Submultipelcentistokes ( cSt ) används ofta istället, 1 cSt = 1 mm 2 ·s −1 = 10 −6 m 2 ·s −1 . Den kinematiska viskositeten för vatten vid 20 °C är cirka 1 cSt.
De vanligaste systemen för amerikanska sedvanliga, eller imperialistiska enheter, är British Gravitational (BG) och English Engineering (EE). I BG-systemet har dynamisk viskositet enheter av pund -sekunder per kvadratfot (lb·s/ft 2 ), och i EE-systemet har den enheter av pund-kraft -sekunder per kvadratfot (lbf·s/ft 2 ) . Pund och pundkraft är likvärdiga; de två systemen skiljer sig bara åt i hur kraft och massa definieras. I BG-systemet är pundet en grundläggande enhet från vilken massaenheten ( snigeln ) definieras av Newtons andra lag , medan kraft- och massaenheterna i EE-systemet (pundkraft respektive pundmassa ) är definieras oberoende genom den andra lagen med hjälp av proportionalitetskonstanten g c .
Kinematisk viskositet har enheter av kvadratfot per sekund (ft 2 /s) i både BG- och EE-systemen.
Icke-standardiserade enheter inkluderar Reyn , en brittisk enhet för dynamisk viskositet. Inom bilindustrin används viskositetsindex för att beskriva förändringen av viskositet med temperatur.
Den reciproka av viskositet är fluiditet , vanligtvis symboliserad av eller , beroende på vilken konvention som används, mätt i reciprok balans (P −1 , eller cm · s · g −1 ), ibland kallad rhe . Fluiditet används sällan i ingenjörspraktik .
En gång i tiden förlitade sig petroleumindustrin på att mäta kinematisk viskositet med hjälp av Saybolt-viskosimetern och uttrycka kinematisk viskositet i enheter av Saybolt universal seconds (SUS). Andra förkortningar som SSU ( Saybolt seconds universal ) eller SUV ( Saybolt universal viscosity ) används ibland. Kinematisk viskositet i centistokes kan konverteras från SUS enligt aritmetiken och referenstabellen i ASTM D 2161.
Molekylärt ursprung
Momentumtransport i gaser förmedlas av diskreta molekylära kollisioner, och i vätskor av attraktionskrafter som binder molekyler nära varandra. På grund av detta är den dynamiska viskositeten hos vätskor vanligtvis mycket större än för gaser. Dessutom tenderar viskositeten att öka med temperaturen i gaser och minska med temperaturen i vätskor.
Ovanför den kritiska punkten för vätskegas ersätts vätske- och gasfasen med en enda superkritisk fas . I denna regim interpolerar mekanismerna för momentumtransport mellan vätskeliknande och gasliknande beteende. Till exempel, längs en superkritisk isobar (yta med konstant tryck), minskar den kinematiska viskositeten vid låg temperatur och ökar vid hög temperatur, med ett minimum däremellan. En grov uppskattning av värdet på minimum är
där är Plancks konstant , är elektronmassan och är molekylmassan.
I allmänhet beror dock ett systems viskositet i detalj på hur molekylerna som utgör systemet interagerar, och det finns inga enkla men korrekta formler för det. De enklaste exakta uttrycken är Green–Kubo-relationerna för linjär skjuvningsviskositet eller transienttidskorrelationsfunktionsuttrycken som härleddes av Evans och Morriss 1988. Även om dessa uttryck är exakta, kräver beräkning av viskositeten för en tät vätska med dessa relationer för närvarande användning av molekylär dynamik datorsimuleringar. Något mer framsteg kan göras för en utspädd gas, eftersom elementära antaganden om hur gasmolekyler rör sig och interagerar leder till en grundläggande förståelse av viskositetens molekylära ursprung. Mer sofistikerade behandlingar kan konstrueras genom att systematiskt grovkorniga gasmolekylernas rörelseekvationer . Ett exempel på en sådan behandling är Chapman–Enskog-teorin , som härleder uttryck för en utspädd gass viskositet från Boltzmann-ekvationen .
Rena gaser
Elementär beräkning av viskositet för en utspädd gas Betrakta en utspädd gas som rör sig parallellt med -axeln med en hastighet som endast beror på koordinaten. För att förenkla diskussionen antas gasen ha enhetlig temperatur och densitet.
Under dessa antaganden är hastigheten för en molekyl som passerar lika med vilken hastighet den molekylen hade när dess genomsnittliga fria väg började. Eftersom den vanligtvis är liten jämfört med makroskopiska skalor, har medelhastigheten för en sådan molekyl formen
där är en numerisk konstant i storleksordningen . (Vissa författare uppskattar ; å andra sidan ger en mer noggrann beräkning för stela elastiska sfärer .) Därefter, eftersom hälften av molekylerna på vardera sidan rör sig mot , och gör det i genomsnitt med hälften av den genomsnittliga molekylära hastigheten , momentumflödet från vardera sidan är
Nettomomentumflödet vid är skillnaden mellan de två:
Enligt definitionen av viskositet bör detta momentumflöde vara lika med , vilket leder till
Viskositeten i gaser uppstår huvudsakligen från den molekylära diffusionen som transporterar rörelsemängd mellan flödesskikten. En elementär beräkning för en utspädd gas vid temperatur och densitet ger
där är Boltzmann-konstanten , molekylmassan och en numerisk konstant i storleksordningen . Kvantiteten , den genomsnittliga fria vägen , mäter det genomsnittliga avståndet en molekyl färdas mellan kollisioner. Även utan a priori kunskap om har detta uttryck icke-triviala implikationer. I synnerhet, eftersom den typiskt är omvänt proportionell mot densiteten och ökar med temperaturen, bör den själv öka med temperaturen och vara oberoende av densiteten vid fast temperatur. Faktum är att båda dessa förutsägelser kvarstår i mer sofistikerade behandlingar och beskriver exakt experimentella observationer. Däremot minskar vätskeviskositeten typiskt med temperaturen.
För stela elastiska sfärer av diameter , kan beräknas, ger
I detta fall är oberoende av temperatur, så . För mer komplicerade molekylära modeller beror dock på temperaturen på ett icke-trivialt sätt, och enkla kinetiska argument som används här är otillräckliga. Mer fundamentalt blir uppfattningen om en medelfri väg oprecis för partiklar som interagerar över ett begränsat område, vilket begränsar användbarheten av konceptet för att beskriva verkliga gaser.
Chapman–Enskogs teori
En teknik som utvecklades av Sydney Chapman och David Enskog i början av 1900-talet möjliggör en mer förfinad beräkning av . Den är baserad på Boltzmann-ekvationen , som ger en statistisk beskrivning av en utspädd gas i termer av intermolekylära interaktioner. Tekniken tillåter noggrann beräkning av molekylära modeller som är mer realistiska än stela elastiska sfärer, såsom de som innehåller intermolekylära attraktioner. Att göra det är nödvändigt för att reproducera det korrekta temperaturberoendet av , vilka experiment visar ökar snabbare än den trend som förutspås för stela elastiska sfärer. Chapman–Enskog-analysen visar faktiskt att det förutspådda temperaturberoendet kan justeras genom att variera parametrarna i olika molekylära modeller. Ett enkelt exempel är Sutherland-modellen, som beskriver stela elastiska sfärer med svag ömsesidig attraktion. I ett sådant fall kan attraktionskraften behandlas störande , vilket leder till ett enkelt uttryck för :
där är oberoende av temperatur och bestäms endast av parametrarna för den intermolekylära attraktionen. För att koppla till experiment är det bekvämt att skriva om som
var är viskositeten vid temperatur . Om det är känt från experiment vid och minst en annan temperatur, då kan beräknas. Uttryck för erhållna på detta sätt är kvalitativt korrekta för ett antal enkla gaser. Något mer sofistikerade modeller, såsom Lennard-Jones potential , kan ge bättre överensstämmelse med experiment, men bara till priset av ett mer ogenomskinligt beroende av temperatur. I vissa system måste antagandet om sfärisk symmetri också överges, vilket är fallet för ångor med mycket polära molekyler som H 2 O . I dessa fall är Chapman–Enskog-analysen betydligt mer komplicerad.
Bulkviskositet
I den kinetisk-molekylära bilden uppstår en bulkviskositet som inte är noll i gaser närhelst det finns icke-försumbara relaxationstidsskalor som styr energiutbytet mellan molekylers translationsenergi och deras inre energi, t.ex. rotations- och vibrationsenergi . Som sådan är bulkviskositeten för en monoatomisk idealgas, i vilken den inre energin hos molekyler är försumbar, men är icke-noll för en gas som koldioxid , vars molekyler har både rotations- och vibrationsenergi.
Rena vätskor
Till skillnad från gaser finns det ingen enkel men korrekt bild för det molekylära ursprunget till viskositet i vätskor.
På den enklaste beskrivningsnivån motverkas den relativa rörelsen av intilliggande skikt i en vätska främst av attraktiva molekylära krafter som verkar över skiktgränsen. På den här bilden förväntar man sig (korrekt) att viskositeten minskar med ökande temperatur. Detta beror på att ökad temperatur ökar den slumpmässiga termiska rörelsen hos molekylerna, vilket gör det lättare för dem att övervinna sina attraktiva interaktioner.
Med utgångspunkt i denna visualisering kan en enkel teori konstrueras i analogi med den diskreta strukturen hos ett fast ämne: grupper av molekyler i en vätska visualiseras som att de bildar "burar" som omger och omsluter enstaka molekyler. Dessa burar kan vara upptagna eller obesatta, och starkare molekylär attraktion motsvarar starkare burar. På grund av slumpmässig termisk rörelse "hoppar" en molekyl mellan burar med en hastighet som varierar omvänt med styrkan hos molekylära attraktioner. I jämvikt är dessa "hopp" inte partiska i någon riktning. Å andra sidan, för att två intilliggande lager ska kunna röra sig i förhållande till varandra, måste "hoppen" vara förspända i den relativa rörelsens riktning. Kraften som krävs för att upprätthålla denna riktade rörelse kan uppskattas för en given skjuvhastighet, vilket leder till
-
( 1 )
där är Avogadro-konstanten , är Planck-konstanten , är volymen av en mol vätska och är den normala kokpunkten . Detta resultat har samma form som det välkända empiriska sambandet
-
( 2 )
var och är konstanter passar från data. Å andra sidan uttrycker flera författare försiktighet med avseende på denna modell. Fel så stora som 30 % kan påträffas med ekvation ( 1 ), jämfört med anpassning av ekvation ( 2 ) till experimentella data. Mer fundamentalt har de fysiska antagandena som ligger bakom ekvationen ( 1 ) kritiserats. Det har också hävdats att det exponentiella beroendet i ekvation ( 1 ) inte nödvändigtvis beskriver experimentella observationer mer exakt än enklare, icke-exponentiella uttryck.
Mot bakgrund av dessa brister är utvecklingen av en mindre ad hoc-modell en fråga av praktiskt intresse. Utanför enkelhet till förmån för precision är det möjligt att skriva rigorösa uttryck för viskositet med utgångspunkt från de grundläggande rörelseekvationerna för molekyler. Ett klassiskt exempel på detta tillvägagångssätt är Irving–Kirkwood-teorin. Å andra sidan ges sådana uttryck som medelvärden över multipartikelkorrelationsfunktioner och är därför svåra att tillämpa i praktiken.
I allmänhet verkar empiriskt härledda uttryck (baserat på befintliga viskositetsmätningar) vara det enda konsekvent tillförlitliga sättet att beräkna viskositet i vätskor.
Blandningar och blandningar
Gasformiga blandningar
Samma molekylärkinetiska bild av en enkomponentgas kan också appliceras på en gasblandning. Till exempel, i Chapman–Enskog-metoden kan viskositeten för en binär blandning av gaser skrivas i termer av de individuella komponentviskositeterna , deras respektive volymfraktioner och de intermolekylära interaktionerna. När det gäller enkomponentgasen kommer beroendet av parametrarna för de intermolekylära interaktionerna in genom olika kollisionsintegraler som kanske inte kan uttryckas i termer av elementära funktioner. För att erhålla användbara uttryck för vilka rimligen matchar experimentella data, måste kollisionsintegralerna typiskt utvärderas med hjälp av någon kombination av analytisk beräkning och empirisk anpassning. Ett exempel på en sådan procedur är Sutherland-metoden för enkomponentgasen, diskuterad ovan.
Blandningar av vätskor
När det gäller rena vätskor är viskositeten hos en vätskeblandning svår att förutsäga utifrån molekylära principer. En metod är att utvidga den molekylära "bur"-teorin som presenteras ovan för en ren vätska. Detta kan göras med olika nivåer av sofistikering. Ett uttryck som är ett resultat av en sådan analys är Lederer-Roegiers ekvation för en binär blandning:
där är en empirisk parameter, och och är respektive molfraktioner och viskositeter för vätskorna.
Eftersom blandning är en viktig process inom smörj- och oljeindustrin, finns det en mängd olika empiriska och lämplighetsekvationer för att förutsäga en blandnings viskositet.
Lösningar och suspensioner
Vattenlösningar
Beroende på löst ämne och koncentrationsintervall kan en vattenhaltig elektrolytlösning ha antingen en större eller mindre viskositet jämfört med rent vatten vid samma temperatur och tryck. Till exempel har en 20 % saltlösning ( natriumklorid ) en viskositet som är över 1,5 gånger den för rent vatten, medan en 20 % kaliumjodidlösning har en viskositet på ungefär 0,91 gånger den för rent vatten.
En idealiserad modell av utspädda elektrolytiska lösningar leder till följande förutsägelse för en lösnings viskositet:
var är lösningsmedlets viskositet, är koncentrationen och är en positiv konstant som beror på både lösningsmedels- och lösta ämnens egenskaper. Detta uttryck är dock endast giltigt för mycket utspädda lösningar som har mindre än 0,1 mol/L. För högre koncentrationer är ytterligare termer nödvändiga som står för högre ordningens molekylära korrelationer:
var och passar från data. I synnerhet kan ett negativt värde av förklara den minskning i viskositet som observerats i vissa lösningar. Uppskattade värden för dessa konstanter visas nedan för natriumklorid och kaliumjodid vid temperatur 25 °C (mol = mol , L = liter ).
| Lösligt ämne | (mol −1/2 L 1/2 ) | (mol −1 L) | (mol −2 L 2 ) |
|---|---|---|---|
| Natriumklorid (NaCl) | 0,0062 | 0,0793 | 0,0080 |
| Kaliumjodid (KI) | 0,0047 | -0,0755 | 0,0000 |
Upphängningar
I en suspension av fasta partiklar (t.ex. mikronstora sfärer suspenderade i olja) kan en effektiv viskositet definieras i termer av spännings- och töjningskomponenter som är medelvärde över en volym som är stor jämfört med avståndet mellan de suspenderade partiklarna, men liten med avseende på till makroskopiska dimensioner. Sådana suspensioner uppvisar i allmänhet icke-newtonskt beteende. Men för utspädda system i stadiga flöden är beteendet Newtonskt och uttryck för kan härledas direkt från partikeldynamiken. I ett mycket utspätt system, med volymfraktion , kan interaktioner mellan de suspenderade partiklarna ignoreras. I ett sådant fall kan man explicit beräkna flödesfältet runt varje partikel oberoende och kombinera resultaten för att få . För sfärer resulterar detta i Einsteins ekvation:
var är viskositeten för den suspenderande vätskan. Det linjära beroendet av är en konsekvens av att man försummar interpartikelinteraktioner. För utspädda system i allmänhet förväntar man sig att ta formen
där koefficienten kan bero på partikelformen (t.ex. sfärer, stavar, skivor). Experimentell bestämning av det exakta värdet av är dock svårt: även förutsägelsen för sfärer har inte slutgiltigt validerats, med olika experiment som hittade värden i intervallet . Denna brist har tillskrivits svårigheter att kontrollera experimentella förhållanden.
I tätare suspensioner, förvärvar ett icke-linjärt beroende av , vilket indikerar vikten av interpartikelinteraktioner. Olika analytiska och semi-empiriska system finns för att fånga denna regim. På den mest grundläggande nivån läggs en term kvadratisk in till :
och koefficienten är anpassad från experimentella data eller approximerad från den mikroskopiska teorin. Vissa författare råder dock till försiktighet vid tillämpning av sådana enkla formler eftersom icke-newtonskt beteende uppträder i täta suspensioner ( för sfärer), eller i suspensioner av långsträckta eller flexibla partiklar.
Det finns en skillnad mellan en suspension av fasta partiklar, som beskrivs ovan, och en emulsion . Den senare är en suspension av små droppar, som själva kan uppvisa inre cirkulation. Närvaron av intern cirkulation kan minska den observerade effektiva viskositeten, och olika teoretiska eller semi-empiriska modeller måste användas.
Amorfa material

I de höga och låga temperaturgränserna har viskös flöde i amorfa material (t.ex. i glas och smältor) Arrhenius-formen :
där Q är en relevant aktiveringsenergi , givet i termer av molekylära parametrar; T är temperatur; R är den molära gaskonstanten ; och A är ungefär en konstant. Aktiveringsenergin Q tar ett annat värde beroende på om den höga eller låga temperaturgränsen beaktas: den ändras från ett högt värde Q H vid låga temperaturer (i glasartat tillstånd) till ett lågt värde Q L vid höga temperaturer (i flytande tillstånd).
För mellantemperaturer, varierar icke trivialt med temperaturen och den enkla Arrhenius-formen misslyckas. Å andra sidan tvåexponentiella ekvationen
där , , , alla är konstanter, ger en bra anpassning till experimentella data över hela temperaturintervallet, samtidigt som det reduceras till korrekt Arrhenius-form i de låga och höga temperaturgränserna. Detta uttryck kan motiveras från olika teoretiska modeller av amorfa material på atomnivå.
En tvåexponentiell ekvation för viskositeten kan härledas inom Dyre shoving-modellen av underkylda vätskor, där Arrhenius-energibarriären identifieras med den högfrekventa skjuvmodulen gånger en karakteristisk tryckvolym. Vid specificering av temperaturberoendet för skjuvmodulen via termisk expansion och via den repulsiva delen av den intermolekylära potentialen, hämtas en annan tvåexponentiell ekvation:
där betecknar högfrekvensskjuvmodulen för materialet utvärderad vid en temperatur som är lika med glasövergångstemperaturen , är den så kallade shoving-volymen, dvs det är den karakteristiska volymen för gruppen av atomer som är involverade i shoving-händelsen genom vilken en atom /molekyl flyr från buren hos närmaste grannar, vanligtvis i storleksordningen av volymen som upptas av få atomer. Dessutom är den termiska expansionskoefficienten för materialet, är en parameter som mäter brantheten i kraftlagshöjningen av den uppåtgående flanken av den första toppen av den radiella fördelningsfunktionen , och är kvantitativt relaterad till den repulsiva delen av den interatomära potentialen . Slutligen betecknar Boltzmann-konstanten .
Eddy viskositet
I studien av turbulens i vätskor är en vanlig praktisk strategi att ignorera de småskaliga virvlarna (eller virvlarna ) i rörelsen och att beräkna en storskalig rörelse med en effektiv viskositet, kallad "virvelviskositeten", som kännetecknar transport och förlust av energi i det mindre flödet (se simulering av stor virvel ). I motsats till själva vätskans viskositet, som måste vara positiv enligt termodynamikens andra lag , kan virvelviskositeten vara negativ.
Förutsägelse
Eftersom viskositeten kontinuerligt beror på temperatur och tryck, kan den inte helt karakteriseras av ett begränsat antal experimentella mätningar. Prediktiva formler blir nödvändiga om experimentella värden inte är tillgängliga vid de temperaturer och tryck som är av intresse. Denna förmåga är viktig för termofysiska simuleringar, där temperaturen och trycket hos en vätska kan variera kontinuerligt med rum och tid. En liknande situation påträffas för blandningar av rena vätskor, där viskositeten kontinuerligt beror på koncentrationsförhållandena för de ingående vätskorna
För de enklaste vätskorna, såsom utspädda monoatomiska gaser och deras blandningar, kan ab initio kvantmekaniska beräkningar exakt förutsäga viskositet i termer av fundamentala atomkonstanter, dvs utan hänvisning till befintliga viskositetsmätningar. För det speciella fallet med utspätt helium är osäkerheterna i den ab initio beräknade viskositeten två storleksordningar mindre än osäkerheterna i experimentella värden.
För de flesta vätskor är sådana högnoggranna beräkningar av de första principerna inte möjliga. Snarare måste teoretiska eller empiriska uttryck anpassas till befintliga viskositetsmätningar. Om ett sådant uttryck är lämpligt för högtrohetsdata över ett stort område av temperaturer och tryck, så kallas det en "referenskorrelation" för den vätskan. Referenskorrelationer har publicerats för många rena vätskor; några exempel är vatten , koldioxid , ammoniak , bensen och xenon . Många av dessa täcker temperatur- och tryckområden som omfattar gas-, vätske- och superkritiska faser.
Termofysisk modelleringsprogram förlitar sig ofta på referenskorrelationer för att förutsäga viskositet vid användarspecificerad temperatur och tryck. Dessa korrelationer kan vara proprietära . Exempel är REFPROP (proprietärt) och CoolProp (öppen källkod).
Viskositeten kan också beräknas med hjälp av formler som uttrycker den i termer av statistik över individuella partikelbanor. Dessa formler inkluderar Green-Kubo-relationerna för linjär skjuvningsviskositet och transienta tidskorrelationsfunktionsuttryck som härleddes av Evans och Morriss 1988. Fördelen med dessa uttryck är att de formellt är exakta och giltiga för allmänna system. Nackdelen är att de kräver detaljerad kunskap om partikelbanor, endast tillgängliga i beräkningsmässigt dyra simuleringar som molekylär dynamik . En noggrann modell för interpartikelinteraktioner krävs också, vilket kan vara svårt att få fram för komplexa molekyler.
Utvalda ämnen

Observerade viskositetsvärden varierar över flera storleksordningar, även för vanliga ämnen (se storleksordningen nedan). Till exempel har en 70-procentig sackaroslösning (socker) en viskositet som är över 400 gånger den för vatten och 26 000 gånger den för luft. Mer dramatiskt har beck uppskattats ha en viskositet som är 230 miljarder gånger den för vatten.
Vatten
Vattens dynamiska viskositet är cirka 0,89 mPa·s vid rumstemperatur (25 °C). Som en funktion av temperaturen i kelvin kan viskositeten uppskattas med den semi-empiriska Vogel-Fulcher-Tammann-ekvationen :
där A = 0,02939 mPa·s, B = 507,88 K och C = 149,3 K. Experimentellt bestämda värden på viskositeten ges också i tabellen nedan. Värdena vid 20 °C är en användbar referens: där är den dynamiska viskositeten cirka 1 cP och den kinematiska viskositeten är cirka 1 cSt.
| Temperatur (°C) | Viskositet (mPa·s eller cP) |
|---|---|
| 10 | 1,3059 |
| 20 | 1,0016 |
| 30 | 0,79722 |
| 50 | 0,54652 |
| 70 | 0,40355 |
| 90 | 0,31417 |
Luft
Under standardatmosfäriska förhållanden (25 °C och ett tryck på 1 bar), är luftens dynamiska viskositet 18,5 μPa·s, ungefär 50 gånger mindre än viskositeten för vatten vid samma temperatur. Förutom vid mycket högt tryck beror luftens viskositet mest på temperaturen. Bland de många möjliga ungefärliga formlerna för temperaturberoendet (se Viskositetens temperaturberoende ) är en:
vilket är noggrant i intervallet -20 °C till 400 °C. För att denna formel ska vara giltig måste temperaturen anges i kelvin ; motsvarar då viskositeten i Pa·s.

Andra vanliga ämnen
| Ämne | Viskositet (mPa·s) | Temperatur (°C) | Ref. |
|---|---|---|---|
| Bensen | 0,604 | 25 | |
| Vatten | 1,0016 | 20 | |
| Merkurius | 1,526 | 25 | |
| Helmjölk | 2.12 | 20 | |
| Mörk öl | 2,53 | 20 | |
| Olivolja | 56,2 | 26 | |
| Honung | 2000–10000 | 20 | |
| Ketchup | 5000–20000 | 25 | |
| Jordnötssmör | 10 4 –10 6 | ||
| Tonhöjd | 2,3 × 10 11 | 10–30 (variabel) |
Uppskattningar av storleksordning
Följande tabell illustrerar intervallet av viskositetsvärden som observerats i vanliga ämnen. Om inget annat anges antas en temperatur på 25 °C och ett tryck på 1 atmosfär.
Värdena som anges är endast representativa uppskattningar, eftersom de inte tar hänsyn till mätosäkerheter, variationer i materialdefinitioner eller icke-newtonskt beteende.
| Faktor (Pa·s) | Beskrivning | Exempel | Värden (Pa·s) | Ref. |
|---|---|---|---|---|
| 10 −6 | Lägre område för gasformig viskositet |
Butan | 7,49 × 10 −6 | |
| Väte | 8,8 × 10 −6 | |||
| 10 −5 | Övre intervall för gasformig viskositet | Krypton | 2,538 × 10 −5 | |
| Neon | 3,175 × 10 −5 | |||
| 10 −4 | Lägre område för vätskeviskositet | Pentan | 2,24 × 10 −4 | |
| Bensin | 6 × 10 −4 | |||
| Vatten | 8,90 × 10 −4 | |||
| 10 −3 | Typiskt intervall för småmolekylära newtonska vätskor |
Etanol | 1,074 × 10 −3 | |
| Merkurius | 1,526 × 10 −3 | |||
| Helmjölk (20 °C) | 2,12 × 10 −3 | |||
| Blod | 3 × 10 −3 till 6 × 10 −3 | |||
| Flytande stål (1550 °C) | 6 × 10 −3 | |||
| 10 −2 – 10 0 | Oljor och långkedjiga kolväten | Linfröolja | 0,028 | |
| Oljesyra | 0,036 | |||
| Olivolja | 0,084 | |||
| SAE 10 Motorolja | 0,085 till 0,14 | |||
| ricinolja | 0,1 | |||
| SAE 20 Motorolja | 0,14 till 0,42 | |||
| SAE 30 Motorolja | 0,42 till 0,65 | |||
| SAE 40 Motorolja | 0,65 till 0,90 | |||
| Glycerin | 1.5 | |||
| Pannkakssirap | 2.5 | |||
| 10 1 – 10 3 | Pastor, geler och andra halvfasta ämnen (i allmänhet icke-newtonska) |
Ketchup | ≈ 10 1 | |
| Senap | ||||
| Gräddfil | ≈ 10 2 | |||
| Jordnötssmör | ||||
| Ister | ≈ 10 3 | |||
| ≈10 8 | Viskoelastiska polymerer | Tonhöjd | 2,3 × 10 8 | |
| ≈10 21 | Vissa fasta ämnen under en viskoelastisk beskrivning |
Mantel (geologi) | ≈ 10 19 till 10 24 |
Se även
- Dashpot
- Deborah nummer
- Dilatant
- Herschel–Bulkley vätska
- Blandare med hög viskositet
- Hyperviskositetssyndrom
- Inre viskositet
- Inviscid flöde
- Joback-metod (uppskattning av vätskeviskositet från molekylstruktur)
- Kaye effekt
- Mikroviskositet
- Morton nummer
- Oljetryck
- Kvasi-solid
- Reologi
- Stokes flödar
- Superfluid helium-4
- Viskoplasticitet
- Viskositetsmodeller för blandningar
- Zahn kopp
Referenser
Fotnoter
Citat
Källor
- Abdulagatov, Ilmutdin M.; Zeinalova, Adelya B.; Azizov, Nazim D. (2006). "Experimentella viskositets B-koefficienter för vattenhaltiga LiCl-lösningar". Journal of Molecular Liquids . 126 (1–3): 75–88. doi : 10.1016/j.molliq.2005.10.006 . ISSN 0167-7322 .
- Assael, MJ; et al. (2018). "Referensvärden och referenskorrelationer för vätskors värmeledningsförmåga och viskositet" . Journal of Physical and Chemical Reference Data . 47 (2): 021501. Bibcode : 2018JPCRD..47b1501A . doi : 10.1063/1.5036625 . ISSN 0047-2689 . PMC 6463310 . PMID 30996494 .
- Avgeri, S.; Assael, MJ; Huber, ML; Perkins, RA (2014). "Referenskorrelation av viskositeten för bensen från trippelpunkten till 675 K och upp till 300 MPa". Journal of Physical and Chemical Reference Data . AIP-publicering. 43 (3): 033103. Bibcode : 2014JPCRD..43c3103A . doi : 10.1063/1.4892935 . ISSN 0047-2689 .
- Balescu, Radu (1975). Jämvikts- och icke-jämviktsstatistisk mekanik . John Wiley & Sons. ISBN 978-0-471-04600-4. Arkiverad från originalet 2020-03-16 . Hämtad 2019-09-18 .
- Bell, Ian H.; Wronski, Jorrit; Quoilin, Sylvain; Lemort, Vincent (2014-01-27). "Ren och pseudo-ren vätska termofysisk egenskapsutvärdering och öppen källkod för termofysiska egenskapsbibliotek CoolProp" . Industriell och teknisk kemiforskning . American Chemical Society (ACS). 53 (6): 2498–2508. doi : 10.1021/ie4033999 . ISSN 0888-5885 . PMC 3944605 . PMID 24623957 .
- Bellac, Michael; Mortessagne, Fabrice; Batrouni, G. George (2004). Jämvikts- och icke-jämviktsstatistisk termodynamik . Cambridge University Press. ISBN 978-0-521-82143-8.
- Bird, R. Byron; Stewart, Warren E.; Lightfoot, Edwin N. (2007). Transportfenomen (2:a uppl.). John Wiley & Sons, Inc. ISBN 978-0-470-11539-8. Arkiverad från originalet 2020-03-02 . Hämtad 2019-09-18 .
- Bird, R. Bryon; Armstrong, Robert C.; Hassager, Ole (1987), Dynamics of Polymeric Liquids, Volym 1: Fluid Mechanics (2:a upplagan), John Wiley & Sons
- Cercignani, Carlo (1975). Teori och tillämpning av Boltzmann-ekvationen . Elsevier. ISBN 978-0-444-19450-3.
- Chapman, Sydney ; Cowling, TG (1970). The Mathematical Theory of Non-Uniform Gases (3:e upplagan). Cambridge University Press. ISBN 9780521075770.
- Citerne, Guillaume P.; Carreau, Pierre J.; Moan, Michel (2001). "Reologiska egenskaper hos jordnötssmör". Rheologica Acta . 40 (1): 86–96. doi : 10.1007/s003970000120 . S2CID 94555820 .
- Cramer, MS (2012). "Numeriska uppskattningar för bulkviskositeten för idealgaser" . Vätskors fysik . 24 (6): 066102–066102–23. Bibcode : 2012PhFl...24f6102C . doi : 10.1063/1.4729611 . hdl : 10919/47646 . Arkiverad från originalet 2022-02-15 . Hämtad 2020-09-19 .
- Doremus, RH (2002). "Viskositet av kiseldioxid". J. Appl. Phys . 92 (12): 7619–7629. Bibcode : 2002JAP....92.7619D . doi : 10.1063/1.1515132 .
- Dyre, JC; Olsen, NB; Christensen, T. (1996). "Lokal elastisk expansionsmodell för aktiveringsenergier för viskös flöde av glasbildande molekylära vätskor" . Fysisk granskning B . 53 (5): 2171–2174. Bibcode : 1996PhRvB..53.2171D . doi : 10.1103/PhysRevB.53.2171 . PMID 9983702 .
- Edgeworth, R.; Dalton, BJ; Parnell, T. (1984). "Pitch drop-experimentet" . European Journal of Physics . 5 (4): 198–200. Bibcode : 1984EJPh....5..198E . doi : 10.1088/0143-0807/5/4/003 . S2CID 250769509 . Arkiverad från originalet 2013-03-28 . Hämtad 2009-03-31 .
- Egelstaff, PA (1992). An Introduction to the Liquid State (2nd ed.). Oxford University Press. ISBN 978-0-19-851012-3.
- Evans, Denis J .; Morriss, Gary P. (2007). Statistical Mechanics of Nonequilibrium Liquids . ANU Tryck. ISBN 9781921313226. JSTOR j.ctt24h99q . Arkiverad från originalet 2022-01-10 . Hämtad 2022-01-10 .
- Evans, Denis J.; Morriss, Gary P. (15 oktober 1988). "Transient-tid-korrelationsfunktioner och vätskors reologi". Fysisk granskning A . 38 (8): 4142–4148. Bibcode : 1988PhRvA..38.4142E . doi : 10.1103/PhysRevA.38.4142 . PMID 9900865 .
- Fellows, PJ (2009). Food Processing Technology: Principles and Practice (3:e upplagan). Woodhead. ISBN 978-1845692162.
- Fluegel, Alexander (2007). "Viskositetsberäkning av glasögon" . Glasproperties.com. Arkiverad från originalet 2010-11-27 . Hämtad 2010-09-14 .
- Gibbs, Philip (januari 1997). "Är glas flytande eller fast?" . math.ucr.edu . Arkiverad från originalet den 29 mars 2007 . Hämtad 19 september 2019 .
- Gyllenbok, Jan (2018). "Encyclopaedia of Historical Metrology, Weights and Measures: Volume 1". Encyclopaedia of Historical Metrology, Weights and Measures . Vol. 1. Birkhäuser. ISBN 9783319575988.
- Hannan, Henry (2007). Teknikerns formuleringshandbok för industri- och hushållsrengöringsprodukter . Waukesha, Wisconsin: Kyral LLC. sid. 7. ISBN 978-0-6151-5601-9.
- Hecksher, Tina; Dyre, Jeppe C. (2015-01-01). "En genomgång av experiment som testar shoving-modellen" . Journal of Non-Crystalline Solids . 7:e IDMRCS: Avslappning i komplexa system. 407 : 14–22. Bibcode : 2015JNCS..407...14H . doi : 10.1016/j.jnoncrysol.2014.08.056 . ISSN 0022-3093 . Arkiverad från originalet 2022-02-15 . Hämtad 2021-10-17 .
- Hildebrand, Joel Henry (1977). Viskositet och diffusivitet: en prediktiv behandling . John Wiley & Sons. ISBN 978-0-471-03072-0.
- Holman, Jack Philip (2002). Värmeöverföring . McGraw-Hill. ISBN 978-0-07-112230-6. Arkiverad från originalet 2020-03-15 . Hämtad 2019-09-18 .
- Huber, ML; Perkins, RA; Laesecke, A.; Vän, GD; Sengers, JV; Assael, MJ; Metaxa, IN; Vogel, E.; Mareš, R.; Miyagawa, K. (2009). "Ny internationell formulering för viskositeten av H2O". Journal of Physical and Chemical Reference Data . AIP-publicering. 38 (2): 101–125. Bibcode : 2009JPCRD..38..101H . doi : 10.1063/1.3088050 . ISSN 0047-2689 .
- Incropera, Frank P.; et al. (2007). Grunderna för värme- och massöverföring . Wiley. ISBN 978-0-471-45728-2. Arkiverad från originalet 2020-03-11 . Hämtad 2019-09-18 .
- Irving, JH; Kirkwood, John G. (1949). "Den statistiska mekaniska teorin om transportprocesser. IV. Hydrodynamikens ekvationer". J. Chem. Phys . 18 (6): 817–829. doi : 10.1063/1.1747782 .
- Kestin, J.; Ro, ST; Wakeham, WA (1972). "Ädelgasernas viskositet i temperaturområdet 25–700°C". The Journal of Chemical Physics . 56 (8): 4119–4124. Bibcode : 1972JChPh..56.4119K . doi : 10.1063/1.1677824 . ISSN 0021-9606 .
- Kestin, J.; Khalifa, HE; Wakeham, WA (1977). "Viskositeten hos fem gasformiga kolväten". The Journal of Chemical Physics . 66 (3): 1132. Bibcode : 1977JChPh..66.1132K . doi : 10.1063/1.434048 .
- Koocheki, Arash; et al. (2009). "Ketchupens reologiska egenskaper som funktion av olika hydrokolloider och temperatur". International Journal of Food Science & Technology . 44 (3): 596–602. doi : 10.1111/j.1365-2621.2008.01868.x .
- Krausser, J.; Samwer, K.; Zaccone, A. (2015). "Interatomisk avstötningsmjukhet styr direkt bräckligheten hos underkylda metalliska smältor" . Proceedings of the National Academy of Sciences of the USA . 112 (45): 13762–13767. arXiv : 1510.08117 . Bibcode : 2015PNAS..11213762K . doi : 10.1073/pnas.1503741112 . PMC 4653154 . PMID 26504208 .
- Kumagai, Naoichi; Sasajima, Sadao; Ito, Hidebumi (15 februari 1978). "Långtidskrypning av stenar: Resultat med stora exemplar erhållna på cirka 20 år och de med små exemplar inom cirka 3 år" . Journal of the Society of Materials Science (Japan) . 27 (293): 157–161. NAID 110002299397 . Arkiverad från originalet 2011-05-21 . Hämtad 2008-06-16 .
- Kwapiszewska, Karina; Szczepański, Krzysztof; Kalwarczyk, Tomasz; Michalska, Bernadeta; Patalas-Krawczyk, Paulina; Szymański, Jędrzej; Andryszewski, Tomasz; Iwan, Michalina; Duszyński, Jerzy; Hołyst, Robert (2020). "Nanoskalaviskositeten hos cytoplasman bevaras i mänskliga cellinjer" . The Journal of Physical Chemistry Letters . 11 (16): 6914–6920. doi : 10.1021/acs.jpclett.0c01748 . PMC 7450658 . PMID 32787203 .
- Laesecke, Arno; Muzny, Chris D. (2017). "Referenskorrelation för koldioxidens viskositet" . Journal of Physical and Chemical Reference Data . AIP-publicering. 46 (1): 013107. Bibcode : 2017JPCRD..46a3107L . doi : 10.1063/1.4977429 . ISSN 0047-2689 . PMC 5514612 . PMID 28736460 .
- Landau, LD ; Lifshitz, EM (1987). Fluid Mechanics (2:a upplagan). Elsevier. ISBN 978-0-08-057073-0. Arkiverad från originalet 2020-03-21 . Hämtad 2019-09-18 .
- Maginn, Edward J.; Messerly, Richard A.; Carlson, Daniel J.; Roe, Daniel R.; Elliott, J. Richard (2019). "Bästa praxis för datatransportegenskaper 1. Självdiffusivitet och viskositet från molekylär jämviktsdynamik [Artikel v1.0]". Living Journal of Computational Molecular Science . University of Colorado i Boulder. 1 (1). doi : 10.33011/livecoms.1.1.6324 . ISSN 2575-6524 . S2CID 104357320 .
- Monogenidou, SA; Assael, MJ; Huber, ML (2018). "Referenskorrelation för ammoniakens viskositet från trippelpunkten till 725 K och upp till 50 MPa" . Journal of Physical and Chemical Reference Data . AIP-publicering. 47 (2): 023102. Bibcode : 2018JPCRD..47b3102M . doi : 10.1063/1.5036724 . ISSN 0047-2689 . PMC 6512859 . PMID 31092958 .
- Lesieur, Marcel (2012). Turbulens i vätskor: Stokastisk och numerisk modellering . Springer. ISBN 978-94-009-0533-7. Arkiverad från originalet 2020-03-14 . Hämtad 2018-11-30 .
- Mewis, Jan; Wagner, Norman J. (2012). Kolloidal suspensionsreologi . Cambridge University Press. ISBN 978-0-521-51599-3. Arkiverad från originalet 2020-03-14 . Hämtad 2018-12-10 .
- McNaught, AD; Wilkinson, A. (1997). "balans". IUPAC. Kompendium för kemisk terminologi ("Guldboken") . SJ Chalk (2:a uppl.). Oxford: Blackwell Scientific. doi : 10.1351/guldbok . ISBN 0-9678550-9-8.
- Millat, Jorgen (1996). Vätskors transportegenskaper: deras korrelation, förutsägelse och uppskattning . Cambridge: Cambridge University Press. ISBN 978-0-521-02290-3. OCLC 668204060 .
- Mueller, S.; Llewellin, EW; Mader, HM (2009). "Reologin hos suspensioner av fasta partiklar" . Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences . 466 (2116): 1201–1228. doi : 10.1098/rspa.2009.0445 . ISSN 1364-5021 .
- Nič, Miloslav; et al., red. (1997). "dynamisk viskositet, η ". IUPAC-kompendium för kemisk terminologi . Oxford: Blackwell Scientific Publications. doi : 10.1351/guldbok . ISBN 978-0-9678550-9-7.
- Ojovan, MI; Lee, WE (2004). "Viskositet för nätverksvätskor inom Doremus-metoden". J. Appl. Phys . 95 (7): 3803–3810. Bibcode : 2004JAP....95.3803O . doi : 10.1063/1.1647260 .
- Ojovan, MI; Travis, KP; Hand, RJ (2007). "Termodynamiska parametrar för bindningar i glasartade material från viskositet-temperaturförhållanden" (PDF) . J. Phys.: Kondens. Materia . 19 (41): 415107. Bibcode : 2007JPCM...19O5107O . doi : 10.1088/0953-8984/19/41/415107 . PMID 28192319 . S2CID 24724512 . Arkiverad (PDF) från originalet 2018-07-25 . Hämtad 2019-09-27 .
- Plumb, Robert C. (1989). "Antika fönsterrutor och flödet av underkylda vätskor" . Journal of Chemical Education . 66 (12): 994. Bibcode : 1989JChEd..66..994P . doi : 10.1021/ed066p994 . Arkiverad från originalet 2005-08-26 . Hämtad 2013-12-25 .
- Rapaport, DC (2004). The Art of Molecular Dynamics Simulation (2:a upplagan). Cambridge University Press. ISBN 9780521825689. Arkiverad från originalet 2018-06-25 . Hämtad 2022-01-10 .
- Reid, Robert C.; Sherwood, Thomas K. (1958). Gaser och vätskors egenskaper . McGraw-Hill.
- Reif, F. (1965), Fundamentals of Statistical and Thermal Physics , McGraw-Hill. En avancerad behandling.
- Rosenson, RS; McCormick, A; Uretz, EF (1996-08-01). "Fördelning av blodviskositetsvärden och biokemiska korrelat hos friska vuxna". Klinisk kemi . Oxford University Press (OUP). 42 (8): 1189–1195. doi : 10.1093/clinchem/42.8.1189 . ISSN 0009-9147 . PMID 8697575 .
- Rowland, Darren; Al Ghafri, Saif ZS; May, Eric F. (2020-03-01). "Breddäckande referenskorrelationer för utspädd gastransportegenskaper baserat på Ab Initio-beräkningar och viskositetsförhållandemätningar" . Journal of Physical and Chemical Reference Data . AIP-publicering. 49 (1): 013101. Bibcode : 2020JPCRD..49a3101X . doi : 10.1063/1.5125100 . ISSN 0047-2689 . S2CID 213794612 .
- Różańska, S.; Różański, J.; Ochowiak, M.; Mitkowski, PT (2014). "Extensionsviskositetsmätningar av koncentrerade emulsioner med användning av den motsatta munstycksanordningen" (PDF) . Brazilian Journal of Chemical Engineering . 31 (1): 47–55. doi : 10.1590/S0104-66322014000100006 . ISSN 0104-6632 . Arkiverad (PDF) från originalet 2020-05-08 . Hämtad 2019-09-19 .
- Rumble, John R., red. (2018). CRC Handbook of Chemistry and Physics (99:e upplagan). Boca Raton, FL: CRC Press. ISBN 978-1138561632.
- Sagdeev, Damir; Gabitov, Il'giz; Isyanov, Chingiz; Khairutdinov, Vener; Farakhov, Mansur; Zaripov, Zufar; Abdulagatov, Ilmutdin (2019-04-22). "Densiteter och viskositeter av oljesyra vid atmosfärstryck". Journal of the American Oil Chemists' Society . Wiley. 96 (6): 647–662. doi : 10.1002/aocs.12217 . ISSN 0003-021X . S2CID 150156106 .
- Scherer, George W.; Pardenek, Sandra A.; Swiatek, Rose M. (1988). "Viskoelasticitet i silikagel". Journal of Non-Crystalline Solids . 107 (1): 14. Bibcode : 1988JNCS..107...14S . doi : 10.1016/0022-3093(88)90086-5 .
- Schroeder, Daniel V. (1999). En introduktion till termisk fysik . Addison Wesley. ISBN 978-0-201-38027-9. Arkiverad från originalet 2020-03-10 . Hämtad 2018-11-30 .
- Sharipov, Felix; Benites, Victor J. (2020-07-01). "Transportkoefficienter för flerkomponentblandningar av ädelgaser baserade på ab initio potentialer: Viskositet och värmeledningsförmåga". Vätskors fysik . AIP-publicering. 32 (7): 077104. arXiv : 2006.08687 . Bibcode : 2020PhFl...32g7104S . doi : 10.1063/5.0016261 . ISSN 1070-6631 . S2CID 219708359 .
- Sivashinsky, V.; Yakhot, G. (1985). "Negativ viskositetseffekt i storskaliga flöden". Vätskors fysik . 28 (4): 1040. Bibcode : 1985PhFl...28.1040S . doi : 10.1063/1.865025 .
- Streeter, Victor Lyle; Wylie, E. Benjamin; Bedford, Keith W. (1998). Vätskemekanik . WCB/McGraw Hill. ISBN 978-0-07-062537-2. Arkiverad från originalet 2020-03-16 . Hämtad 2019-09-18 .
- Sutherland, William (1893). "LII. Viskositeten hos gaser och molekylär kraft" (PDF) . London, Edinburgh och Dublin Philosophical Magazine och Journal of Science . 36 (223): 507–531. doi : 10.1080/14786449308620508 . ISSN 1941-5982 . Arkiverad (PDF) från originalet 2019-07-20 . Hämtad 2019-09-18 .
- Symon, Keith R. (1971). Mekanik (3:e upplagan). Addison-Wesley. ISBN 978-0-201-07392-8. Arkiverad från originalet 2020-03-11 . Hämtad 2019-09-18 .
- Trachenko, K.; Brazhkin, VV (2020-04-22). "Minimal kvantviskositet från grundläggande fysiska konstanter" . Vetenskapens framsteg . American Association for the Advancement of Science (AAAS). 6 (17): eaba3747. arXiv : 1912.06711 . Bibcode : 2020SciA....6.3747T . doi : 10.1126/sciadv.aba3747 . ISSN 2375-2548 . PMC 7182420 . PMID 32426470 .
- Trachenko, Kostya; Brazhkin, Vadim V. (2021-12-01). "Viskositetens kvantmekanik" (PDF) . Fysik idag . AIP-publicering. 74 (12): 66–67. Bibcode : 2021PhT....74l..66T . doi : 10.1063/pt.3.4908 . ISSN 0031-9228 . S2CID 244831744 . Arkiverad (PDF) från originalet 2022-01-10 . Hämtad 2022-01-10 .
- Trouton, Fred. T. (1906). "Om koefficienten för viskös dragkraft och dess förhållande till viskositeten" . Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences . 77 (519): 426–440. Bibcode : 1906RSPSA..77..426T . doi : 10.1098/rspa.1906.0038 . ISSN 1364-5021 .
- Velliadou, Danai; Tasidou, Katerina A.; Antoniadis, Konstantinos D.; Assael, Marc J.; Perkins, Richard A.; Huber, Marcia L. (2021-03-25). "Referenskorrelation för viskositeten för xenon från trippelpunkten till 750 K och upp till 86 MPa" . International Journal of Thermophysics . Springer Science and Business Media LLC. 42 (5): 74. Bibcode : 2021IJT....42...74V . doi : 10.1007/s10765-021-02818-9 . ISSN 0195-928X . PMC 8356199 . PMID 34393314 .
- Viswanath, DS; Natarajan, G. (1989). Databok om vätskors viskositet . Hemisphere Publishing Corporation. ISBN 0-89116-778-1.
- Viswanath, Dabir S.; et al. (2007). Viskositet av vätskor: teori, uppskattning, experiment och data . Springer. ISBN 978-1-4020-5481-5.
- Walzer, Uwe; Hendel, Roland; Baumgardner, John (nd), Mantle Viscosity and the Thickness of the Convective Downwellings , arkiverad från originalet 2007-06-11
- Xie, Hong-Yi; Levchenko, Alex (23 januari 2019). "Negativ viskositet och virvelflöde av den obalanserade elektronhålsvätskan i grafen". Phys. Rev. B. 99 (4): 045434. arXiv : 1807.04770 . Bibcode : 2019PhRvB..99d5434X . doi : 10.1103/PhysRevB.99.045434 . S2CID 51792702 .
- Yanniotis, S.; Skaltsi, S.; Karaburnioti, S. (februari 2006). "Effekt av fukthalt på viskositeten av honung vid olika temperaturer". Journal of Food Engineering . 72 (4): 372–377. doi : 10.1016/j.jfoodeng.2004.12.017 .
- Zhao, Mengjing; Wang, Yong; Yang, Shufeng; Li, Jingshe; Liu, Wei; Song, Zhaoqi (2021). "Flödesbeteende och värmeöverföring av smält stål i en tvåsträngad gjutlåda uppvärmd av plasma". Journal of Materials Research and Technology . Elsevier BV. 13 : 561-572. doi : 10.1016/j.jmrt.2021.04.069 . ISSN 2238-7854 . S2CID 236277034 .
- Zhmud, Boris (2014). "Viskositetsblandningsekvationer" (PDF) . Lube-Tech:93. Lube . Nr 121. s. 22–27. Arkiverad (PDF) från originalet 2018-12-01 . Hämtad 2018-11-30 .
- "NIST Reference Fluid Thermodynamic and Transport Properties Database (REFPROP): Version 10" . Nist . 2018-01-01. Arkiverad från originalet 2021-12-16 . Hämtad 2021-12-23 .
- tec-science (2020-03-25). "Viskositet för vätskor och gaser" . tec-vetenskap . Arkiverad från originalet 2020-04-19 . Hämtad 2020-05-07 .
externa länkar
- Vätskeegenskaper – hög noggrann beräkning av viskositet för ofta förekommande rena vätskor och gaser
- Gasviskositetskalkylator som funktion av temperatur
- Luftviskositetskalkylator som funktion av temperatur och tryck
- Fluid Characteristics Chart – en tabell över viskositeter och ångtryck för olika vätskor
- Gas Dynamics Toolbox – beräkna viskositetskoefficienten för blandningar av gaser
- Glasviskositetsmätning – viskositetsmätning, viskositetsenheter och fixpunkter, glasviskositetsberäkning
- Kinematisk viskositet – omvandling mellan kinematisk och dynamisk viskositet
- Vattens fysiska egenskaper – en tabell över vattnets viskositet som funktion av temperatur
- Vogel–Tammann–Fulchers ekvationsparametrar
- Beräkning av temperaturberoende dynamiska viskositeter för några vanliga komponenter
- "Testprocedurer för att testa motorvägs- och icke-vägsmotorer och tekniska tillägg för omnibus" – United States Environmental Protection Agency
- Artificiell viskositet
- Luftens viskositet, dynamisk och kinematisk, Engineers Edge










![{\displaystyle [\mu ]={\frac {\rm {kg}}{\rm {m\cdot s}}}={\frac {\rm {N}}{\rm {m^{2}} }}\cdot s={\rm {Pa\cdot s}}=}](https://wikimedia.org/api/rest_v1/media/math/render/svg/94672cf9c544af92f8e598bdd2b764795ad29697)








![{\displaystyle [\nu ]={\frac {\rm {m^{2}}}{\rm {s}}}=\mathrm {{\frac {\rm {N\cdot m}}{\rm {kg}}}\cdot s} =\mathrm {{\frac {\rm {J}}{\rm {kg}}}\cdot s} =}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9d3199a04f1776c84ac6126806304099e08dbe61)













![{\displaystyle {\boldsymbol {\tau }}=\mu \left[\nabla \mathbf {v} +(\nabla \mathbf {v} )^{\dolk }\right]-\left({\frac { 2}{3}}\mu -\kappa \right)(\nabla \cdot \mathbf {v} )\mathbf {\delta } ,}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5e5b06e2df4001df52d323172cd43795795fff66)





![{\displaystyle {\begin{aligned}\mathbf {J} &=-D{\frac {\partial \rho }{\partial x}}&&{\text{(Ficks diffusionslag)}}\\[5pt ]\mathbf {q} &=-k_{t}{\frac {\partial T}{\partial x}}&&{\text{(Fouriers lag om värmeledning)}}\\[5pt]\tau &= \mu {\frac {\partial u}{\partial y}}&&{\text{(Newtons viskositetslag)}}\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6380b89b0d24d9c9deb9ef04f333430b073c45cc)


































































![{\displaystyle \mu =AT\exp \left({\frac {B}{RT}}\right)\left[1+C\exp \left({\frac {D}{RT}}\right)\ höger],}](https://wikimedia.org/api/rest_v1/media/math/render/svg/38aa9224e9ac73624655cd20405e140af63a62eb)
![{\displaystyle \mu =\exp {\left\{{\frac {V_{c}C_{G}}{k_{B}T}}\exp {\left[(2+\lambda )\alpha _{ T}T_{g}\left(1-{\frac {T}{T_{g}}}\right)\right]}\right\}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d7c6670713177337446c22a7976e9664d2008526)








