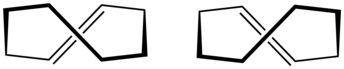
trans -cykloocten - trans-Cyclooctene
|
|
| Namn | |
|---|---|
|
Föredraget IUPAC -namn
( E ) -cykloocten |
|
| Andra namn
trans -cykloocten
|
|
| Identifierare | |
|
3D -modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| EG -nummer | |
|
PubChem CID
|
|
|
|
|
|
| Egenskaper | |
| C 8 H 14 | |
| Molmassa | 110.200 g · mol −1 |
| Utseende | färglös vätska |
| Densitet | 0,848 g/ml |
| Smältpunkt | −59 ° C (−74 ° F; 214 K) |
| Kokpunkt | 143 ° C (1 atm); 68-72 ° C (100 torr) |
| Faror | |
| GHS -piktogram |
 
|
| GHS Signalord | Fara |
|
Om inte annat anges, ges data för material i deras standardtillstånd (vid 25 ° C [77 ° F], 100 kPa). |
|
| Infobox -referenser | |
trans -Cyclooctene är en cyklisk kolväte med formeln [- (CH 2 ) 6 = CH-], där de två C-C-enkelbindningar angränsande till dubbelbindningen befinner sig på motsatta sidor av den senares plan. Det är en färglös vätska med en obehaglig lukt.
Cyklookten är noterbar som den minsta cykloalken som lätt isoleras som dess trans - isomeren . De cis -isomeren är mycket mer stabil; varvid ringspänningsenergierna är 16,7 respektive 7,4 kcal/mol.
 |
|
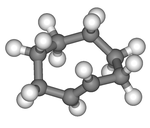
| cis -cykloocten | trans -cykloocten |
Ett plant arrangemang av ringkolarna skulle vara för ansträngt, och därför har transformens stabila konformationer en böjd (icke-plan) ring. Beräkningar indikerar att den mest stabila "krona" -konformationen har kolatomerna växelvis över och under ringens plan. En "halvstol" -konformation, med cirka 6 kcal/mol högre energi, har kol 2,3,5,6 och 8 på samma sida av planet 1,4 och 7.
Alla konformationer av trans -cyclooctene är kirala (specifikt, vad vissa kallar plant-kiral ) och enantiomerer kan separeras. I teorin kan omvandlingen mellan enantiomererna göras, utan att bryta några bindningar, genom att vrida hela –CH = CH– gruppen, styvt, med 180 grader. Det innebär emellertid att en av dess väten passerar genom den trånga ringen.
Förberedelse
trans -cykloocten syntetiserades först i en förberedande skala av Arthur C. Cope med en Hofmann -elimineringsreaktion av N, N, N -trimetylcyklooktylammoniumjodid. Reaktionen ger en blandning av cis- och trans -isomerer, och trans -isomeren fångas selektivt som ett komplex med silvernitrat .
Andra metoder finns där trans -isomeren syntetiseras från cis -isomeren i flera syntetiska steg. Det kan till exempel framställas i nästan 100% utbyte genom att omvandla cis- isomeren till 1,2-epoxicyklooktan ("cyklooctenoxid") följt av reaktioner med litiumdifenylfosfid ( LiPPh
2) och med metyljodid CH
3I . (Liknande procedurer kan ge cis , transisomerer av 1,4-cyklooktadien och 1,5-cyklooktadien ).
Dessutom finns en fotokemisk metod för direkt cis - trans -isomerisering. Även om denna jämvikt starkt gynnar den mer stabila cis -formen, kan reaktionen drivas mot transformen genom att fånga med silverjoner.
Reaktioner
På grund av den högre inre belastningen på dubbelbindningen är trans -isomeren mer reaktiv än cis -isomeren och typiska omättade kolväten. Till exempel kommer dess dubbelbindning snabbt att lägga till tetrazin och dess derivat. Föreningen polymeriserar också lätt med en ruteniumbaserad initiator.
