Nickeloxidhydroxid - Nickel oxide hydroxide
|
|
|
|
| Namn | |
|---|---|
| Andra namn
Nickeloxihydroxid
|
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
|
PubChem CID
|
|
|
|
|
|
| Egenskaper | |
| Ni (O) (OH) | |
| Molmassa | 91,699 g / mol |
| Utseende | svart fast |
| Smältpunkt | 230 ° C (446 ° F, 503 K) |
|
Om inte annat anges anges data för material i standardtillstånd (vid 25 ° C [77 ° F], 100 kPa). |
|
| Infoboxreferenser | |
Nickeloxidhydroxid är den oorganiska föreningen med den kemiska formeln NiO (OH). Det är ett svart fast ämne som är olösligt i alla lösningsmedel men attackeras av bas och syra. Det är en komponent i nickel-metallhydridbatteriet och i nickel-järnbatteriet .
Relaterade material
Nickel (III) -oxider karakteriseras ofta dåligt och antas vara icke-støkiometriska föreningar . Nickel (III) oxid (Ni 2 O 3 ) inte har verifierats kristallografiskt. För applikationer inom organisk kemi genereras nickeloxider eller peroxider in situ och saknar kristallografisk karakterisering. Exempelvis är "nickelperoxid" ( CAS # 12035-36-8) också nära besläktad med eller till och med identisk med NiO (OH).
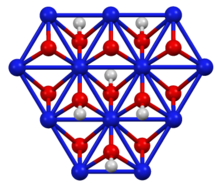
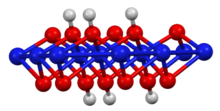
Syntes och struktur
Dess skiktade struktur liknar den hos brucitpolymorfen av nickel (II) hydroxid , men med hälften så många väten. Oxidationstillståndet för nickel är 3+. Det kan framställas genom reaktion av nickel (II) hydroxid med vattenhaltigt kaliumhydroxid och brom som oxidationsmedel:
- 2 Ni (OH) 2 + 2 KOH + Br 2 → 2 KBr + 2 H 2 O + 2 NiOOH
Använd inom organisk kemi
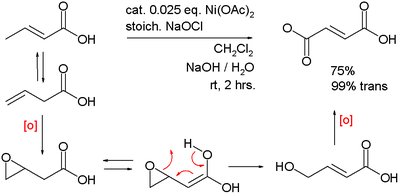
Nickel (III) oxider katalyserar oxidationen av bensylalkohol till bensoesyra med blekmedel:
På liknande sätt katalyserar den dubbeloxidationen av 3-butensyra till fumarsyra :
Referenser
- ^ Gary W. Morrow "Nickel (II) Peroxide" Encyclopedia of Reagents for Organic Synthesis, 2001 John Wiley & Sons. doi : 10.1002 / 047084289X.rn017
- ^ Casas-Cabanas, M .; Canales-Vazquez, J .; Rodriguez Carvajal, J .; Palacin, MR "Characterizing nickel battery materials: crystal structure of beta- (NiOOH)" Materials Research Society Symposia Proceedings (2009) 1126, p131-p136.
- ^ O. Glemser "β-Nickel (III) Hydroxide" i Handbook of Preparative Inorganic Chemistry, 2nd Ed. Redigerad av G. Brauer, Academic Press, 1963, NY. Vol. 1. s. 1549.
- ^ Ett effektivt och praktiskt system för katalytisk oxidation av alkoholer, aldehyder och omättade karboxylsyror Joseph M. Grill, James W. Ogle och Stephen A. Miller J. Org. Chem. ; 2006 ; 71 (25) sid 9291 - 9296; (Artikel) doi : 10.1021 / jo0612574