Gaskromatografi - Gas chromatography
 En gaskromatograf med en provtagare på huvudutrymme
| |
| Akronym | GC |
|---|---|
| Klassificering | Kromatografi |
| Analytiker |
Organiskt oorganiskt Måste vara flyktigt |
| Andra tekniker | |
| Relaterad |
Tunnskiktskromatografi Högpresterande vätskekromatografi |
| Bindestreck | Gaskromatografi-masspektrometri |
Gaskromatografi ( GC ) är en vanlig typ av kromatografi som används i analytisk kemi för att separera och analysera föreningar som kan förångas utan sönderdelning . Typiska användningar av GC inkluderar att testa renheten hos ett visst ämne eller separera de olika komponenterna i en blandning. Vid preparativ kromatografi kan GC användas för att framställa rena föreningar från en blandning.
Gaskromatografi är också ibland känd som ångfaskromatografi (VPC) eller gas-vätskefördelningskromatografi (GLPC). Dessa alternativa namn, liksom deras respektive förkortningar, används ofta i vetenskaplig litteratur.
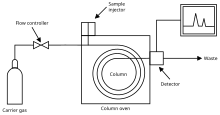
Gaskromatografi är processen att separera föreningar i en blandning genom att injicera ett gasformigt eller flytande prov i en mobil fas, vanligtvis kallad bärgasen, och passera gasen genom en stationär fas. Den mobila fasen är vanligtvis en inert gas eller en oreaktiv gas såsom helium , argon , kväve eller väte . Den stationära fasen är ett mikroskopiskt lager av viskös vätska på en yta av fasta partiklar på ett inert fast underlag inuti ett glas- eller metallrör som kallas en kolonn. De fasta partiklarnas yta kan också fungera som den stationära fasen i vissa kolumner. Glas- eller metallkolonnen genom vilken gasfasen passerar är placerad i en ugn där temperaturen på gasen kan kontrolleras och elueringsmedlet som kommer från kolonnen övervakas av en datoriserad detektor.
Historia
Kromatografi dateras till 1903 i arbetet med den ryska forskaren, Mikhail Semenovich Tswett , som separerade växtpigment via vätskekolonnkromatografi. Den tyska fysikaliska kemisten Erika Cremer 1947 tillsammans med den österrikiska doktoranden Fritz Prior utvecklade de teoretiska grunderna för GC och byggde den första vätskekromatografen, men hennes arbete ansågs irrelevant och ignorerades länge. Engelska kemister Archer Martin och Richard Synge fick ett Nobelpris 1952 för uppfinningen av partitionskromatografi på 1940 -talet och lade grunden för gaskromatografi. Gaskromatografins popularitet ökade snabbt efter utvecklingen av flamjoniseringsdetektorn.
GC -analys
En gaskromatograf är ett kemiskt analysinstrument för att separera kemikalier i ett komplext prov. En gaskromatograf består av ett smalt genomströmningsrör, kallat kolonnen, genom vilket provet passerar i en gasström (bärgasen) med olika hastigheter beroende på deras olika kemiska och fysikaliska egenskaper och deras interaktion med en specifik kolumnfoder eller fyllning, kallad 'stationär fas' . När kemikalierna lämnar änden av kolonnen detekteras och identifieras de elektroniskt. Funktionen för den stationära fasen i kolumnen är att separera olika komponenter, vilket får var och en att lämna kolonnen vid en annan tidpunkt. Andra parametrar som kan användas för att ändra ordning eller lagringstid är bärargasflödeshastighet, kolonnlängd och temperatur.
I en GC -analys injiceras en känd volym gasformig eller flytande analyt genom en gummiskiva och in i en varm, temperaturkontrollerad port ansluten till kolonnen. Som bärargas transporterar analytmolekylerna genom kolonnen finns det adsorption av analytmolekylerna antingen på kolonnen väggar eller på förpackningsmaterial (stationär fas) i kolonnen för att ge separation. Eftersom varje typ av molekyl har en annan progressionshastighet separeras de olika komponenterna i analytblandningen när de går längs kolonnen och når kolumnens ände vid olika tidpunkter (retentionstid). En detektor används för att övervaka tiden vid vilken varje komponent når utloppet och slutligen kan mängden av den komponenten bestämmas. I allmänhet identifieras ämnen (kvalitativt) av den ordning i vilken de eluerar från kolonnen och av retenttiden för analyten i kolonnen.
Fysiska komponenter
Autosamplers
Autosamplern tillhandahåller medel för att automatiskt införa ett prov i inloppen. Manuell insättning av provet är möjlig men är inte längre vanlig. Automatisk insättning ger bättre reproducerbarhet och tidsoptimering.
Olika typer av autosamplers finns. Autosamplers kan klassificeras i förhållande till provkapacitet (autoinjektorer vs. autosamplers, där autoinjektorer kan arbeta ett litet antal prover), till robotteknik (XYZ-robot vs. roterande robot-den vanligaste) eller till analys:
- Flytande
- Statiskt huvudutrymme med sprutteknik
- Dynamiskt huvudutrymme med överföringslinjeteknik
- Fast fas mikroextraktion (SPME)
Inlopp
Kolonninloppet (eller injektorn) tillhandahåller medel för att införa ett prov i ett kontinuerligt flöde av bärargas. Inloppet är en hårdvara fäst vid kolumnhuvudet.
Vanliga inloppstyper är:
- S/SL (split/splitless) injektor; ett prov införs i en uppvärmd liten kammare via en spruta genom en septum - värmen underlättar förångning av provet och provmatrisen. Bärgasen sveper sedan antingen hela (splitless mode) eller en del (split mode) av provet in i kolonnen. I delat läge töms en del av prov/bärargasblandningen i injektionskammaren ut genom den delade ventilen. Delad injektion är att föredra när man arbetar med prover med höga analytkoncentrationer (> 0,1%) medan splitless injektion är bäst lämpad för spåranalys med låga mängder analytter (<0,01%). I splitless-läge öppnas splitventilen efter en förinställd tid för att rensa tyngre element som annars skulle förorena systemet. Denna förinställda (splitless) tid bör optimeras, ju kortare tid (t.ex. 0,2 min) säkerställer mindre svansning men förlust i svar, desto längre tid (2 min) ökar avlägsnande men också signal.
- Inlopp på kolumnen; provet införs här direkt i kolonnen i sin helhet utan värme eller vid en temperatur under lösningsmedlets kokpunkt. Den låga temperaturen kondenserar provet till en smal zon. Kolonnen och inloppet kan sedan värmas upp och provet släpps ut i gasfasen. Detta säkerställer lägsta möjliga temperatur för kromatografi och hindrar prover från att brytas ned över kokpunkten.
- PTV -injektor; Temperaturprogrammerad provintroduktion beskrevs först av Vogt 1979. Ursprungligen utvecklade Vogt tekniken som en metod för införande av stora provvolymer (upp till 250 µL) i kapillär GC. Vogt införde provet i fodret med en kontrollerad injektionshastighet. Fodertemperaturen valdes något under lösningsmedlets kokpunkt. Det lågkokande lösningsmedlet avdunstades kontinuerligt och ventilerades genom den delade linjen. Baserat på denna teknik utvecklade Poy den programmerade förångningsinjektorn för temperatur; PTV. Genom att införa provet vid en låg initial fodertemperatur skulle många av nackdelarna med de klassiska heta injektionsteknikerna kunna kringgås.
- Gaskällans inlopp eller gasomkopplingsventil; gasprover i uppsamlingsflaskor är anslutna till det som oftast är en sexports omkopplingsventil. Bärgasflödet avbryts inte medan ett prov kan expanderas till en tidigare evakuerad provslinga. Vid omkoppling införs innehållet i provslingan i bärgasströmmen.
- P/T (Purge-and-Trap) -system; En inert gas bubblas genom ett vattenhaltigt prov vilket gör att olösliga flyktiga kemikalier rensas ut från matrisen. De flyktiga ämnena "fångas" på en absorberande kolonn (känd som en fälla eller koncentrat) vid omgivningstemperatur. Fällan värms sedan upp och flyktiga ämnen riktas in i bärgasströmmen. Prover som kräver förkoncentration eller rening kan införas via ett sådant system, vanligtvis anslutna till S/SL -porten.
Valet av bärargas (mobil fas) är viktigt. Väte har en rad flödeshastigheter som är jämförbara med helium i effektivitet. Helium kan dock vara mer effektivt och ge den bästa separationen om flödeshastigheterna är optimerade. Helium är icke brandfarligt och fungerar med ett större antal detektorer och äldre instrument. Därför är helium den vanligaste bärgasen som används. Priset på helium har dock stigit avsevärt under de senaste åren, vilket fått ett ökande antal kromatografer att byta till vätgas. Historisk användning, snarare än rationell hänsyn, kan bidra till fortsatt förmånlig användning av helium.
Detektorer
Vanliga detektorer är flamjoniseringsdetektorn (FID) och värmeledningsförmågningsdetektorn (TCD). Även om TCD är fördelaktiga i och med att de är icke-destruktiva, hämmar dess låga detektionsgräns för de flesta analyser utbredd användning. FID är främst känsliga för kolväten och är mer känsliga för dem än TCD. FID kan inte detektera vatten eller koldioxid som gör dem idealiska för miljöanalys av organiska analyser. FID är två till tre gånger mer känslig för analytdetektering än TCD.
TCD förlitar sig på värmeledningsförmågan hos materia som passerar runt en tunn tråd av volfram-rhenium med en ström som passerar genom den. I denna uppsättning fungerar helium eller kväve som bärargas på grund av deras relativt höga värmeledningsförmåga som håller filamentet svalt och upprätthåller enhetlig resistivitet och elektrisk effektivitet hos filamentet. När analytmolekyler eluerar från kolonnen, blandat med bärargas, minskar värmeledningsförmågan medan det finns en ökning av glödtrådstemperatur och resistivitet, vilket resulterar i fluktuationer i spänningen som i slutändan orsakar ett detektorsvar. Detektorkänslighet är proportionell mot filamentström medan den är omvänt proportionell mot den omedelbara omgivningstemperaturen för den detektorn samt flödeshastigheten för bärargasen.
I en flamjoniseringsdetektor (FID) placeras elektroder intill en låga som drivs av väte / luft nära kolonnens utlopp, och när kolhaltiga föreningar lämnar kolonnen pyrolyseras de av lågan. Denna detektor fungerar endast för organiska / kolväteinnehållande föreningar på grund av kolens förmåga att bilda katjoner och elektroner vid pyrolys som genererar en ström mellan elektroderna. Ökningen av strömmen översätts och visas som en topp i ett kromatogram. FID har låga detektionsgränser (några pikogram per sekund) men de kan inte generera joner från karbonylhaltiga kol. FID -kompatibla bärargaser inkluderar helium, väte, kväve och argon.
Alkali flamdetektor (AFD) eller alkali flamjoniseringsdetektor (AFID) har hög känslighet för kväve och fosfor, liknande NPD. De alkaliska metalljonerna tillförs emellertid vätgasen, snarare än en pärla ovanför lågan. Av denna anledning lider AFD inte av "trötthet" hos NPD, utan ger en konstant känslighet under lång tid. Dessutom, när alkalijoner inte tillsätts till lågan, fungerar AFD som en standard FID. En katalytisk förbränningsdetektor (CCD) mäter brännbara kolväten och väte. Urladdningsjoniseringsdetektor (DID) använder en högspännings elektrisk urladdning för att producera joner.
Den polyarc reaktorn är en add-on till nya eller befintliga GC-FID instrument som konverterar alla organiska föreningar till metan molekyler före deras detektering av FID. Denna teknik kan användas för att förbättra responsen hos FID och möjliggöra upptäckt av många fler kolhaltiga föreningar. Den fullständiga omvandlingen av föreningar till metan och det nu ekvivalenta svaret i detektorn eliminerar också behovet av kalibreringar och standarder eftersom svarsfaktorer alla är ekvivalenta med metan. Detta möjliggör snabb analys av komplexa blandningar som innehåller molekyler där standarder inte är tillgängliga.
Flamfotometrisk detektor (FPD) använder ett fotomultiplikatorrör för att detektera spektrallinjer av föreningarna när de bränns i en låga. Föreningar som eluerar från kolonnen förs in i en vätedriven låga som exciterar specifika element i molekylerna, och de exciterade elementen (P, S, halogener, vissa metaller) avger ljus av specifika karakteristiska våglängder. Det utsända ljuset filtreras och detekteras av ett fotomultiplikatorrör. Speciellt är fosforutsläppet cirka 510–536 nm och svavelutsläppet är 394 nm. Med en atomemissionsdetektor (AED) kommer ett prov som eluerar från en kolonn in i en kammare som drivs av mikrovågor som inducerar en plasma. Plasman får analytprovet att sönderdelas och vissa element genererar ett atomspektrum. Atomemissionsspektra diffrakteras av ett diffraktionsgaller och detekteras av en serie fotomultiplikatorrör eller fotodioder.
Elektronfångningsdetektor (ECD) använder en radioaktiv betapartikelkälla (elektron) för att mäta graden av elektronfångst. ECD används för detektering av molekyler som innehåller elektronegativa / uttagande element och funktionella grupper som halogener, karbonyl, nitriler, nitrogrupper och organometal. I denna typ av detektor används antingen kväve eller 5% metan i argon som bärarfas för mobil fas. Bärgasen passerar mellan två elektroder placerade vid änden av kolonnen, och intill katoden (negativ elektrod) ligger en radioaktiv folie såsom 63Ni. Den radioaktiva folien avger en betapartikel (elektron) som kolliderar med och joniserar bärgasen för att generera fler joner vilket resulterar i en ström. När analytmolekyler med elektronegativa / uttagande element eller funktionella grupper fångas elektroner vilket resulterar i en minskning av strömmen som genererar ett detektorsvar.
Kväve -fosfor -detektor (NPD), en form av termionisk detektor där kväve och fosfor förändrar arbetsfunktionen på en specialbelagd pärla och en resulterande ström mäts.
Torr elektrolytisk konduktivitetsdetektor (DELCD) använder en luftfas och hög temperatur (v. Coulsen) för att mäta klorerade föreningar.
Masspektrometer (MS), även kallad GC-MS ; mycket effektiv och känslig, även i en liten mängd prov. Denna detektor kan användas för att identifiera analyterna i kromatogram med deras masspektrum. Vissa GC-MS är anslutna till en NMR-spektrometer som fungerar som en reservdetektor. Denna kombination är känd som GC-MS-NMR . Vissa GC-MS-NMR är anslutna till en infraröd spektrofotometer som fungerar som en reservdetektor. Denna kombination är känd som GC-MS-NMR-IR. Det måste dock betonas att detta är mycket sällsynt eftersom de flesta analyser som behövs kan avslutas via rent GC-MS.
Vakuum ultraviolett (VUV) representerar den senaste utvecklingen inom gaskromatografedetektorer. De flesta kemiska arter absorberar och har unika gasfasabsorptionstvärsnitt i det övervakade våglängdsintervallet på cirka 120–240 nm. Där absorptionstvärsnitt är kända för analytter, kan VUV -detektorn absolut bestämma (utan kalibrering) av antalet molekyler som finns i flödescellen i frånvaro av kemiska störningar.
Olfaktometrisk detektor , även kallad GC-O, använder en mänsklig bedömare för att analysera luktaktiviteten hos föreningar. Med en luktport eller en sniffande port kan kvaliteten på lukten, luktens intensitet och varaktigheten av luktaktiviteten hos en förening bedömas.
Andra detektorer inkluderar Hall elektrolytisk konduktivitetsdetektor (ElCD), heliumjoniseringsdetektor (HID), infraröd detektor (IRD), fotojoniseringsdetektor (PID), pulserad urladdningsjoniseringsdetektor (PDD) och termjonisk joniseringsdetektor (TID).
Metoder

Metoden är insamling av villkor under vilka GC fungerar för en given analys. Metodutveckling är processen för att bestämma vilka förutsättningar som är lämpliga och/eller idealiska för den analys som krävs.
Förhållanden som kan varieras för att tillgodose en erforderlig analys inkluderar inloppstemperatur, detektortemperatur, kolonntemperatur och temperaturprogram, bärargas och bärargasflödeshastigheter, kolonnens stationära fas, diameter och längd, inloppstyp och flödeshastigheter, provstorlek och injektion Metod. Beroende på detektor (er) (se nedan) som är installerade på GC kan det finnas ett antal detektorförhållanden som också kan varieras. Vissa GC innehåller också ventiler som kan ändra provvägen och bärarflödet. Tidpunkten för öppning och stängning av dessa ventiler kan vara viktig för metodutveckling.
Bärgasval och flödeshastigheter
Typiska bärargaser inkluderar helium , kväve , argon och väte . Vilken gas som ska användas bestäms vanligtvis av detektorn som används, till exempel kräver en DID helium som bärargas. När man analyserar gasprover väljs bäraren också baserat på provets matris, till exempel, när man analyserar en blandning i argon, föredras en argonbärare eftersom argon i provet inte dyker upp på kromatogrammet. Säkerhet och tillgänglighet kan också påverka transportörens val.
Bärgasens renhet bestäms också ofta av detektorn, även om känslighetsnivån som behövs kan också spela en betydande roll. Vanligtvis används renheter på 99,995% eller högre. De vanligaste renhetsgraderna som krävs av moderna instrument för majoriteten av känsligheterna är 5,0 grader, eller 99,999% rena, vilket betyder att det finns totalt 10 ppm föroreningar i bärgasen som kan påverka resultaten. De högsta renhetsgraderna i vanligt bruk är 6,0 -kvaliteter, men behovet av detektion vid mycket låga nivåer i vissa rättsmedicinska och miljömässiga tillämpningar har drivit behovet av bärargaser till 7,0 -renhet och dessa är nu kommersiellt tillgängliga. Handelsnamn för typiska renheter inkluderar "Zero Grade", "Ultra-High Purity (UHP) Grade", "4.5 Grade" och "5.0 Grade".
Bärgasens linjära hastighet påverkar analysen på samma sätt som temperaturen gör (se ovan). Ju högre linjär hastighet desto snabbare analys, men desto lägre är skillnaden mellan analytter. Att välja den linjära hastigheten är därför samma kompromiss mellan separationsnivån och analyslängden som att välja kolumnens temperatur. Den linjära hastigheten kommer att implementeras med hjälp av bärgasflödeshastigheten med avseende på kolonnens innerdiameter.
Med GC gjorda före 1990 -talet kontrollerades bärarflödeshastigheten indirekt genom att kontrollera bärarens inloppstryck, eller "kolumnhuvudstryck". Den faktiska flödeshastigheten mättes vid kolonnens eller detektorns utlopp med en elektronisk flödesmätare eller en bubbelflödesmätare och kan vara en involverad, tidskrävande och frustrerande process. Det var inte möjligt att variera tryckinställningen under körningen, och därför var flödet väsentligen konstant under analysen. Förhållandet mellan flödeshastighet och inloppstryck beräknas med Poiseuilles ekvation för komprimerbara vätskor .
Många moderna GC mäter emellertid elektroniskt flödeshastigheten och styr elektroniskt bärargastrycket för att ställa in flödeshastigheten. Följaktligen kan bärartryck och flödeshastigheter justeras under körningen, vilket skapar tryck/flödesprogram som liknar temperaturprogram.
Stationärt sammansatt urval
Den polariteten av det lösta ämnet är avgörande för valet av stationära förening, som på ett optimalt fall skulle ha en liknande polaritet som det lösta ämnet. Vanliga stationära faser i öppna rörformiga kolonner är cyanopropylfenyldimetylpolysiloxan, karbowaxpolyetylenglykol, biscyanopropylcyanopropylfenylpolysiloxan och difenyldimetylpolysiloxan. För packade kolumner finns fler alternativ.
Inloppstyper och flödeshastigheter
Valet av inloppstyp och injektionsteknik beror på om provet är i vätska, gas, adsorberad eller fast form och om det finns en lösningsmedelsmatris som måste förångas. Upplösta prover kan införas direkt på kolonnen via en COC -injektor, om förhållandena är välkända; om en lösningsmedelsmatris måste förångas och delvis avlägsnas, används en S/SL -injektor (vanligaste injektionsteknik); gasprover (t.ex. luftcylindrar) injiceras vanligtvis med användning av ett gasomkopplingsventilsystem; adsorberade prover (t.ex. på adsorberande rör) införs med antingen en extern (on-line eller off-line) desorptionsapparat, såsom ett rensnings-och-fällsystem, eller desorberas i injektorn (SPME-applikationer).
Provstorlek och injektionsteknik
Provinjektion
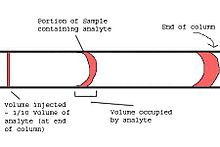
Den verkliga kromatografiska analysen börjar med införandet av provet på kolonnen. Utvecklingen av kapillärgaskromatografi resulterade i många praktiska problem med injektionstekniken. Tekniken med injektion på kolonnen, som ofta används med packade kolonner, är vanligtvis inte möjlig med kapillarkolonner. I injektionssystemet i kapillärgaskromatografen ska den injicerade mängden inte överbelasta kolonnen och bredden på den injicerade pluggen bör vara liten jämfört med spridningen på grund av den kromatografiska processen. Underlåtenhet att följa detta senare krav kommer att minska kolonnens separationsförmåga. Som en allmän regel bör den injicerade volymen, V inj och volymen av detektorcellen, V det , vara cirka 1/10 av volymen som upptas av den del av provet som innehåller molekylerna av intresse (analyter) när de lämnar kolumn.
Några allmänna krav som en bra injektionsteknik bör uppfylla är att det ska vara möjligt att uppnå kolonnens optimala separeringseffektivitet, den ska möjliggöra noggranna och reproducerbara injektioner av små mängder representativa prover, det ska inte orsaka någon förändring i provkompositionen, det bör inte uppvisar diskriminering på grund av skillnader i kokpunkt, polaritet, koncentration eller termisk/katalytisk stabilitet, och det bör vara tillämpligt för spåranalys såväl som för outspädda prover.
Det finns emellertid ett antal problem med användningen av sprutor för injektion. Även de bästa sprutorna hävdar en noggrannhet på endast 3%, och i okvalificerade händer är felen mycket större. Nålen kan skära små bitar av gummi från septum när den injicerar prov genom den. Dessa kan blockera nålen och förhindra att sprutan fylls nästa gång den används. Det är kanske inte uppenbart att detta har hänt. En bråkdel av provet kan fastna i gummit för att frigöras under efterföljande injektioner. Detta kan ge upphov till spökstoppar i kromatogrammet. Det kan ske en selektiv förlust av de mer flyktiga komponenterna i provet genom avdunstning från nålspetsen.
Kolumnval
Valet av kolumn beror på provet och den uppmätta aktiva. Det huvudsakliga kemiska attributet som betraktas när man väljer en kolumn är blandningen polaritet , men funktionella grupper kan spela en stor roll vid val av kolonn. Polens polaritet måste stämma överens med polariteten hos den stationära fasen i kolonnen för att öka upplösningen och separationen samtidigt som körtiden reduceras. Separationen och drifttiden beror också på filmtjockleken (i den stationära fasen), kolonnens diameter och kolonnlängden.
Kolumnstemperatur och temperaturprogram
Kolonn (erna) i en GC finns i en ugn, vars temperatur exakt styrs elektroniskt. (När man diskuterar "kolumnens temperatur" hänvisar en analytiker tekniskt till kolumnugnens temperatur. Skillnaden är dock inte viktig och kommer inte att göras senare i denna artikel.)
Den hastighet med vilken ett prov passerar genom kolonnen är direkt proportionell mot kolonnens temperatur. Ju högre kolonnens temperatur desto snabbare rör sig provet genom kolonnen. Men ju snabbare ett prov rör sig genom kolumnen, desto mindre interagerar det med den stationära fasen och desto mindre separeras analyterna.
I allmänhet väljs kolonnens temperatur för att kompromissa mellan analysens längd och separationsnivån.
En metod som håller kolonnen vid samma temperatur för hela analysen kallas "isotermisk". De flesta metoder ökar dock kolonnens temperatur under analysen, den initiala temperaturen, temperaturhöjningshastigheten (temperatur "rampen") och den slutliga temperaturen kallas temperaturprogrammet.
Ett temperaturprogram tillåter att analytter som eluerar tidigt i analysen separeras på ett adekvat sätt, samtidigt som den förkortar den tid det tar för sent eluerande analytter att passera genom kolonnen.
Datareduktion och analys
Kvalitativ analys
I allmänhet presenteras kromatografiska data som ett diagram över detektorsvar (y-axel) mot retentionstid (x-axel), vilket kallas ett kromatogram. Detta ger ett spektrum av toppar för ett prov som representerar analyterna närvarande i ett prov som eluerar från kolonnen vid olika tidpunkter. Retentionstid kan användas för att identifiera analytter om metodförhållandena är konstanta. Mönstret för toppar kommer också att vara konstant för ett prov under konstanta förhållanden och kan identifiera komplexa blandningar av analytter. I de flesta moderna applikationer är GC dock ansluten till en masspektrometer eller liknande detektor som kan identifiera de analytter som representeras av topparna.
Kvantitativ analys
Ytan under en topp är proportionell mot mängden analyt som finns i kromatogrammet. Genom att beräkna toppen av toppen med hjälp av den matematiska integrationsfunktionen kan koncentrationen av en analyt i det ursprungliga provet bestämmas. Koncentrationen kan beräknas med hjälp av en kalibreringskurva som skapas genom att hitta svaret för en serie koncentrationer av analyt eller genom att bestämma den relativa responsfaktorn för en analyt. Den relativa svarsfaktorn är det förväntade förhållandet mellan en analyt och en intern standard (eller extern standard ) och beräknas genom att hitta svaret för en känd mängd analyt och en konstant mängd intern standard (en kemikalie tillsatt provet vid en konstant koncentration, med en distinkt retentionstid till analyten).
I de flesta moderna GC-MS -system, dator programvara används för att rita och integrera toppar, och matcha MS spektra till biblioteket spektra.
Ansökningar
I allmänhet kan ämnen som förångas under 300 ° C (och därför är stabila upp till den temperaturen) mätas kvantitativt. Proverna måste också vara salt -fri; de ska inte innehålla joner . Mycket små mängder av ett ämne kan mätas, men det krävs ofta att provet måste mätas i jämförelse med ett prov som innehåller det rena, misstänkta ämnet som kallas en referensstandard .
Olika temperaturprogram kan användas för att göra avläsningarna mer meningsfulla; till exempel för att skilja mellan ämnen som beter sig på samma sätt under GC -processen.
Professionella som arbetar med GC analyserar innehållet i en kemisk produkt, till exempel för att säkerställa kvaliteten på produkterna i den kemiska industrin; eller mäta kemikalier i jord, luft eller vatten, till exempel jordgaser . GC är mycket exakt om det används på rätt sätt och kan mäta picomol av ett ämne i ett 1 ml flytande prov eller delar per miljard koncentrationer i gasprover.
I praktiska kurser på högskolor får eleverna ibland bekanta sig med GC genom att studera innehållet i lavendelolja eller mäta den eten som utsöndras av Nicotiana benthamiana -växter efter att ha artificiellt skadat sina löv. Dessa GC analyserar kolväten (C2-C40+). I ett typiskt experiment används en packad kolonn för att separera de lätta gaserna, som sedan detekteras med en TCD . De kolvätena separeras med användning av en kapillärkolonn och detekterades med en FID . En komplikation med lätta gasanalyser som inkluderar H 2 är att Han, som är den vanligaste och mest känsliga inert bärare (känslighet är proportionell mot molekylmassa) har en nästan identisk värmeledningsförmåga till väte (det är skillnaden i värmeledningsförmågan mellan två separata trådar i ett Wheatstone Bridge -typarrangemang som visar när en komponent har eluerats). Av denna anledning är dubbla TCD -instrument som används med en separat kanal för väte som använder kväve som bärare vanliga. Argon används ofta vid analys av gasfaskemiska reaktioner såsom FT -syntes så att en enda bärargas kan användas snarare än två separata. Känsligheten minskas, men detta är en avvägning för enkelhet i gastillförseln.
Gaskromatografi används flitigt inom rättsmedicinsk vetenskap . Lika olika discipliner som fast läkemedelsdos (förkonsumtionsform) identifiering och kvantifiering, mordbrandutredning, färgflisanalys och toxikologiska fall använder GC för att identifiera och kvantifiera olika biologiska prover och bevis från brottsplatsen.
Se även
- Analytisk kemi
- Kromatografi
- Gaskromatografi - masspektrometri
- Gaskromatografi-olfaktometri
- Högpresterande vätskekromatografi
- Invers gaskromatografi
- Protonöverföringsreaktionsmasspektrometri
- Sekundär elektrosprayjonisering
- Vald jonflödesrör masspektrometri
- Standardtillägg
- Tunnskiktskromatografi
- Oupplöst komplex blandning
Referenser
externa länkar
![]() Media relaterat till gaskromatografi på Wikimedia Commons
Media relaterat till gaskromatografi på Wikimedia Commons
- Kromatografiska kolumner i Chemistry LibreTexts -biblioteket
- Gaskromatografi på Curlie