Alfred Werner - Alfred Werner
Alfred Werner | |
|---|---|
 | |
| Född | 12 december 1866 |
| Död | 15 november 1919 (52 år) |
| Nationalitet | Schweiziska |
| Alma mater |
Zürichs universitet ETH Zürich |
| Känd för | konfiguration av övergångsmetallkomplex |
| Utmärkelser | Nobelpriset för kemi (1913) |
| Vetenskaplig karriär | |
| Fält | Oorganisk kemi |
| Institutioner | Zürichs universitet |
| Doktorandrådgivare | Arthur Rudolf Hantzsch , Marcellin Berthelot |
Alfred Werner (12 december 1866 - 15 november 1919) var en schweizisk kemist som var student vid ETH Zürich och professor vid universitetet i Zürich . Han vann Nobelpriset i kemi 1913 för att ha föreslagit den oktaedriska konfigurationen av övergångsmetallkomplex . Werner utvecklade grunden för modern samordningskemi . Han var den första oorganiska kemisten som vann Nobelpriset, och den enda före 1973.
Biografi
Werner föddes 1866 i Mulhouse , Alsace (som då var en del av Frankrike , men som annekterades av Tyskland 1871). Han växte upp som romersk katolik . Han var det fjärde och sista barnet till Jean-Adam Werner, en gjuteriarbetare, och hans andra fru, Salomé Jeanette Werner, som härstammade från en välbärgad familj. Han reste till Schweiz för att studera kemi vid Swiss Federal Institute (Polytechnikum) i Zürich , men eftersom detta institut inte hade behörighet att bevilja doktorsexamen förrän 1909 tog Werner doktorsexamen formellt från universitetet i Zürich 1890. Efter postdoktorala studier i Paris , han återvände till schweiziska federala institutet för att undervisa (1892). 1893 flyttade han till universitetet i Zürich , där han blev professor 1895. 1894 blev han schweizisk medborgare.
Under sitt sista år led han av en allmän, progressiv, degenerativ åderförkalkning , särskilt i hjärnan, förvärrad av år med överdrivet drickande och överansträngning. Han dog på ett psykiatriskt sjukhus i Zürich.
Forskning
Koordineringskemi
År 1893 var Werner den första att föreslå korrekta strukturer för koordinationsföreningar som innehåller komplexa joner , där en central övergångsmetallatom är omgiven av neutrala eller anjoniska ligander .
Till exempel, var det känt att kobolt bildar ett "komplex" hexamminecobalt (III) klorid, med formeln CoCl 3 • 6NH 3 , men naturen av föreningen som anges av pricken var mystisk. Werner föreslagna strukturen [Co (NH 3 ) 6 ] Cl 3 , med Co 3+ jon omgiven av sex NH 3 i hörnen av en oktaeder. De tre Cl - dissocieras som fria joner, vilket Werner bekräftade genom att mäta föreningens konduktivitet i vattenlösning, och även genom kloridanjonanalys med användning av utfällning med silvernitrat . Senare användes också magnetisk känslighetsanalys för att bekräfta Werners förslag om den kemiska beskaffenheten av CoCl 3 • 6NH 3 .
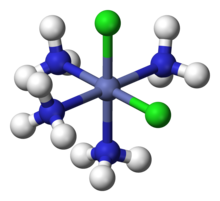
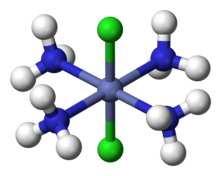
För komplex med mer än en typ av ligand lyckades Werner förklara antalet observerade isomerer . Till exempel förklarade han förekomsten av två tetramminisomerer, "Co (NH 3 ) 4 Cl 3 ", en grön och en lila. Werner föreslog att dessa är två geometriska isomerer med formeln [Co (NH 3 ) 4 Cl 2 ] Cl, med en Cl - jon dissocieras vilket bekräftas av konduktivitetsmätningar. Co-atomen är omgiven av fyra NH 3 och två Cl-ligander i hörnen av en oktaeder. Den gröna isomeren är "trans" med de två Cl -liganderna vid motsatta hörn, och den lila är "cis" med de två Cl vid intilliggande hörn.
Werner ställdes också komplex med optiska isomerer , och i 1914 han rapporterade den första syntetiska kiral förening som saknar kol, känd som hexol med formeln [Co (Co (NH 3 ) 4 (OH) 2 ) 3 ] Br 6 .
Valens natur
Före Werner definierade kemister ett valens valens som antalet bindningar utan att skilja olika typer av bindningar. Emellertid, i komplex, såsom [Co (NH 3 ) 6 ] Cl 3 exempelvis Werner ansåg att Co-Cl-bindningar motsvara en "primär" valens tre på långa avstånd, medan Co-NH 3 bindningar som motsvarar en "sekundär" eller svagare valens av 6 på kortare avstånd. Denna sekundära valens av 6 kallade han koordinationsnumret som han definierade som antalet molekyler (här av NH 3 ) direkt kopplade till den centrala metallatomen. I andra komplex hittade han koordinationsnummer på 4 eller 8.
Om dessa åsikter och andra liknande åsikter formulerade Richard Abegg 1904 det som nu kallas Abeggs regel som säger att skillnaden mellan den maximala positiva och negativa valensen för ett element ofta är åtta. Denna regel användes senare 1916 när Gilbert N. Lewis formulerade " oktettregeln " i sin kubiska atomteori.
I modern terminologi motsvarar Werners primära valens oxidationstillståndet , och hans sekundära valens kallas koordinationsnummer . Co-Cl-bindningar (i exemplet ovan) är nu klassas som jonisk, och varje Co-N-bindningen är en koordinerande kovalent bindning mellan Lewis-syran Co 3+ och Lewis-bas NH 3 .
Arbetar
- Lehrbuch der Stereochemie . Fischer, Jena 1904 Digital upplaga av universitetet och statsbiblioteket Düsseldorf
Referenser
- W. Gregory Jackson; Josephine A. McKeon; Silvia Cortez (2004). "Alfred Werners oorganiska motsvarigheter till racemisk och mesomerisk vinsyra: en milstolpe reviderad". Inorg. Chem. 43 (20): 6249–6254. doi : 10.1021/ic040042e . PMID 15446870 .
- Kristin Bowman-James (2005). "Alfred Werner Revisited: The Coordination Chemistry of Anions". Acc. Chem. Res. 38 (8): 671–678. doi : 10.1021/ar040071t . PMID 16104690 .
externa länkar
-
Alfred Werner på Nobelprize.org
 inklusive Nobelföreläsningen, 11 december 1913 om konstitutionen och konfigurationen av föreningar med högre ordning
inklusive Nobelföreläsningen, 11 december 1913 om konstitutionen och konfigurationen av föreningar med högre ordning
- Nobelpriset i kemi 1913 - en kort artikel om hans arbete med koppling av atomer i molekyler genom vilka han har kastat nytt ljus på tidigare undersökningar och öppnat nya forskningsområden, särskilt inom oorganisk kemi.