Leigh syndrom - Leigh syndrome
| Leigh syndrom | |
|---|---|
| Andra namn | Juvenil subakut nekrotiserande encefalomyelopati, Leighsjukdom, infantil subakut nekrotiserande encefalomyelopati, subakut nekrotiserande encefalomyelopati (SNEM) |
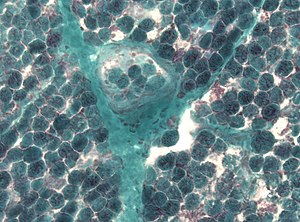 | |
| Detektion av många trasiga röda fibrer i en muskelbiopsi | |
| Specialitet |
Neurologi |
Leigh syndrom (även kallat Leigh sjukdom och subakut nekrotiserande encefalomyelopati ) är en ärftlig neurometabolisk störning som påverkar centrala nervsystemet . Det är uppkallat efter Archibald Denis Leigh, en brittisk neuropsykiater som först beskrev tillståndet 1951. Normala nivåer av tiamin , tiaminmonofosfat och tiamindifosfat finns vanligtvis men det finns en reducerad eller frånvarande nivå av tiamintrifosfat . Detta antas orsakas av en blockering i enzymet tiamindifosfatkinas , och därför skulle behandling hos vissa patienter vara att ta tiamintrifosfat dagligen.
tecken och symtom
Symtomen på Leigh syndrom beskrivs klassiskt som början i spädbarn och leder till döden inom flera år; emellertid, eftersom fler fall känns igen, är det uppenbart att symtom kan uppstå i alla åldrar - inklusive tonåren eller vuxen ålder - och patienter kan överleva i många år efter diagnosen. Symtom ses ofta först efter en utlösande händelse som beskattar kroppens energiproduktion, såsom en infektion eller operation. Den allmänna kursen för Leigh syndrom är en av episodisk utvecklingsregression under tider av metabolisk stress. Vissa patienter har långa perioder utan sjukdomsprogression medan andra utvecklar progressiv nedgång.
Spädbarn med syndromet har symtom som inkluderar diarré , kräkningar och dysfagi (svårigheter att svälja eller suga), vilket leder till ett misslyckande med att trivas . Barn med tidig Leigh-sjukdom kan också verka irriterade och gråta mycket mer än friska barn. Anfall ses ofta. Överskott av laktat kan ses i urinen , cerebrospinalvätskan och blodet hos en person med Leighs syndrom.
När sjukdomen fortskrider är muskelsystemet försvagat i hela kroppen, eftersom hjärnan inte kan kontrollera muskelsammandragningen. Hypotoni (låg muskeltonus och styrka), dystoni (ofrivillig, ihållande muskelsammandragning) och ataxi (brist på kontroll över rörelse) ses ofta hos personer med Leigh-sjukdom. De ögon är särskilt drabbade; musklerna som kontrollerar ögonen blir svaga, förlamade eller okontrollerbara vid tillstånd som kallas oftalmopares (svaghet eller förlamning) och nystagmus (ofrivilliga ögonrörelser). Långsamma sackader ses också ibland. Den hjärta och lungor kan också misslyckas på grund av Leigh sjukdom. Hypertrofisk kardiomyopati (förtjockning av en del av hjärtmuskeln) finns också ibland och kan orsaka död; asymmetrisk septalhypertrofi har också associerats med Leigh syndrom. Hos barn med Leigh-syndrom associerade ventrikelseptumdefekter , orsakade av brist på pyruvatdehydrogenas, syns hög panna och stora öron; ansiktsavvikelser är inte typiska för Leigh syndrom.
Men andningssvikt är den vanligaste dödsorsaken hos personer med Leigh syndrom. Andra neurologiska symtom inkluderar perifer neuropati , förlust av känsla i extremiteter orsakade av skador på det perifera nervsystemet .
Hypertrikos ses i Leigh syndrom orsakad av mutationer i kärngenen SURF1 .
Genomik
Mutationer i mitokondrie-DNA (mtDNA) och över 30 gener i kärn-DNA (gen SURF1 och vissa COX- monteringsfaktorer) har varit inblandade i Leigh-sjukdomen.
Störningar av oxidativ fosforylering , den process genom vilken celler producerar sin huvudsakliga energikälla av adenosintrifosfat (ATP), kan orsakas av mutationer i antingen mtDNA eller i kärnkodade gener. Den senare står för majoriteten av Leigh-sjukdomen, även om det inte alltid är möjligt att identifiera den specifika mutationen som är ansvarig för tillståndet hos en viss individ. Fyra av de fem proteinkomplexen som är involverade i oxidativ fosforylering störs oftast i Leigh-syndromet, antingen på grund av missbildat protein eller på grund av ett fel vid sammansättningen av dessa komplex. Oavsett den genetiska grunden resulterar det i oförmåga hos komplexen som påverkas av mutationen att utföra sin roll i oxidativ fosforylering. I fallet med Leigh sjukdom påverkas viktiga celler i hjärnstammen och basala ganglier. Detta orsakar en kronisk brist på energi i cellerna, vilket leder till celldöd och i sin tur påverkar centrala nervsystemet och hämmar motoriska funktioner. Hjärtat och andra muskler kräver också mycket energi och påverkas av celldöd orsakad av kroniska energibrist i Leigh syndrom.
Mitokondriella DNA-mutationer
Mitokondrier är essentiella organeller i eukaryota celler. Deras funktion är att omvandla den potentiella energin hos glukos , aminosyror och fettsyror till adenosintrifosfat (ATP) i en process som kallas oxidativ fosforylering . Mitokondrier bär sitt eget DNA , kallat mitokondriellt DNA (mtDNA). Informationen lagrad i mtDNA används för att producera flera av de enzymer som är nödvändiga för produktionen av ATP.
Mellan 20 och 25 procent av fallen med Leigh syndrom orsakas av mutationer i mitokondriellt DNA. Den vanligaste av dessa mutationer finns i 10 till 20 procent av Leigh syndrom och förekommer i MT-ATP6 , en gen som kodar för ett protein i det sista komplexet i den oxidativa fosforyleringskedjan, ATP-syntas , ett enzym som direkt genererar ATP. Utan ATP-syntas producerar inte elektrontransportkedjan något ATP. Den vanligaste MT-ATP6-mutationen som finns med Leigh-syndrom är en punktmutation vid nukleotid 8993 som ändrar en tymin till en guanin . Denna och andra punktmutationer associerade med Leigh syndrom destabiliserar eller missbildar proteinkomplexet och håller energiproduktionen nere i drabbade celler. Flera mitokondriella gener som är involverade i att skapa det första komplexet av den oxidativa fosforyleringskedjan kan vara inblandade i ett fall av Leigh syndrom, inklusive gener MT-ND2 , MT-ND3 , MT-ND5 , MT-ND6 och MT-CO1 .
Mitokondriellt DNA överförs matrilinealt i ett mönster som kallas moderns arv - en mamma kan överföra generna för Leigh syndrom till både manliga och kvinnliga barn, men fäder kan inte överföra mitokondriella gener.
Kärn-DNA-mutationer
Kärn-DNA omfattar det mesta av genomet i en organism och i sexuellt reproducerande organismer ärvs det från båda föräldrarna, i motsats till mitokondriellt DNA: s moderns arvsmönster. Leigh-syndrom som orsakas av DNA-kärnmutationer ärvs i ett autosomalt recessivt mönster. Detta innebär att två kopior av den muterade genen krävs för att orsaka sjukdomen, så två opåverkade föräldrar, som var och en bär en mutantallel , kan få ett drabbat barn om det barnet ärver mutantallelen från båda föräldrarna.
75 till 80 procent av Leigh syndrom orsakas av mutationer i kärn-DNA; mutationer som påverkar funktionen eller sammansättningen av det fjärde komplexet som är involverat i oxidativ fosforylering, cytokrom c-oxidas (COX), orsakar de flesta fall av Leigh-sjukdom. Mutationer i en gen som kallas SURF1 (surfeit1) är den vanligaste orsaken till denna subtyp av Leigh-syndrom. Proteinet som SURF1 kodar för avslutas tidigt och kan därför inte utföra sin funktion, och herda underenheterna av COX till ett funktionellt proteinkomplex. Detta resulterar i ett underskott av COX-protein, vilket minskar mängden energi som produceras av mitokondrier. SURF1 ligger på den långa armen av kromosom 9 . En annan kärn-DNA-mutation som orsakar Leigh-syndrom påverkar ett annat proteinkomplex i mitokondrierna, pyruvatdehydrogenas , som är ett enzym i Link-reaktionsvägen . Vissa typer av SURF1-mutationer orsakar en subtyp av Leigh-syndrom som har en särskilt sen debut men på samma sätt varierande klinisk kurs.
Andra nukleära gener associerade med Leigh syndrom finns på kromosom 2 ( BCS1L och NDUFA10 ); kromosom 5 ( SDHA , NDUFS4 , NDUFAF2 och NDUFA2 ); kromosom 8 ( NDUFAF6 ), kromosom 10 ( COX15 ); kromosom 11 ( NDUFS3 , NDUFS8 och FOXRED1 ); kromosom 12 ( NDUFA9 och NDUFA12 ); och kromosom 19 ( NDUFS7 ). Många av dessa gener påverkar det första oxidativa fosforyleringskomplexet.
X-bundet Leigh syndrom

Leigh syndrom kan också orsakas av brist på pyruvatdehydrogenaskomplexet (PDHC), som oftast involverar en PDHC-underenhet som kodas av en X-länkad gen ( OMIM 308930 ). De neurologiska egenskaperna hos Leigh syndrom orsakade av PDHC-brist skiljer sig inte från andra former. Icke-neurologiska egenskaper (andra än mjölksyraacidos) ses dock inte vid PDHC-brist.
X-länkat recessivt Leigh-syndrom drabbar manliga barn mycket oftare än kvinnliga barn eftersom de bara har en kopia av X-kromosomen . Kvinnliga barn skulle behöva två kopior av den felaktiga genen för att påverkas av X-bundet Leigh-syndrom.
Franska kanadensiska Leigh syndromet
Den typ av Leigh-syndrom som hittades i mycket högre takt i Saguenay-Lac-Saint-Jean- regionen i Quebec orsakas av en mutation i LRPPRC- genen, belägen på den lilla ('p') armen av kromosom 2. Båda sammansatta heterozygositeten och homozygota mutationer har observerats i det franska kanadensiska Leigh-syndromet. Denna subtyp av sjukdomen beskrivs först 1993 hos 34 barn från regionen, som alla hade en allvarlig brist i cytokrom c-oxidas (COX), det fjärde komplexet i den mitokondriella elektrontransportkedjan . Även om underenheterna av proteinet som finns i de drabbade cellerna var funktionella, var de inte korrekt monterade. Bristen befanns vara nästan fullständig i hjärn- och levervävnader och betydande (cirka 50% av normal enzymaktivitet) i fibroblaster (bindvävsceller) och skelettmuskel . Njur- och hjärtvävnader visade sig inte ha COX-brist.
Franska kanadensiska Leigh syndromet har liknande symtom som andra typer av Leigh syndrom. Startåldern är i genomsnitt 5 månader och medianåldern för dödsfall är 1 år och 7 månader. Barn med sjukdomen är utvecklingsmässigt fördröjda , har milt avvikelser i ansiktsdrag, bland hypoplasi av mellanansiktet och bred nasal bridge , kronisk metabolisk acidos , och hypotoni (minskad muskelstyrka). Andra symtom inkluderar takypné (ovanligt snabb andningsfrekvens), dålig sugförmåga, hypoglykemi (lågt blodsocker) och skakningar . Allvarlig, plötslig metabolisk acidos är en vanlig dödsorsak.
Uppskattningar av frekvensen för genetiska bärare i regionen Saguenay-Lac-Saint-Jean varierar från 1 till 23 till 1 av 28; antalet barn födda med sjukdomen har uppskattats till 1 år 2063 till 1 av 2473 levande födda. Släktforskning tyder på att den ansvariga mutationen infördes i regionen av tidiga europeiska bosättare.
Patofysiologi
De karakteristiska symptomen på Leigh syndrom orsakas åtminstone delvis av bilaterala, fokala lesioner i hjärnstammen , basala ganglier , lillhjärnan och andra hjärnregioner. Skadorna tar olika former, inklusive områden med demyelinisering , spongios , glios , nekros och kapillärproliferation . Demyelinisering är förlusten av myelinhöljet runt nervcellernas axoner , vilket hämmar deras förmåga att kommunicera med andra nervceller. Hjärnstammen är involverad i att upprätthålla grundläggande livsfunktioner som andning, sväljning och cirkulation; basala ganglier och cerebellum kontrollerar rörelse och balans. Skador på dessa områden resulterar därför i de största symtomen på Leigh-syndromet - förlust av kontroll över funktioner som kontrolleras av dessa områden.
Laktacidosen ibland associerad med Leigh-syndrom orsakas av uppbyggnaden av pyruvat , som inte kan bearbetas hos individer med vissa typer av oxidativ fosforyleringsbrister. Pyruvat omvandlas antingen till alanin via alaninaminotransferas eller omvandlas till mjölksyra med laktatdehydrogenas ; båda dessa ämnen kan sedan byggas upp i kroppen.
Diagnos
Leigh syndrom föreslås av kliniska fynd och bekräftas med laboratorietest och genetisk testning.
Kliniska fynd
Dystoni, nystagmus och problem med det autonoma nervsystemet tyder på skada på basala ganglier och hjärnstammen som kan orsakas av Leigh syndrom. Andra symtom indikerar också hjärnskador, såsom hypertrikos och neurologiskt orsakad dövhet . Laboratoriefynd av laktacidos eller acidemi och hyperalaninemi (förhöjda nivåer av alanin i blodet) kan också föreslå Leigh-syndrom. Att bedöma nivån av organiska syror i urinen kan också indikera en dysfunktion i den metaboliska vägen .
Differentiell diagnos
Andra sjukdomar kan ha en liknande klinisk presentation som Leigh syndrom; Att utesluta andra orsaker till liknande kliniska symtom är ofta ett första steg för att diagnostisera Leigh syndrom. Förhållanden som kan se ut som Leigh-sjukdomen inkluderar perinatal asfyxi , kernicterus , kolmonoxidförgiftning , metanoltoxicitet , tiaminbrist , Wilsons sjukdom , biotin-respons basal ganglier sjukdom och vissa former av encefalit . Perinatal kvävning kan orsaka bilaterala ganglialskador och skada på talamus , som liknar de tecken som ses med Leigh-syndromet. När hyperbilirubinemi inte behandlas med fototerapi kan bilirubinet ackumuleras i basala ganglier och orsaka lesioner som liknar dem som ses i Leigh-syndromet. Detta är inte vanligt sedan fototerapi tillkom.
Behandling
Bärnstenssyra har studerats och visat sig vara effektiv för både Leigh syndrom och MELAS syndrom . En diet med hög fetthalt och lågt kolhydratinnehåll kan följas om en gen på X-kromosomen är inblandad i en persons Leigh-syndrom. Tiamin (vitamin B 1 ) kan ges om brist på pyruvatdehydrogenas är känd eller misstänkt. Symtomen på mjölksyraacidos behandlas genom att komplettera kosten med natriumbikarbonat (natron) eller natriumcitrat , men dessa ämnen behandlar inte orsaken till Leigh-syndromet. Dikloracetat kan också vara effektivt vid behandling av Leigh syndromassocierad mjölksyraacidos; forskning pågår om detta ämne. Koenzym Q10- tillskott har i vissa fall visat sig förbättra symtomen.
Kliniska prövningar av läkemedlet EPI-743 för Leigh syndrom pågår.
År 2016 utförde John Zhang och hans team vid New Hope Fertility Center i New York, USA, en spindelöverföring mitokondriell donationsteknik på en mamma i Mexiko som riskerade att producera en bebis med Leigh-sjukdom. En frisk pojke föddes den 6 april 2016. Det är dock ännu inte säkert om tekniken är helt pålitlig och säker.
Prognos
Olika genetiska orsaker och typer av Leigh-syndrom har olika prognoser, även om alla är dåliga. De allvarligaste formerna av sjukdomen, orsakad av full brist i ett av de drabbade proteinerna, orsakar död vid några års ålder. Om bristen inte är fullständig, är prognosen något bättre och ett drabbat barn förväntas överleva 6-7 år och i sällsynta fall till tonåren.
Epidemiologi
Leigh syndrom förekommer i minst 1 av 40000 levande födda, även om vissa populationer har mycket högre frekvenser. I regionen Saguenay-Lac-Saint-Jean i centrala Quebec förekommer Leigh-syndromet med en hastighet av 1 år 2000 nyfödda.
Historia
Leigh syndrom beskrevs först av Denis Leigh 1951 och skilde sig från liknande Wernickes encefalopati 1954. 1968 upptäcktes först sjukdomens koppling till mitokondriell aktivitet, även om mutationerna i cytokrom c oxidas och andra elektrontransportkedjeproteiner upptäcktes först 1977 .
Se även
Referenser
Vidare läsning
- GeneReviews / NCBI / NIH / UW-post om mitokondriellt DNA-associerat Leigh-syndrom och NARP
- OMIM-poster om mitokondriellt DNA-associerat Leigh-syndrom och NARP
- Leigh syndrom; Subakut nekrotiserande encefalopati; Leighs sjukdom vid NIH : s kontor för sällsynta sjukdomar
- leighsdisease på NINDS
- Maternally Inherited Leigh Syndrome vid NIH : s kontor för sällsynta sjukdomar
externa länkar
| Klassificering |
|---|


