Ketamin - Ketamine
 | |
 | |
| Kliniska data | |
|---|---|
| Handelsnamn | Ketalar, andra |
| Andra namn | CI-581; CL-369; CM-52372-2 |
| AHFS / Drugs.com | Monografi |
| Licensdata | |
| graviditet kategori |
|
| Addiction ansvar |
Låg - måttlig |
| Vägar administrering |
Några |
| Drogklass | NMDA -receptorantagonister ; Allmän bedövning ; Dissociativa hallucinogener ; Analgetika ; Antidepressiva medel |
| ATC -kod | |
| Rättslig status | |
| Rättslig status | |
| Farmakokinetiska data | |
| Biotillgänglighet |
|
| Proteinbindning | 23 till 47%. |
| Ämnesomsättning | Lever , tarm (oral): |
| Metaboliter | |
| Åtgärdens början |
|
| Eliminering halveringstid |
|
| Åtgärdens längd |
|
| Exkretion | |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.027.095 |
| Kemiska och fysiska data | |
| Formel | C 13 H 16 Cl N O |
| Molmassa | 237,73 g · mol −1 |
| 3D -modell ( JSmol ) | |
| Kiralitet | Racemisk blandning : |
| Smältpunkt | 92 ° C (198 ° F) |
| |
| |
| (kontrollera) | |
Ketamin är ett läkemedel som främst används för att starta och underhålla anestesi . Det framkallar dissociativ anestesi, en trance -liknande tillstånd som ger smärtlindring , sedering och amnesi . Ketaminanestesiens särdrag är bevarade andnings- och luftvägsreflexer, stimulerad hjärtfunktion med ökat blodtryck och måttlig bronkodilatation. Vid lägre subbedövningsdoser är ketamin ett lovande medel för smärta och behandlingsresistent depression . Den antidepressiva effekten av en enda administrering av ketamin avtar emellertid med tiden och effekterna av upprepad användning har inte studerats tillräckligt.
Psykiatriska biverkningar är frekventa såväl som förhöjt blodtryck och illamående. Lever- och urintoxicitet är vanligt bland vanliga användare av höga doser ketamin för fritidsändamål. Ketamin är en NMDA -receptorantagonist , och det står för de flesta av dess handlingar utom den antidepressiva effekten, vars mekanism är en fråga om mycket forskning och debatt.
Ketamin upptäcktes 1956 och godkändes för användning i USA 1970. Det användes regelbundet på hundar och hästar och användes i stor utsträckning för kirurgisk anestesi i Vietnamkriget . Ketamin används också som rekreationsmedicin , både i pulverform och flytande form, för dess hallucinogena och dissociativa effekter.
Det finns på Världshälsoorganisationens lista över viktiga läkemedel . Det finns som en generisk medicinering .
Medicinsk användning
Anestesi
Användningen av ketamin i anestesi speglar dess egenskaper. Det är ett läkemedel som valts för kortsiktiga ingrepp när muskelavslappning inte krävs. Ketamins effekt på andnings- och cirkulationssystemet skiljer sig från andra bedövningsmedel. Det undertrycker andning mycket mindre än de flesta andra tillgängliga bedövningsmedel. När det används vid bedövningsdoser, stimulerar ketamin vanligtvis snarare än att trycka ned cirkulationssystemet. Skyddande luftvägsreflexer bevaras, och det är ibland möjligt att administrera ketaminanestesi utan skyddsåtgärder för luftvägarna. Psykotomimetiska effekter begränsar acceptansen av ketamin; de kan emellertid motverkas genom administrering av bensodiazepiner eller propofol .
Ketamin används ofta hos svårt skadade personer och verkar vara säker i denna grupp. Det har använts i stor utsträckning för akutoperationer vid fältförhållanden i krigszoner, till exempel under Vietnamkriget . En riktlinje från klinisk praxis från 2011 stöder användningen av ketamin som lugnande medel i akutmedicin , inklusive under fysiskt smärtsamma ingrepp. Det är det valda läkemedlet för personer i traumatisk chock som löper risk för hypotoni . Lågt blodtryck är skadligt för personer med allvarlig huvudskada, och ketamin är minst sannolikt att orsaka lågt blodtryck och ofta till och med kunna förhindra det.
Ketamin är ett alternativ för barn, som enda bedövningsmedel för mindre ingrepp eller som ett induktionsmedel följt av neuromuskulär blockerare och trakeal intubation Särskilt barn med cyanotisk hjärtsjukdom och neuromuskulära störningar är bra kandidater för ketaminanestesi.
På grund av ketamins bronkodilaterande egenskaper kan den användas för anestesi hos personer med astma , kronisk obstruktiv luftvägssjukdom och med svår reaktiv luftvägssjukdom inklusive aktiv bronkospasm .
Smärta
Ketamininfusioner används för akut smärtbehandling på akutmottagningar och under perioperativ period hos individer med eldfast smärta. Doserna är lägre än de som används för anestesi; de brukar kallas sub-bedövningsdoser. Tillägg till morfin eller på egen hand minskar ketamin morfinanvändning , smärtnivå, illamående och kräkningar efter operationen. Ketamin kommer sannolikt att vara mest fördelaktigt för kirurgiska patienter när svår postoperativ smärta förväntas och för opioidtoleranta patienter.
Ketamin är särskilt användbart i prehospitalt miljö, på grund av dess effektivitet och låg risk för andningsdepression. Ketamin har liknande effekt som opioider på sjukhusets akutmottagning för behandling av akut smärta och för kontroll av procedurell smärta. Det kan också förhindra opioidinducerad hyperalgesi och postanestetisk skakning .
För kronisk smärta används ketamin som intravenöst smärtstillande medel, särskilt om smärtan är neuropatisk. Det har den extra fördelen att motverka ryggmärgsensibilisering eller avvecklingsfenomen som upplevs med kronisk smärta . I flera kliniska prövningar levererade ketamininfusioner kortsiktig smärtlindring vid neuropatiska smärtdiagnoser, smärta efter traumatisk ryggradskada, fibromyalgi och komplext regionalt smärtsyndrom (CRPS). 2018 års konsensusriktlinjer för kronisk smärta drog dock slutsatsen att det totalt sett bara finns svaga bevis för ketaminanvändning vid ryggskada, måttliga bevis för ketamin för CRPS och svaga eller inga bevis för ketamin vid blandad neuropatisk smärta, fibromyalgi och cancervärk. I synnerhet finns det bara för CRPS tecken på smärtlindring på medellång till längre sikt.
Depression
Ketamin är ett robust och snabbverkande antidepressivt medel , även om dess effekt är övergående. Intravenös ketamininfusion vid behandlingsresistent depression resulterar i förbättrat humör inom 4 timmar och når toppen vid 24 timmar. Effekten minskas efter 7 dagar, och de flesta patienter återfaller inom 10 dagar, även om förbättringen kan pågå i 30 dagar eller längre för en betydande minoritet. Den främsta utmaningen med ketaminbehandling är vad man ska göra när den antidepressive effekten löper ut. Underhållsterapin med ketamin (från två gånger i veckan till en gång i två veckor) verkar vara ett lovande alternativ, även om bevisen för att bestämt rekommendera det är otillräckliga. Ketamin kan också minska självmordstankar i upp till tre dagar efter injektionen. Ketamin kan vara effektivt för bipolär depression , men uppgifterna om dess användning är knappa.
Det har visat sig att en enda dos av iv ketamin resulterar i en svarsfrekvens över 60% så tidigt som 4,5 timmar efter dosen (med ihållande effekt efter 24 timmar) och över 40% efter 7 dagar.
Även om det bara finns några pilotstudier som studerar den optimala dosen, tyder ökande bevis på att 0,5 mg/kg dos injicerad över 40 minuter ger ett optimalt resultat.
Ketamin har inte godkänts för användning som ett antidepressivt medel, men det kanadensiska nätverket för humör- och ångestbehandlingar rekommenderar det som en tredje linjens behandling för depression. En av enantiomererna av ketamin, esketamin , har godkänts som en nässpray för behandlingsresistent depression i USA och på andra ställen (se Esketamine#Depression ). Intravenös infusion av ketamin har aldrig jämförts direkt med intranasalt esketamin, men en jämförande metaanalys av kliniska prövningar indikerar överlägsenhet av intravenös ketamin, som har större övergripande respons och remission, och ett lägre antal bortfall.
Beslag
Ketamin används ibland vid behandling av status epilepticus som inte har svarat tillräckligt på standardbehandlingar, även om endast begränsade bevis (fallstudier och inga randomiserade kontrollerade prövningar) finns till fördel.
Kontraindikationer
Huvudkontraindikationer för ketamin:
- Allvarlig kardiovaskulär sjukdom som instabil angina eller dåligt kontrollerad hypertoni
- Ökat intrakraniellt eller intraokulärt tryck. Båda dessa kontraindikationer är kontroversiella
- Dåligt kontrollerad psykos
- Allvarlig leversjukdom som cirros
- Graviditet
- Störning av aktiv substans (för seriella ketamininjektioner)
- Ålder mindre än 3 månader
Bieffekter
Vid bedövningsdoser upplever 10–20% av vuxna (1-2% av barnen) negativa psykiatriska reaktioner som uppstår under uppkomsten av anestesi, allt från drömmar och dysfori till hallucinationer och uppkomstdelirium . Dessa kan motverkas genom förbehandling med bensodiazepin eller propofol . Ketaminanestesi orsakar vanligtvis tonisk - kloniska rörelser (mer än 10% av människorna) och sällan hypertoni . Kräkningar kan förväntas hos 5–15% av patienterna; förbehandling med propofol mildrar det också. Laryngospasm förekommer endast sällan med ketamin. Ketamin stimulerar i allmänhet andningen; under de första 2-3 minuterna av en högdos snabb intravenös injektion kan det dock orsaka en övergående andningsdepression.
Vid lägre subbedövningsdoser är psykiatriska biverkningar framträdande. En majoritet av patienterna känner sig konstiga, rymliga, luddiga eller flytande eller har visuella snedvridningar eller domningar. Mycket vanliga (20–50%) är svårigheter att tala, förvirring, eufori, dåsighet och koncentrationssvårigheter. Symtomen på psykos som att gå in i ett hål, försvinna, känna sig smälta, uppleva färger och hallucinationer beskrivs av 6–10% av människorna. Yrsel, dimsyn, muntorrhet, högt blodtryck, illamående, ökad/minskad kroppstemperatur eller rodnadskänsla är de vanliga (> 10%) icke-psykiatriska biverkningarna. Alla dessa negativa effekter är mest uttalade vid slutet av injektionen, reduceras dramatiskt 40 minuter efter och försvinner helt inom 4 timmar efter injektionen.
Urin- och levertoxicitet
Urintoxicitet förekommer främst hos personer som regelbundet använder stora mängder ketamin, där 20–30% av de frekventa användarna har blåsor. Det inkluderar en rad sjukdomar från blåsor till hydronefros till njursvikt . De typiska symptomen på ketamininducerad cystit är frekvent urinering , dysuri och brådskande urin ibland som åtföljs av smärta under urinering och blod i urinen . Skadan på blåsväggen har likheter med både interstitiell och eosinofil cystit . Väggen är förtjockad och den funktionella urinblåsan är så låg som 10–150 ml.
Hantering av ketamininducerad cystit innefattar ketaminavbrott som det första steget. Detta följs av NSAID och antikolinergika och, om svaret är otillräckligt, av tramadol . Andra linjens behandlingar är epitelskyddsmedel såsom oralt pentosanpolysulfat eller intravesikal (intrablåsan) instillation av hyaluronsyra . Intravesikalt botulinumtoxin är också användbart.
Levertoxicitet av ketamin innebär också högre doser och upprepad administrering. I en grupp av kroniska högdoserade ketaminanvändare rapporterades frekvensen av leverskada vara cirka 10%. Det finns fallrapporter om ökade leverenzymer som involverar ketaminbehandling av kronisk smärta.
Beroende och tolerans
Även om förekomsten av ketaminberoende är okänd, utvecklar vissa människor som regelbundet använder ketamin ketaminberoende. Djurförsök bekräftar också risken för missbruk. Dessutom kan den snabba effekten av insufflering öka efter läkemedlets potential för fritidsanvändning. Den korta varaktigheten av effekter främjar bingeing . Ketamin tolerans snabbt utvecklas, även med upprepad medicinsk användning, vilket föranledde användning av högre doser. Vissa dagliga användare rapporterade abstinenssymtom , främst ångest, skakningar, svettningar och hjärtklappning, efter försöken att sluta. Kognitiva underskott samt ökad dissociation och vanföreställningssymtom observerades hos frekventa fritidsanvändare av ketamin.
Interaktioner
Ketamin förstärker de lugnande effekterna av propofol och midazolam . Naltrexon förstärker psykotomimetiska effekter av en låg dos ketamin, medan lamotrigin och nimodipin minskar dem. Klonidin minskar saliven, hjärtfrekvensen och blodtrycket ökar under ketaminanestesi och minskar förekomsten av mardrömmar.
Kliniska observationer tyder på att bensodiazepiner kan minska de antidepressiva effekterna av ketamin. Ketamin används ofta för att behandla resistent depression som ett tillägg till en mängd olika antidepressiva medel. Därför verkar det som om de flesta konventionella antidepressiva läkemedel säkert kan kombineras med ketamin.
Farmakologi
Farmakodynamik
Handlingsmekanism
Antagonism hos NMDA -receptorn är ansvarig för de bedövande, analgetiska och psykotomimetiska effekterna av ketamin. NMDA -receptorantagonism resulterar i analgesi genom att förhindra central sensibilisering i dorsala hornneuroner; med andra ord, ketamins handlingar stör smärtöverföring i ryggmärgen .
Ketamins antidepressiva verkan är osäker. Det är inte klart om NMDA -receptorn är ensam ansvarig för denna åtgärd eller om interaktioner med andra receptorer också är nödvändiga. Det är inte klart om ketamin ensam är tillräckligt för den antidepressiva effekten eller dess metaboliter är också viktiga. Det har i alla fall klargjorts att akut blockad av NMDA-receptorer i hjärnan resulterar i en aktivering av α-amino-3-hydroxi-5-metyl-4-isoxazolepropionsyra-receptorer (AMPA-receptorer), som i sin tur modulerar en mängd av nedströms signalvägar för att påverka neurotransmission i det limbiska systemet och förmedla antidepressiva effekter av NMDA -receptorantagonister som ketamin. Sådana nedströms åtgärder för denna aktivering av AMPA-receptorer inkluderar uppreglering av hjärnhärledd neurotrofisk faktor (BDNF) och aktivering av dess signalreceptor tropomyosinreceptorkinas B (TrkB), aktivering av däggdjursmålet för rapamycin (mTOR) väg, deaktivering av glykogensyntas kinas 3 (GSK-3) och hämning av fosforylering av eukaryot förlängningsfaktor 2 (eEF2) kinas . Förutom blockering av NMDA-receptorn kan den aktiva metaboliten av ketaminhydroxynorketamin, som inte interagerar viktigt med NMDA-receptorn men inte desto mindre indirekt aktiverar AMPA-receptorer på samma sätt, också eller alternativt vara inblandad i de snabbt antidepressiva effekterna av ketamin. Ny forskning har klargjort att en akut inhibering av lateral habenula , en del av hjärnan i det limbiska systemet som har kallats "anti-belöningscentrum" (projicerar till och hämmar den mesolimbiska belöningsvägen och modulerar andra limbiska områden) , kan vara inblandade i ketidins antidepressiva effekter.
Ketamin är en blandning av lika stora mängder av två enantiomerer : esketamin och arketamin . Esketamin är en mer potent NMDA -receptorantagonist och dissociativ hallucinogen än arketamin. På grund av hypotesen att NMDA -receptorantagonism ligger till grund för ketaminens antidepressiva effekter, utvecklades esketamin som ett antidepressivt medel. Emellertid har flera andra NMDA-receptorantagonister , inklusive memantin , lanicemin , rislenemdaz , rapastinel och 4-klorokynurenin , hittills inte visat tillräcklig effektivitet för depression. Vidare indikerar djurförsök som arketamine, enantiomeren med en svagare NMDA-receptorantagonism, samt (2 R , 6 R ) -hydroxynorketamine , den metabolit med försumbar affinitet för NMDA-receptorn men en potent alfa-7 nikotinreceptorantagonist kan ha antidepressiv verkan. Det hävdas nu att NMDA -receptorantagonism kanske inte är ansvarig för ketaminens antidepressiva effekter.
Molekylära mål
| Webbplats | Värde ( μM ) | Typ | Handling | Arter | Ref |
|---|---|---|---|---|---|
| NMDA | 0,25–0,66 | K i | Antagonist | Mänsklig | |
| MOR | 42 | K i | Antagonist | Mänsklig | |
| MOR 2 | 12.1 | K i | Antagonist | Mänsklig | |
| KOR | 28 25 |
K i K i |
Antagonist Agonist |
Mänsklig |
|
| σ 2 | 26 | K i | ND | Råtta | |
| D 2 | 0,5 > 10 |
K i K i |
Agonist ND |
Mänsklig |
|
| M 1 | 45 | K i | ND | Mänsklig | |
| α 2 β 2 | 92 | IC 50 | Antagonist | Mänsklig | |
| α 2 β 4 | 29 | IC 50 | Antagonist | Mänsklig | |
| α 3 β 2 | 50 | IC 50 | Antagonist | Mänsklig | |
| α 3 β 4 | 9.5 | IC 50 | Antagonist | Mänsklig | |
| α 4 β 2 | 72 | IC 50 | Antagonist | Mänsklig | |
| α 4 β 4 | 18 | IC 50 | Antagonist | Mänsklig | |
| α 7 | 3.1 | IC 50 | Antagonist | Råtta | |
| ERα | 0,34 | K i | ND | Mänsklig | |
| NETTO | 82–291 | IC 50 | Inhibitor | Mänsklig | |
| DAT | 63 | K i | Inhibitor | Råtta | |
| HCN1 | 8–16 | EC 50 | Inhibitor | Mus | |
| Ju mindre värde, desto starkare interaktion med webbplatsen. | |||||
Ketamin fungerar huvudsakligen som en antagonist av NMDA -receptorn , en jonotropisk glutamatreceptor . Den S (+) och R (-) stereoisomerer av ketamin binder till dizocilpin på NMDA-receptorn med olika affiniteter , fd visar approximativt 2- till 3-faldigt högre affinitet till receptorn än den senare.
Ketamin kan också interagera med och hämma NMDAR via en annan allosterisk plats på receptorn.
Med ett par undantag är ketaminåtgärder vid andra receptorer mycket svagare än ketamins antagonism mot NMDA -receptorn (se aktivitetstabellen till höger).
Även om ketamin är en mycket svag ligand av monoamin transportörer (K i > 60 ^ M), har det föreslagits att det kan interagera med allosteriska platser på monoamin transportörer för att producera monoaminåterupptagshämning . Emellertid ingen funktionell hämning ( IC 50 har) av de humana monoamin transportörer observerats med ketamin eller dess metaboliter vid koncentrationer av upp till 10 tusen nM. Dessutom har djurstudier och åtminstone tre rapporter om mänskliga fall inte funnit någon interaktion mellan ketamin och monoaminoxidashämmare (MAOI) tranylcypromin , vilket är viktigt eftersom kombinationen av en monoaminåterupptagshämmare med en MAO -hämmare kan ge allvarlig toxicitet såsom serotonergt syndrom eller hypertensiv kris . Sammantaget ifrågasätter dessa fynd tvivel på inblandningen av monoaminåterupptagshämning i effekterna av ketamin hos människor. Ketamin har visat sig öka dopaminerg neurotransmission i hjärnan, men istället för att bero på hämning av dopaminåterupptag kan detta ske via indirekta/nedströms mekanismer, nämligen genom antagonism av NMDA -receptorn.
Huruvida ketamin är en agonist till D 2 receptorer är kontroversiell. Tidig forskning av Philip Seeman s grupp fann ketamin vara en D 2 partiell agonist med potensen liknande den i dess NMDA-receptorantagonism. Emellertid senare studier av olika forskare funnit affiniteten hos ketamin av> 10 ^ M för reguljärt humant och rått-D 2 -receptorer, Dessutom, medan D 2 -receptoragonister såsom bromokriptin har möjlighet att snabbt och kraftfullt undertrycka prolaktin utsöndring , subanesthetic doser av ketamin har har inte visat sig göra detta hos människor och har faktiskt visat sig att dosberoende ökar prolaktinnivåerna. Imagingstudier har visat blandade resultat på inhibering av striatal [ 11 C] raclopridbindning av ketamin hos människor, medan vissa studier fann en signifikant minskning och andra fann ingen sådan effekt. Men förändringar i [ 11 C] rakloprid-bindning kan bero på förändringar i dopaminkoncentrationer inducerade av ketamin snarare än bindning av ketamin till D 2 receptorn.
Förhållanden mellan nivåer och effekter
Dissociation och psykotomimetiska effekter rapporteras hos patienter som behandlats med ketamin vid plasmakoncentrationer på cirka 100 till 250 ng/ml (0,42–1,1 μM). Den typiska intravenösa antidepressiva dosen av ketamin som används för att behandla depression är låg och resulterar i maximala plasmakoncentrationer på 70 till 200 ng/ml (0,29–0,84 μM). Vid liknande plasmakoncentrationer (70 till 160 ng/ml; 0,29–0,67 μM) visar det också smärtstillande effekter. På 1–5 minuter efter att anestesi inducerats genom en snabb intravenös injektion av ketamin når dess plasmakoncentration så högt som 60–110 μM. När bedövningen upprätthölls med användning av lustgas tillsammans med kontinuerlig injektion av ketamin stabiliserades ketaminkoncentrationen vid cirka 9,3 μM. I ett experiment med rent ketaminanestesi började patienterna vakna när plasmanivån av ketamin minskade till cirka 2600 ng/ml (11 μM) och blev orienterad på plats och tid när nivån var nere till 1000 ng/ml (4 μM) . I en enstaka studie varierade koncentrationen av ketamin i cerebrospinalvätska , en proxy för hjärnkoncentrationen, under anestesi mellan 2,8 och 6,5 μM och var cirka 40% lägre än i plasma.
Farmakokinetik
Ketamin kan absorberas på många olika sätt på grund av både dess vatten- och lipidlöslighet. Intravenös ketamin biotillgängligheten är 100% per definition, är intramuskulär injektion biotillgängligheten något lägre vid 93%, och epidural biotillgänglighet är 77%. Subkutan biotillgänglighet har aldrig mätts men antas vara hög. Bland de mindre invasiva vägarna har intranasal den högsta biotillgängligheten (45–50%) och oralt - den lägsta (16–20%). Sublinguala och rektala biotillgängligheter är mellanliggande med cirka 25–50%.
Efter absorptionen distribueras ketamin snabbt till hjärnan och andra vävnader. Den plasmaproteinbindning av ketamin är variabel vid 23 till 47%.
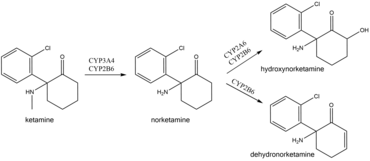
I kroppen genomgår ketamin en omfattande metabolism . Det biotransformeras av CYP3A4 och CYP2B6 isoenzymer till norketamin , som i sin tur omvandlas av CYP2A6 och CYP2B6 till hydroxynorketamin och dehydronorketamin . Låg oral biotillgänglighet av ketamin beror på first-pass-effekten och möjligen ketamin-tarmmetabolismen av CYP3A4. Som ett resultat är norketamins plasmanivåer flera gånger högre än ketamin efter oral administrering, och norketamin kan spela en roll vid bedövning och analgetisk verkan av oral ketamin. Detta förklarar också varför orala ketaminnivåer är oberoende av CYP2B6 -aktivitet, till skillnad från subkutana ketaminnivåer.
Efter en intravenös injektion av tritium -märkt ketamin, är 91% av radioaktiviteten utvanns från urin och 3% från avföring. Läkemedlet utsöndras mestadels i form av metaboliter , med endast 2% oförändrade. Konjugerade hydroxylerade derivat av ketamin (80%) följt av dehydronorketamin (16%) är de vanligaste metaboliterna som upptäcks i urinen.
Kemi
Syntes
2-klorbensonitril omsätts med Grignard-reagenset cyklopentylmagnesiumbromid för att ge (2-klorfenyl) (cyklopentyl) metanon. Detta bromeras sedan med användning av brom för att bilda motsvarande bromoketon, som sedan bringas att reagera med metylamin i en vattenlösning för att bilda metyliminoderivatet, 1- (2-klor-N-metylbensimidoyl) cyklopentanol , med hydrolys av den tertiära bromatomen. Denna slutliga mellanprodukt upphettas sedan i dekalin eller ett annat lämpligt högkokande lösningsmedel, på vilket en ombyggnad av ringutvidgning sker och bildar ketamin.
Strukturera
I kemisk struktur är ketamin ett arylcyklohexylaminderivat . Ketamin är en kiral förening. Den mer aktiva enantiomeren, esketamin ( S -ketamin), är också tillgänglig för medicinskt bruk under varumärket Ketanest S, medan den mindre aktiva enantiomeren, arketamin ( R -ketamin), aldrig har marknadsförts som ett enantiopent läkemedel för kliniskt bruk.
Den optiska rotationen av en given enantiomer av ketamin kan variera mellan dess salter och fri basform . Den fria basformen av ( S ) -ketamin uppvisar dextrorotation och är därför märkt ( S ) - (+) - ketamin. Emellertid dess hydrokloridsalt visar levorotation är och sålunda märkta ( S ) - (-) - ketaminhydroklorid.
Upptäckt
Ketamin kan kvantifieras i blod eller plasma för att bekräfta en diagnos av förgiftning hos patienter på sjukhus, tillhandahålla bevis vid nedsatt körstopp eller för att hjälpa till vid en medicinsk legal dödsutredning. Blod- eller plasmaketaminkoncentrationer ligger vanligtvis i intervallet 0,5–5,0 mg/L hos personer som får läkemedlet terapeutiskt (under narkos), 1–2 mg/L hos de som gripits för nedsatt körning och 3–20 mg/L hos offer av akut dödlig överdosering. Urin är ofta det föredragna exemplaret för rutinmässiga övervakningsändamål. Närvaron av norketamin, en farmakologiskt aktiv metabolit, är användbar för bekräftelse av ketaminintag.
Historia
Ketamin syntetiserades först 1962 av Calvin L. Stevens , professor i kemi vid Wayne State University och en Parke-Davis- konsult. Det var känt under utvecklingskodnamnet CI-581 . Efter lovande preklinisk forskning på djur testades ketamin hos mänskliga fångar 1964. Dessa undersökningar visade ketamins korta verkningstid och minskade beteendestoxicitet gjorde det till ett fördelaktigt val framför fencyclidine (PCP) som bedövningsmedel. Forskarna tänkte kalla tillståndet för ketaminanestesi "drömma" men Parke-Davis tyckte inte om det. När hon hörde om detta problem och om patienternas "frånkopplade" utseende föreslog fruen till en av farmakologerna som arbetar med ketamin, Edward Domino, "dissociativ anestesi". Efter FDA -godkännande 1970 gavs ketaminanestesi först till amerikanska soldater under Vietnamkriget .
Upptäckten av ketamins antidepressiva verkan år 2000 har beskrivits som det enskilt viktigaste framsteget vid behandling av depression på över 50 år. Det har väckt intresse för NMDA -receptorantagonister för depression och har flyttat riktningen för forskning och utveckling av antidepressiva medel.
Samhälle och kultur
Rättslig status
Medan ketamin marknadsförs lagligt i många länder världen över, är det också ett kontrollerat ämne i många länder.
- I Australien är ketamin listat som ett schema 8 kontrollerat läkemedel enligt Poisons Standard (oktober 2015).
- I Kanada har ketamin klassificerats som ett narkotiskt schema I sedan 2005.
- I december 2013 har Indiens regering , som svar på den ökande fritidsanvändningen och användningen av ketamin som en våldtäktsdrog, lagt till den i schema X i läkemedels- och kosmetikallagen som kräver en särskild licens för försäljning och underhåll av register över alla försäljning i två år.
- I Storbritannien märktes det som ett läkemedel i klass B den 12 februari 2014.
- Ökningen av fritidsanvändningen fick ketamin att placeras i Schema III i USA: s kontrollerade ämneslag i augusti 1999.
Fritidsbruk
Vid subanestetiska doser producerar ketamin ett dissociativt tillstånd , kännetecknat av en känsla av lossning från ens fysiska kropp och den yttre världen som kallas depersonalisering och derealisering . Vid tillräckligt höga doser kan användare uppleva det som kallas "K-hålet", ett tillstånd av dissociation med visuella och hörselhallucinationer. John C. Lilly , Marcia Moore , DM Turner och David Woodard (bland andra) har skrivit mycket om sin egen enteogena användning av och psykonautiska erfarenheter av ketamin. Turner dog för tidigt på grund av drunkning under förmodad användning utan tillsyn av ketamin. År 2006 den ryska utgåvan av Adam Parfrey s Apocalypse kultur II förbjöds och förstördes av myndigheter på grund av dess införande av en essä av Woodard om entheogenic användning av och psychonautic erfarenheter med ketamin. Fritidsanvändning av ketamin har varit inblandad i dödsfall globalt, med mer än 90 dödsfall i England och Wales åren 2005–2013. De inkluderar oavsiktliga förgiftningar, drunkningar, trafikolyckor och självmord. Majoriteten av dödsfallen var bland unga. På grund av dess förmåga att orsaka förvirring och minnesförlust har ketamin använts för dadelvåldtäkt .
Forskning
Den ryska läkaren Evgeny Krupitsky har hävdat att han har uppnått uppmuntrande resultat genom att använda ketamin som en del av en behandling för alkoholstörning , som kombinerar psykedeliska och aversiva tekniker. Krupitsky och Kolp sammanfattade sitt arbete hittills 2007.
Veterinärmedicin
Vid veterinärbedövning används ketamin ofta för sina bedövnings- och smärtstillande effekter på katter, hundar, kaniner , råttor och andra smådjur. Det används ofta vid induktion och narkosunderhåll hos hästar. Det är en viktig del av " gnagarcocktailen ", en blandning av läkemedel som används för att bedöva gnagare . Veterinärer använder ofta ketamin med lugnande läkemedel för att producera balanserad anestesi och analgesi, och som en konstant infusion för att förhindra smärta . Ketamin används också för att hantera smärta bland stora djur. Det är det primära intravenösa bedövningsmedlet som används vid hästkirurgi, ofta i samband med detomidin och tiopental , eller ibland guaifenesin .
Ketamin verkar inte producera sedering eller bedövning hos sniglar. Istället verkar det ha en excitatorisk effekt.
Referenser
externa länkar
- "Ketamin" . Läkemedelsinformationsportal . US National Library of Medicine.
- "Ketaminhydroklorid" . Läkemedelsinformationsportal . US National Library of Medicine.
- DEA: Ketamin Faktablad