Destillation -Distillation
Destillation , eller klassisk destillation, är processen att separera komponenterna eller ämnena från en flytande blandning genom att använda selektiv kokning och kondensation . Torrdestillation är uppvärmning av fasta material för att producera gasformiga produkter (som kan kondensera till vätskor eller fasta ämnen). Torrdestillation kan innebära kemiska förändringar såsom destruktiv destillation eller sprickbildning och diskuteras inte under denna artikel. Destillation kan resultera i väsentligen fullständig separation (nästan rena komponenter), eller så kan det vara en partiell separation som ökar koncentrationen av utvalda komponenter i blandningen. I båda fallen utnyttjar processen skillnader i den relativa flyktigheten hos blandningens komponenter. I industriella tillämpningar är destillation en enhetsoperation av praktiskt taget universell betydelse, men det är en fysisk separationsprocess, inte en kemisk reaktion .
Destillation har många tillämpningar. Till exempel:
- Destillering av jästa produkter ger destillerade drycker med hög alkoholhalt , eller separerar andra jäsningsprodukter av kommersiellt värde.
- Destillation är en effektiv och traditionell metod för avsaltning .
- Inom petroleumindustrin är oljestabilisering en form av partiell destillation som minskar ångtrycket hos råolja, vilket gör den säker för lagring och transport samt minskar de atmosfäriska utsläppen av flyktiga kolväten. I mellanverksamheter vid oljeraffinaderier är fraktionerad destillation en viktig verksamhetsklass för att omvandla råolja till bränslen och kemiska råvaror .
- Kryogen destillation leder till separation av luft i dess komponenter – särskilt syre , kväve och argon – för industriellt bruk .
- Inom den kemiska industrin destilleras stora mängder råa flytande produkter från kemisk syntes för att separera dem, antingen från andra produkter, från föroreningar eller från oreagerade utgångsmaterial.
En anläggning som används för destillering, särskilt av destillerade drycker, är ett destilleri. Själva destillationsutrustningen är en destillation .
Historia

Tidiga bevis på destillation hittades på akkadiska tabletter daterade c. 1200 f.Kr. som beskriver parfymverksamhet. Tabletterna gav textbevis för att en tidig primitiv form av destillation var känd för babylonierna i det forntida Mesopotamien . Tidiga bevis på destillation hittades också relaterade till alkemister som arbetade i Alexandria i det romerska Egypten under 1:a århundradet CE.
Destillation praktiserades i den forntida indiska subkontinenten , vilket framgår av bakade lerretorter och mottagare som hittats vid Taxila , Shaikhan Dheri och Charsadda i det moderna Pakistan , som dateras till de tidiga århundradena av den gemensamma epoken . Dessa " Gandhara destillations" kunde bara producera mycket svag sprit , eftersom det inte fanns något effektivt sätt att samla upp ångorna vid låg värme. Destillerat vatten har använts sedan åtminstone ca. 200 e.Kr., när Alexander av Afrodisias beskrev processen. Arbetet med att destillera andra vätskor fortsatte i det tidiga bysantinska Egypten under Zosimus av Panopolis på 300-talet.
Destillering i Kina kan ha börjat under den östra Han -dynastin (1:a–2:a århundradena e.Kr.), men destilleringen av drycker började i dynastierna Jin (1100–1200-talen) och södra Song (10–1200-talen), enligt arkeologiska bevis.
Medeltida muslimska kemister som Jābir ibn Ḥayyān (latin: Geber, 800-talet) och Abū Bakr al-Rāzī (latin: Rhazes, ca 865–925 ) experimenterade omfattande med destillering av olika ämnen.
Destilleringen av vin är intygad i arabiska verk som tillskrivs al-Kindī (ca 801–873 e.Kr.) och till al-Fārābī (ca 872–950), och i den 28:e boken av al-Zahrāwīs (latin: Abulcasis) , 936–1013) Kitāb al-Taṣrīf (senare översatt till latin som Liber servatoris ). På 1100-talet började recept för framställning av aqua ardens ("brinnande vatten", dvs. etanol) genom att destillera vin med salt att dyka upp i ett antal latinska verk, och i slutet av 1200-talet hade det blivit en utbredd känt ämne bland västeuropeiska kemister. Taddeo Alderottis ( 1223–1296) verk beskriver en metod för att koncentrera alkohol med upprepad destillation genom en vattenkyld destillation, genom vilken en alkoholrenhet på 90 % kunde erhållas.
Fraktionerad destillation av organiska ämnen spelar en viktig roll i de verk som tillskrivs Jābir ibn Ḥayyān, såsom i Kitāb al-Sabʿīn ('Boken om de sjuttio'), översatt till latin av Gerard av Cremona (ca 1114–1187) under titeln Liber de septuaginta . Jabiriska experiment med fraktionerad destillation av animaliska och vegetabiliska ämnen, och i mindre grad även av mineralämnen, är huvudämnet för De anima in arte alkimiae , ett ursprungligen arabiskt verk som felaktigt tillskrivits Avicenna som översattes till latin och skulle gå vidare för att bilda den viktigaste alkemiska källan för Roger Bacon ( ca 1220–1292 ).
En destillation hittades på en arkeologisk plats i Qinglong, Hebei -provinsen, i Kina, med anor från 1100-talet. Destillerade drycker var vanliga under Yuan-dynastin (1200–1300-talen).
År 1500 publicerade den tyske alkemisten Hieronymus Braunschweig Liber de arte destillandi ( Boken om konsten att destillera ), den första boken enbart tillägnad ämnet destillation, följt 1512 av en mycket utökad version. År 1651 publicerade John French The Art of Destillation , det första stora engelska kompendiet om praktiken, men det har hävdats att mycket av det härrör från Braunschweigs arbete. Detta inkluderar diagram med personer i dem som visar verksamhetens industriella snarare än bänkskalan.



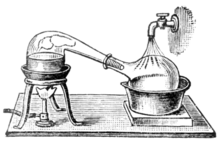
När alkemin utvecklades till vetenskapen om kemi , användes kärl som kallas retorter för destillationer. Både alembics och retorter är former av glasvaror med långa halsar som pekar åt sidan i en nedåtgående vinkel för att fungera som luftkylda kondensorer för att kondensera destillatet och låta det droppa nedåt för uppsamling. Senare uppfanns koppar alembics. Nitfogar hölls ofta täta genom att använda olika blandningar, till exempel en deg gjord av rågmjöl. Dessa alembics hade ofta ett kylsystem runt näbben, med till exempel kallt vatten, vilket gjorde kondenseringen av alkohol mer effektiv. Dessa kallades pot stills . Idag har retorterna och pot stills till stor del ersatts av effektivare destillationsmetoder i de flesta industriella processer. Emellertid används potten fortfarande i stor utsträckning för framställning av några fina alkoholer, såsom konjak , skotsk whisky , irländsk whisky , tequila , rom , cachaça och en del vodka . Pot stills gjorda av olika material (trä, lera, rostfritt stål) används också av bootleggers i olika länder. Små pot stills säljs också för användning i inhemsk produktion av blomvatten eller eteriska oljor .
Tidiga former av destillation involverade satsvisa processer med en förångning och en kondensation. Renheten förbättrades genom ytterligare destillation av kondensatet. Större volymer bearbetades genom att helt enkelt upprepa destillationen. Kemister har enligt uppgift utfört så många som 500 till 600 destillationer för att få en ren förening.
I början av 1800-talet utvecklades grunderna för modern teknik, inklusive förvärmning och återflöde . År 1822 utvecklade Anthony Perrier en av de första kontinuerliga stillbilderna, och sedan, 1826, förbättrade Robert Stein den designen för att göra sitt patentstillbildande . 1830 fick Aeneas Coffey patent för att förbättra designen ytterligare. Coffeys kontinuerliga stillbild kan betraktas som arketypen för moderna petrokemiska enheter. Den franske ingenjören Armand Savalle utvecklade sin ångregulator runt 1846. 1877 beviljades Ernest Solvay ett amerikanskt patent på en trågkolonn för ammoniakdestillation , och samma och efterföljande år såg utvecklingen inom detta tema för oljor och sprit.
Med framväxten av kemiteknik som en disciplin i slutet av 1800-talet kunde vetenskapliga metoder snarare än empiriska tillämpas. Den utvecklande petroleumindustrin i början av 1900-talet gav impulsen till utvecklingen av exakta designmetoder, som McCabe-Thiele-metoden av Ernest Thiele och Fenske-ekvationen . Den första industrianläggningen i USA som använde destillation som ett medel för havsavsaltning öppnade i Freeport, Texas 1961 med hopp om att föra vattensäkerhet till regionen. Tillgången till kraftfulla datorer har möjliggjort direkta datorsimuleringar av destillationskolonner.
Ansökningar
Tillämpningen av destillation kan grovt delas in i fyra grupper: laboratorieskala , industriell destillation , destillation av örter för parfymer och läkemedel ( örtdestillat ) och livsmedelsbearbetning . De två sistnämnda skiljer sig tydligt från de två förstnämnda genom att destillation inte används som en verklig reningsmetod utan mer för att överföra alla flyktiga ämnen från ursprungsmaterialen till destillatet vid bearbetning av drycker och örter.
Huvudskillnaden mellan destillation i laboratorieskala och industriell destillation är att destillation i laboratorieskala ofta utförs på batch-basis, medan industriell destillation ofta sker kontinuerligt. Vid batchdestillation förändras källmaterialets sammansättning, ångorna i destillationsföreningarna och destillatet under destillationen. Vid batchdestillation laddas (levereras) en destillation med en sats av foderblandning, som sedan separeras i sina komponentfraktioner, som samlas upp sekventiellt från de mest flyktiga till mindre flyktiga, med bottnarna – återstående minsta eller icke-flyktiga fraktion – borttagen i slutet. Destillationsenheten kan sedan laddas om och processen upprepas.
Vid kontinuerlig destillation hålls källmaterialen, ångorna och destillatet vid en konstant sammansättning genom att noggrant fylla på källmaterialet och avlägsna fraktioner från både ånga och vätska i systemet. Detta resulterar i en mer detaljerad kontroll av separationsprocessen.
Idealiserad modell
En vätskas kokpunkt är den temperatur vid vilken vätskans ångtryck är lika med trycket runt vätskan, vilket gör att bubblor kan bildas utan att krossas. Ett specialfall är den normala kokpunkten , där vätskans ångtryck är lika med det omgivande atmosfärstrycket .
Det är en missuppfattning att i en flytande blandning vid ett givet tryck kokar varje komponent vid den kokpunkt som motsvarar det givna trycket, vilket gör att ångorna från varje komponent kan samlas separat och rent. Detta sker dock inte, inte ens i ett idealiserat system. Idealiserade modeller för destillation styrs i huvudsak av Raoults lag och Daltons lag och antar att ång-vätskejämvikter uppnås.
Raoults lag säger att ångtrycket i en lösning är beroende av 1) ångtrycket för varje kemisk komponent i lösningen och 2) den fraktion av lösning varje komponent utgör, aka molfraktionen . Denna lag gäller idealiska lösningar , eller lösningar som har olika komponenter men vars molekylära interaktioner är desamma som eller mycket lik rena lösningar.
Daltons lag säger att det totala trycket är summan av partialtrycken för varje enskild komponent i blandningen. När en flerkomponentsvätska värms upp kommer ångtrycket för varje komponent att stiga, vilket gör att det totala ångtrycket stiger. När det totala ångtrycket når trycket som omger vätskan, uppstår kokning och vätskan förvandlas till gas i hela vätskan. En blandning med en given sammansättning har en kokpunkt vid ett givet tryck när komponenterna är ömsesidigt lösliga. En blandning av konstant sammansättning har inte flera kokpunkter.
En implikation av en kokpunkt är att lättare komponenter aldrig rent "kokar först". Vid kokpunkten kokar alla flyktiga komponenter, men för en komponent är dess procentandel i ångan densamma som dess procentandel av det totala ångtrycket. Lättare komponenter har ett högre partialtryck och är således koncentrerade i ångan, men tyngre flyktiga komponenter har också ett (mindre) partialtryck och förångas nödvändigtvis också, om än i en lägre koncentration i ångan. Faktum är att batchdestillation och fraktionering lyckas genom att variera blandningens sammansättning. Vid batchdestillation förångas satsen, vilket ändrar dess sammansättning; vid fraktionering innehåller vätska högre upp i fraktioneringskolonnen mer ljus och kokar vid lägre temperaturer. Därför, med utgångspunkt från en given blandning, verkar den ha ett kokpunktsintervall istället för en kokpunkt, även om detta beror på att dess sammansättning ändras: varje mellanblandning har sin egen, singulära kokpunkt.
Den idealiserade modellen är korrekt när det gäller kemiskt likartade vätskor, såsom bensen och toluen . I andra fall observeras allvarliga avvikelser från Raoults lag och Daltons lag, mest känt i blandningen av etanol och vatten. Dessa föreningar bildar, när de värms ihop, en azeotrop , vilket är när ångfasen och vätskefasen innehåller samma sammansättning. Även om det finns beräkningsmetoder som kan användas för att uppskatta beteendet hos en blandning av godtyckliga komponenter, är det enda sättet att få exakta ång-vätskejämviktsdata genom mätning.
Det är inte möjligt att fullständigt rena en blandning av komponenter genom destillation, eftersom detta skulle kräva att varje komponent i blandningen har ett nollpartialtryck . Om ultrarena produkter är målet måste ytterligare kemisk separation tillämpas. När en binär blandning förångas och den andra komponenten, t.ex. ett salt, har noll partialtryck för praktiska ändamål, är processen enklare.
Batch- eller differentialdestillation
Uppvärmning av en idealisk blandning av två flyktiga ämnen, A och B, där A har den högre flyktigheten, eller den lägre kokpunkten, i en satsvis destillationsuppsättning (som i en apparat som avbildas i den inledande figuren) tills blandningen kokar resulterar i en ånga ovanför vätskan som innehåller en blandning av A och B. Förhållandet mellan A och B i ångan kommer att skilja sig från förhållandet i vätskan. Förhållandet i vätskan kommer att bestämmas av hur den ursprungliga blandningen framställdes, medan förhållandet i ångan kommer att anrikas på den mer flyktiga föreningen, A (på grund av Raoults lag, se ovan). Ångan går genom kondensorn och avlägsnas från systemet. Detta betyder i sin tur att förhållandet mellan föreningar i den återstående vätskan nu skiljer sig från det initiala förhållandet (dvs mer anrikat på B än i utgångsvätskan).
Resultatet är att förhållandet i vätskeblandningen förändras och blir rikare på komponent B. Detta gör att blandningens kokpunkt stiger, vilket resulterar i en höjning av temperaturen i ångan, vilket resulterar i att förhållandet A ändras. : B i gasfasen (i takt med att destillationen fortsätter, finns det en ökande andel B i gasfasen). Detta resulterar i ett långsamt föränderligt förhållande av A:B i destillatet.
Om skillnaden i ångtryck mellan de två komponenterna A och B är stor – vanligtvis uttryckt som skillnaden i kokpunkter – är blandningen i början av destillationen starkt anrikad på komponent A, och när komponent A har destillerat bort, kokningen vätskan är berikad med komponent B.
Kontinuerlig destillation
Kontinuerlig destillation är en pågående destillation där en vätskeblandning kontinuerligt (utan avbrott) matas in i processen och separerade fraktioner avlägsnas kontinuerligt när utströmmar uppstår över tiden under operationen. Kontinuerlig destillation ger minst två utgående fraktioner, inklusive minst en fraktion av flyktigt destillat, som har kokat och separat uppfångats som en ånga och sedan kondenserats till en vätska. Det finns alltid en bottenfraktion (eller rest) som är den minst flyktiga återstoden som inte har fångats separat som en kondenserad ånga.
Kontinuerlig destillation skiljer sig från batchdestillation i det avseendet att koncentrationerna inte bör ändras över tiden. Kontinuerlig destillation kan köras vid ett stabilt tillstånd under en godtycklig tid. För alla källmaterial med specifik sammansättning är de huvudsakliga variablerna som påverkar renheten hos produkter vid kontinuerlig destillation återflödesförhållandet och antalet teoretiska jämviktssteg, i praktiken bestämt av antalet brickor eller packningshöjden. Återflöde är ett flöde från kondensorn tillbaka till kolonnen, vilket genererar en återvinning som möjliggör en bättre separation med ett givet antal brickor. Jämviktssteg är idealiska steg där kompositioner uppnår ång-vätskejämvikt, upprepar separationsprocessen och tillåter bättre separation givet ett återflödesförhållande. En kolonn med ett högt återflödesförhållande kan ha färre steg, men den återflödessätter en stor mängd vätska, vilket ger en bred kolonn med ett stort uppehåll. Omvänt måste en kolonn med ett lågt återflödesförhållande ha ett stort antal steg, vilket kräver en högre kolonn.
Allmänna förbättringar
Både satsvisa och kontinuerliga destillationer kan förbättras genom att använda en fraktioneringskolonn ovanpå destillationskolven. Kolonnen förbättrar separationen genom att ge en större yta för ångan och kondensatet att komma i kontakt. Detta hjälper den att förbli i jämvikt så länge som möjligt. Kolonnen kan till och med bestå av små delsystem ('brickor' eller 'skålar') som alla innehåller en berikad, kokande vätskeblandning, alla med sin egen ång-vätska-jämvikt.
Det finns skillnader mellan fraktioneringskolonner i laboratorieskala och industriell skala, men principerna är desamma. Exempel på fraktioneringskolonner i laboratorieskala (i ökande effektivitet) inkluderar
- Luftkondensor
- Vigreux kolumn (vanligtvis endast laboratorieskala)
- Packad kolonn (packad med glaspärlor, metallbitar eller annat kemiskt inert material)
- Spinnbandsdestillationssystem .
Laboratorieförfaranden
Destillationer i laboratorieskala körs nästan uteslutande som batchdestillationer. Anordningen som används vid destillation, ibland kallad destillation, består åtminstone av en återkokare eller kastrull i vilken källmaterialet värms upp, en kondensor i vilken den uppvärmda ångan kyls tillbaka till flytande tillstånd och en behållare i vilken den koncentrerade eller renade vätskan, som kallas destillatet, samlas upp. Det finns flera tekniker i laboratorieskala för destillation (se även destillationstyper ).
En helt förseglad destillationsapparat kan uppleva extremt och snabbt varierande inre tryck, vilket kan leda till att den spricker upp vid fogarna. Därför lämnas vanligtvis någon väg öppen (till exempel vid mottagande kolven) för att tillåta det inre trycket att utjämnas med atmosfärstrycket. Alternativt kan en vakuumpump användas för att hålla apparaten vid ett lägre tryck än atmosfärstryck. Om de inblandade ämnena är luft- eller fuktkänsliga kan anslutningen till atmosfären göras genom ett eller flera torkrör packade med material som rensar upp de oönskade luftkomponenterna, eller genom bubblare som ger en rörlig vätskebarriär. Slutligen kan inträde av oönskade luftkomponenter förhindras genom att pumpa in ett lågt men stadigt flöde av lämplig inert gas, såsom kväve , in i apparaten.
Enkel destillation
Vid enkel destillation kanaliseras ångan omedelbart in i en kondensor. Följaktligen är destillatet inte rent utan dess sammansättning är snarare identisk med sammansättningen av ångorna vid den givna temperaturen och trycket. Denna koncentration följer Raoults lag .
Som ett resultat är enkel destillation endast effektiv när vätskekokpunkterna skiljer sig mycket (tumregeln är 25 °C) eller när vätskor separeras från icke-flyktiga fasta ämnen eller oljor. I dessa fall är komponenternas ångtryck vanligtvis tillräckligt olika för att destillatet kan vara tillräckligt rent för sitt avsedda ändamål.
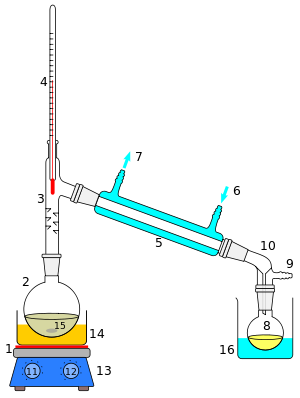
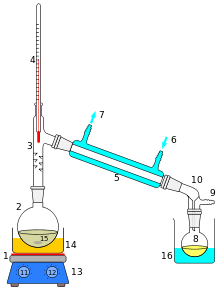
Ett utskuret schema över en enkel destillationsoperation visas till höger. Startvätskan 15 i kokkolven 2 värms upp av en kombinerad värmeplatta och magnetomrörare 13 via ett silikonoljebad (orange, 14). Ångan strömmar genom en kort Vigreux-kolonn 3, sedan genom en Liebig-kondensor 5, kyls av vatten (blått) som cirkulerar genom portarna 6 och 7. Den kondenserade vätskan droppar in i mottagningskolven 8, sittande i ett kylbad (blå, 16). Adaptern 10 har en anslutning 9 som kan monteras på en vakuumpump. Komponenterna är sammankopplade med slipade glasfogar .
Fraktionerad destillation
I många fall kommer kokpunkterna för komponenterna i blandningen att vara tillräckligt nära för att Raoults lag måste beaktas. Därför måste fraktionerad destillation användas för att separera komponenterna genom upprepade förångnings-kondensationscykler i en packad fraktioneringskolonn. Denna separation, genom successiva destillationer, kallas även rektifikation.
När lösningen som ska renas upphettas stiger dess ångor till fraktioneringskolonnen . När den stiger svalnar den och kondenserar på kondensorns väggar och ytorna på förpackningsmaterialet. Här fortsätter kondensatet att värmas upp av de uppstigande heta ångorna; det förångas en gång till. Men sammansättningen av de färska ångorna bestäms återigen av Raoults lag. Varje förångnings-kondensationscykel (kallad en teoretisk platta ) kommer att ge en renare lösning av den mer flyktiga komponenten. I verkligheten inträffar inte varje cykel vid en given temperatur vid exakt samma position i fraktioneringskolonnen; teoretisk platta är alltså ett begrepp snarare än en korrekt beskrivning.
Fler teoretiska plattor leder till bättre separationer. Ett spinnbandsdestillationssystem använder ett spinnband av teflon eller metall för att tvinga de stigande ångorna i nära kontakt med det fallande kondensatet, vilket ökar antalet teoretiska plattor.
Ångdestillation
Liksom vakuumdestillation är ångdestillation en metod för att destillera föreningar som är värmekänsliga. Temperaturen på ångan är lättare att kontrollera än ytan på ett värmeelement , och tillåter en hög hastighet av värmeöverföring utan uppvärmning vid en mycket hög temperatur. Denna process innebär att ånga bubblar genom en upphettad blandning av råmaterialet. Enligt Raoults lag kommer en del av målföreningen att förångas (i enlighet med dess partialtryck). Ångblandningen kyls och kondenseras, vilket vanligtvis ger ett lager olja och ett lager vatten.
Ångdestillation av olika aromatiska örter och blommor kan resultera i två produkter; en eterisk olja samt ett vattnigt örtdestillat . De eteriska oljorna används ofta i parfymeri och aromaterapi medan de vattniga destillaten har många tillämpningar inom aromaterapi , livsmedelsbearbetning och hudvård .

Vakuumdestillation
Vissa föreningar har mycket höga kokpunkter. För att koka sådana föreningar är det ofta bättre att sänka trycket vid vilket sådana föreningar kokas istället för att öka temperaturen. När trycket väl har sänkts till föreningens ångtryck (vid den givna temperaturen), kan kokning och resten av destillationsprocessen påbörjas. Denna teknik kallas vakuumdestillation och den finns vanligtvis i laboratoriet i form av en rotationsindunstare .
Denna teknik är också mycket användbar för föreningar som kokar över sin sönderdelningstemperatur vid atmosfärstryck och som därför skulle sönderdelas genom varje försök att koka dem under atmosfärstryck.
Kort väg och molekylär destillation
Molekylär destillation är vakuumdestillation under trycket på 0,01 torr . 0,01 torr är en storleksordning över högvakuum , där vätskor är i det fria molekylära flödesregimen , dvs den genomsnittliga fria vägen för molekyler är jämförbar med storleken på utrustningen. Gasfasen utövar inte längre något betydande tryck på ämnet som ska förångas, och följaktligen beror avdunstningshastigheten inte längre på trycket. Det vill säga, eftersom kontinuumantagandena om vätskedynamik inte längre gäller, styrs masstransport av molekylär dynamik snarare än vätskedynamik. Således är en kort väg mellan den varma ytan och den kalla ytan nödvändig, typiskt genom att hänga upp en varm platta täckt med en film av foder bredvid en kall platta med en siktlinje däremellan. Molekylär destillation används industriellt för rening av oljor.
Kortvägsdestillation är en destillationsteknik som innebär att destillatet färdas en kort sträcka, ofta bara några centimeter, och som normalt görs vid reducerat tryck. Ett klassiskt exempel skulle vara en destillation där destillatet går från en glaskolv till en annan, utan att det behövs en kondensor som separerar de två kamrarna. Denna teknik används ofta för föreningar som är instabila vid höga temperaturer eller för att rena små mängder förening. Fördelen är att uppvärmningstemperaturen kan vara avsevärt lägre (vid reducerat tryck) än vätskans kokpunkt vid standardtryck, och destillatet behöver bara färdas en kort sträcka innan det kondenserar. En kort väg säkerställer att lite blandning går förlorad på sidorna av apparaten. Kugelrohr -apparaten är en sorts kortvägsdestillationsmetod som ofta innehåller flera kammare för att samla destillatfraktioner.
Luftkänslig vakuumdestillation
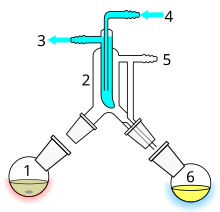
Vissa föreningar har höga kokpunkter och är luftkänsliga . Ett enkelt vakuumdestillationssystem som exemplifierats ovan kan användas, varvid vakuumet ersätts med en inert gas efter att destillationen är fullbordad. Detta är emellertid ett mindre tillfredsställande system om man önskar samla fraktioner under reducerat tryck. För att göra detta kan en "ko" eller "gris" adapter läggas till i änden av kondensorn, eller för bättre resultat eller för mycket luftkänsliga föreningar kan en Perkin triangelapparat användas.
Perkin-triangeln har medel via en serie glas- eller teflonkranar för att tillåta fraktioner att isoleras från resten av destillationen , utan att huvuddelen av destillationen avlägsnas från vare sig vakuum- eller värmekällan, och kan därför förbli i en tillstånd av reflux . För att göra detta isoleras provet först från vakuumet med hjälp av kranarna, vakuumet över provet ersätts sedan med en inert gas (som kväve eller argon ) och kan sedan stoppas och avlägsnas. Ett färskt uppsamlingskärl kan sedan läggas till systemet, evakueras och länkas tillbaka till destillationssystemet via kranarna för att samla upp en andra fraktion, och så vidare, tills alla fraktioner har samlats upp.
Zondestillation
Zondestillation är en destillationsprocess i en lång behållare med partiell smältning av raffinerat material i rörlig vätskezon och kondensation av ånga i den fasta fasen vid kondensatdragning i kallt område. Processen bearbetas i teorin. När zonvärmaren rör sig från toppen till botten av behållaren bildas fast kondensat med oregelbunden föroreningsfördelning. Då kan den mesta rena delen av kondensatet extraheras som produkt. Processen kan upprepas många gånger genom att flytta (utan omsättning) det mottagna kondensatet till bottendelen av behållaren på platsen för raffinerat material. Den oregelbundna föroreningsfördelningen i kondensatet (det vill säga effektiviteten av reningen) ökar med antalet iterationer. Zondestillation är destillationsanalogen för zonomkristallisation. Fördelning av föroreningar i kondensatet beskrivs med kända ekvationer för zonomkristallisation – med ersättning av fördelningskoefficienten k för kristallisation – för separationsfaktorn α för destillationen.
Andra typer
- Processen med reaktiv destillation innebär att man använder reaktionskärlet som destillationsapparat. I denna process är produkten vanligtvis betydligt lägre kokande än dess reaktanter. När produkten bildas från reaktanterna förångas den och avlägsnas från reaktionsblandningen. Denna teknik är ett exempel på en kontinuerlig kontra en satsvis process; Fördelarna inkluderar mindre stilleståndstid för att ladda reaktionskärlet med utgångsmaterial och mindre upparbetning. Destillation "över en reaktant" skulle kunna klassificeras som en reaktiv destillation. Det används vanligtvis för att avlägsna flyktiga föroreningar från destallationsmatningen. Till exempel kan lite kalk tillsättas för att avlägsna koldioxid från vattnet följt av en andra destillation med lite svavelsyra tillsatt för att avlägsna spår av ammoniak.
- Katalytisk destillation är den process genom vilken reaktanterna katalyseras medan de destilleras för att kontinuerligt separera produkterna från reaktanterna. Denna metod används för att hjälpa jämviktsreaktioner att nå fullbordan.
- Pervaporation är en metod för att separera blandningar av vätskor genom partiell förångning genom ett icke-poröst membran .
- Extraktiv destillation definieras som destillation i närvaro av en blandbar, högkokande, relativt icke-flyktig komponent, lösningsmedlet, som inte bildar någon azeotrop med de andra komponenterna i blandningen.
- Snabbavdunstning (eller partiell förångning) är den partiella förångning som uppstår när en mättad vätskeström genomgår en minskning av trycket genom att passera genom en strypventil eller annan strypanordning. Denna process är en av de enklaste enhetsoperationerna, som motsvarar en destillation med endast ett jämviktssteg.
- Samdestillation är destillation som utförs på blandningar där de två föreningarna inte är blandbara. I laboratoriet används Dean-Stark-apparaten för detta ändamål för att avlägsna vatten från syntesprodukter. Bleidner-apparaten är ett annat exempel med två återloppskokande lösningsmedel.
- Membrandestillation är en typ av destillation där ångor från en blandning som ska separeras leds genom ett membran som selektivt tränger igenom en komponent av blandningen. Ångtrycksskillnaden är drivkraften. Det har potentiella tillämpningar vid avsaltning av havsvatten och vid avlägsnande av organiska och oorganiska komponenter.
Enhetsprocessen för avdunstning kan också kallas "destillation":
- Vid rotationsindunstning används en vakuumdestillationsapparat för att avlägsna bulklösningsmedel från ett prov. Vanligtvis genereras vakuumet av en vattensug eller en membranpump .
- I en Kugelrohr-apparat används vanligtvis en kortvägsdestillationsapparat (i allmänhet i kombination med ett (högt) vakuum) för att destillera högkokande (>300 °C) föreningar. Apparaten består av en ugn i vilken blandningen som ska destilleras placeras, en mottagningsdel som är utanför ugnen och ett sätt att rotera provet. Vakuumet genereras normalt genom att använda en högvakuumpump.
Andra användningsområden:
- Torr destillation eller destruktiv destillation , trots namnet, är inte riktigt destillation, utan snarare en kemisk reaktion känd som pyrolys där fasta ämnen värms upp i en inert eller reducerande atmosfär och eventuella flyktiga fraktioner som innehåller högkokande vätskor och pyrolysprodukter, samlas in. Den destruktiva destillationen av trä för att ge metanol är roten till dess vanliga namn – träsprit .
- Frysdestillation är en analog metod för rening med frysning istället för avdunstning. Det är inte riktigt destillation, utan en omkristallisation där produkten är moderluten och inte producerar produkter som motsvarar destillation. Denna process används vid tillverkning av isöl och isvin för att öka etanol- respektive sockerhalten . Det används också för att producera applejack . Till skillnad från destillation koncentrerar frysdestillation giftiga kongener snarare än att ta bort dem; Som ett resultat förbjuder många länder sådan äppeljacka som en hälsoåtgärd. Dessutom kan destillation genom indunstning separera dessa eftersom de har olika kokpunkter.
- Destillation genom filtrering: I tidig alkemi och kemi, även känd som naturfilosofi, var en form av "destillation" genom kapillärfiltrering känd som en form av destillation på den tiden. I denna sattes en serie av koppar eller skålar på ett avtrappat stöd med en "veke" av bomull eller filtliknande material, som hade blötts med vatten eller en klar vätska med varje steg som droppade ner genom den blöta duken genom kapillärverkan i efterföljande steg, skapar en "rening" av vätskan, lämnar fast material kvar i de övre skålarna och renar den efterföljande produkten genom kapillärverkan genom den fuktade trasan. Detta kallades "destillatio" genom filtrering av de som använde metoden.
Azeotropisk process
Interaktioner mellan komponenterna i lösningen skapar egenskaper som är unika för lösningen, eftersom de flesta processer innebär icke-ideala blandningar, där Raoults lag inte håller. Sådana interaktioner kan resultera i en konstant kokande azeotrop som beter sig som om den vore en ren förening (dvs kokar vid en enda temperatur istället för ett område). Vid en azeotrop innehåller lösningen den givna komponenten i samma proportion som ångan, så att avdunstning inte förändrar renheten, och destillation åstadkommer inte separation. Till exempel bildar etylalkohol och vatten en azeotrop på 95,6 % vid 78,1 °C.
Om azeotropen inte anses vara tillräckligt ren för användning, finns det några tekniker för att bryta azeotropen för att ge ett rent destillat. Denna uppsättning tekniker är känd som azeotropisk destillation . Vissa tekniker uppnår detta genom att "hoppa" över den azeotropiska sammansättningen (genom att lägga till ytterligare en komponent för att skapa en ny azeotrop, eller genom att variera trycket). Andra fungerar genom att kemiskt eller fysiskt avlägsna eller binda föroreningen. Till exempel, för att rena etanol över 95 %, kan ett torkmedel (eller torkmedel , såsom kaliumkarbonat ) tillsättas för att omvandla det lösliga vattnet till olösligt kristallvatten . Molekylsilar används ofta även för detta ändamål.
Oblandbara vätskor, såsom vatten och toluen , bildar lätt azeotroper. Vanligtvis hänvisas dessa azeotroper till som en lågkokande azeotrop eftersom kokpunkten för azeotropen är lägre än kokpunkten för någon av de rena komponenterna. Temperaturen och sammansättningen av azeotropen är lätt att förutsäga från ångtrycket hos de rena komponenterna, utan användning av Raoults lag. Azeotropen bryts lätt i en destillationsuppställning genom att använda en vätske-vätskeseparator (en dekanterare) för att separera de två vätskeskikten som kondenseras ovanför. Endast ett av de två vätskeskikten återloppskokas till destillationsuppställningen.
Högkokande azeotroper, såsom en 20 viktprocent blandning av saltsyra i vatten, finns också. Som antyds av namnet är kokpunkten för azeotropen högre än kokpunkten för någon av de rena komponenterna.
För att bryta azeotropiska destillationer och korsa destillationsgränser, som i DeRosier-problemet, är det nödvändigt att öka sammansättningen av ljusnyckeln i destillatet.
Att bryta en azeotrop med enkelriktad tryckmanipulation
Kokpunkterna för komponenter i en azeotrop överlappar varandra för att bilda ett band. Genom att utsätta en azeotrop för ett vakuum eller positivt tryck, är det möjligt att förskjuta kokpunkten för en komponent bort från den andra genom att utnyttja de olika ångtryckskurvorna för var och en; kurvorna kan överlappa vid den azeotropa punkten, men det är osannolikt att de förblir identiska längre längs tryckaxeln till vardera sidan av den azeotropa punkten. När förspänningen är tillräckligt stor överlappar de två kokpunkterna inte längre och därför försvinner det azeotropiska bandet.
Denna metod kan ta bort behovet av att lägga till andra kemikalier till en destillation, men den har två potentiella nackdelar.
Under negativt tryck behövs kraft till en vakuumkälla och destillatens reducerade kokpunkter kräver att kondensorn körs svalare för att förhindra att destillatångor går förlorade till vakuumkällan. Ökade kylbehov kräver ofta extra energi och eventuellt ny utrustning eller byte av kylvätska.
Alternativt, om övertryck krävs, kan standardglas inte användas, energi måste användas för trycksättning och det finns en högre chans att sidoreaktioner inträffar i destillationen, såsom sönderdelning, på grund av de högre temperaturer som krävs för att åstadkomma kokning.
En enkelriktad destillation kommer att förlita sig på en tryckförändring i en riktning, antingen positiv eller negativ.
Trycksvängningsdestillation
Trycksvängningsdestillation är i huvudsak densamma som den enkelriktade destillationen som används för att bryta azeotropa blandningar, men här kan både positiva och negativa tryck användas .
Detta förbättrar destillationens selektivitet och gör det möjligt för en kemist att optimera destillationen genom att undvika extrema tryck och temperaturer som slösar energi. Detta är särskilt viktigt i kommersiella tillämpningar.
Ett exempel på tillämpning av trycksvängningsdestillation är under industriell rening av etylacetat efter dess katalytiska syntes från etanol .
Industriell process
Storskaliga industriella destillationstillämpningar inkluderar både satsvis och kontinuerlig fraktionerad, vakuum-, azeotropisk, extraktiv och ångdestillation. De mest använda industriella tillämpningarna för kontinuerlig fraktionerad destillation i stationärt tillstånd är i petroleumraffinaderier , petrokemiska och kemiska anläggningar och naturgasbearbetningsanläggningar .
För att kontrollera och optimera sådan industriell destillation etableras en standardiserad laboratoriemetod, ASTM D86. Denna testmetod sträcker sig till atmosfärisk destillation av petroleumprodukter med användning av en laboratoriesatsvis destillationsenhet för att kvantitativt bestämma petroleumprodukters kokområdesegenskaper.
Industriell destillation utförs vanligtvis i stora, vertikala cylindriska kolonner, kända som destillationstorn eller destillationskolonner med diametrar från cirka 0,65 till 16 meter (2 ft 2 in till 52 ft 6 in) och höjder som sträcker sig från cirka 6 till 90 meter (20 till 295 fot) eller mer. När processmatningen har en varierande sammansättning, såsom vid destillering av råolja , tillåter vätskeutlopp i intervaller uppåt kolonnen uttag av olika fraktioner eller produkter med olika kokpunkter eller kokintervall. De "lättaste" produkterna (de med den lägsta kokpunkten) kommer ut från toppen av kolonnerna och de "tyngsta" produkterna (de med den högsta kokpunkten) kommer ut från botten av kolonnen och kallas ofta bottnar.
Industriella torn använder återflöde för att uppnå en mer fullständig separation av produkter. Återflöde avser den del av den kondenserade överliggande flytande produkten från ett destillations- eller fraktioneringstorn som återförs till den övre delen av tornet som visas i det schematiska diagrammet för ett typiskt, storskaligt industriellt destillationstorn. Inuti tornet tillhandahåller den nedåtströmmande återflödesvätskan kylning och kondensering av de uppåtströmmande ångorna och ökar därigenom effektiviteten hos destillationstornet. Ju mer återflöde som ges för ett givet antal teoretiska plattor , desto bättre är tornets separation av lägre kokande material från högre kokande material. Alternativt, ju mer återflöde som tillhandahålls för en given önskad separation, desto färre antal teoretiska plattor krävs. Kemiingenjörer måste välja vilken kombination av återflödeshastighet och antal plattor som är både ekonomiskt och fysikaliskt genomförbar för de produkter som renats i destillationskolonnen.
Sådana industriella fraktioneringstorn används också vid kryogen luftseparering , vilket ger flytande syre , flytande kväve och högrent argon . Destillation av klorsilaner möjliggör också produktion av högrent kisel för användning som halvledare .
Design och drift av ett destillationstorn beror på fodret och önskade produkter. Givet en enkel, binär komponentmatning kan analytiska metoder som McCabe–Thiele-metoden eller Fenske-ekvationen användas. För en flerkomponentmatning används simuleringsmodeller både för design och drift. Dessutom är effektiviteten för ång-vätskekontaktanordningarna (kallade "plattor" eller "brickor") som används i destillationstorn vanligtvis lägre än den för ett teoretiskt 100 % effektivt jämviktssteg . Därför behöver ett destillationstorn fler brickor än antalet teoretiska ång-vätskejämviktssteg. En mängd olika modeller har postulerats för att uppskatta brickeffektiviteten.
I modern industriell användning används ett förpackningsmaterial i kolonnen istället för brickor när låga tryckfall över kolonnen krävs. Andra faktorer som gynnar packning är: vakuumsystem, kolonner med mindre diameter, korrosiva system, system som är benägna att skumma, system som kräver låg vätskeuppehåll och batchdestillation. Omvänt är faktorer som gynnar plattkolonner : förekomst av fasta ämnen i inmatningen, höga vätskehastigheter, stora kolonndiametrar, komplexa kolonner, kolonner med stor variation i fodersammansättningen, kolonner med en kemisk reaktion, absorptionskolonner, kolonner begränsade av grundviktstolerans, låg vätskehastighet, stort nedgångsförhållande och de processer som utsätts för processökningar.
Detta förpackningsmaterial kan antingen vara slumpmässigt dumpad packning (25–76 millimeter (1–3 tum) bred) såsom Raschig-ringar eller strukturerad plåt . Vätskor tenderar att väta ytan på förpackningen och ångorna passerar över denna våta yta, där massöverföring äger rum. Till skillnad från konventionell brickdestillation där varje bricka representerar en separat punkt för ång-vätska-jämvikt, är ång-vätska-jämviktskurvan i en packad kolonn kontinuerlig. Vid modellering av packade kolonner är det emellertid användbart att beräkna ett antal "teoretiska steg" för att beteckna separationseffektiviteten för den packade kolonnen med avseende på mer traditionella brickor. Olika formade packningar har olika ytareor och hålrum mellan packningarna. Båda dessa faktorer påverkar packningsprestandan.
En annan faktor utöver packningsformen och ytarean som påverkar prestandan för slumpmässig eller strukturerad packning är vätske- och ångfördelningen som kommer in i den packade bädden. Antalet teoretiska steg som krävs för att göra en given separation beräknas med användning av ett specifikt förhållande mellan ånga och vätska. Om vätskan och ångan inte är jämnt fördelade över det ytliga tornet när den kommer in i den packade bädden, kommer förhållandet mellan vätska och ånga inte att vara korrekt i den packade bädden och den erforderliga separationen kommer inte att uppnås. Packningen verkar inte fungera som den ska. Höjden som motsvarar en teoretisk platta (HETP) kommer att vara större än förväntat. Problemet är inte själva packningen utan den felaktiga fördelningen av vätskorna som kommer in i den packade bädden. Felfördelning av vätska är oftare problemet än ånga. Utformningen av de vätskefördelare som används för att införa matningen och återflödet till en packad bädd är avgörande för att packningen ska prestera maximal effektivitet. Metoder för att utvärdera effektiviteten hos en vätskefördelare för att jämnt fördela vätskan som kommer in i en packad bädd finns i referenser. Betydande arbete har gjorts på detta ämne av Fractionation Research, Inc. (allmänt känd som FRI).
Multieffektdestillation
Målet med multieffektdestillation är att öka energieffektiviteten i processen, för användning vid avsaltning, eller i vissa fall ett steg i produktionen av ultrarent vatten . Antalet effekter är omvänt proportionellt mot kW·h/m 3 för återvunnen vatten, och hänvisar till volymen vatten som återvinns per energienhet jämfört med enkeleffektsdestillation. En effekt är ungefär 636 kW·h/m 3 .
- Flerstegs flashdestillation kan uppnå mer än 20 effekter med termisk energitillförsel, som nämnts i artikeln.
- Ångkompressionsförångning – Kommersiella storskaliga enheter kan uppnå cirka 72 effekter med elektrisk energitillförsel, enligt tillverkarna.
Det finns många andra typer av multi-effektdestillationsprocesser, inklusive en som kallas enkel multi-effektdestillation (MED), där flera kammare, med mellanliggande värmeväxlare, används.
Inom livsmedelsförädling
Drycker
Kolhydratinnehållande växtmaterial tillåts jäsa, vilket ger en utspädd lösning av etanol i processen. Sprit som whisky och rom framställs genom att destillera dessa utspädda lösningar av etanol. Andra komponenter än etanol, inklusive vatten, estrar och andra alkoholer, samlas i kondensatet, vilket står för smaken av drycken. Vissa av dessa drycker lagras sedan i fat eller andra behållare för att få fler smakföreningar och karakteristiska smaker.
Galleri
 |
Kemin använde i sin början retorter som laboratorieutrustning uteslutande för destillationsprocesser. |
 |
En enkel installation för att destillera torr och syrefri toluen . |
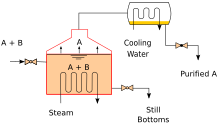
 |
Diagram över en vakuumdestillationskolonn i industriell skala som vanligen används i oljeraffinaderier |
 |
En rotationsindunstare kan destillera lösningsmedel snabbare vid lägre temperaturer genom användning av ett vakuum . |
 |
Destillation med apparater i halvmikroskala. Den fogfria designen eliminerar behovet av att passa ihop bitarna. Den päronformade kolven gör att den sista droppen av rester kan avlägsnas, jämfört med en rundbottnad kolv av liknande storlek . Den lilla uppehållsvolymen förhindrar förluster. En "gris" används för att kanalisera de olika destillaten till tre mottagande kolvar. Vid behov kan destillationen utföras under vakuum med hjälp av vakuumadaptern vid grisen. |
Se även
- Atmosfärisk destillation av råolja
- Clyssus
- Doftextraktion
- Lågtemperaturdestillation
- Mikrodestilleri
- Sublimering
- Dixon ringar
- Slumpmässig kolumnpackning
Referenser
Vidare läsning
- Allchin, FR (mars 1979). "Indien: Destillationens gamla hem?". Man . 14 (1): 55–63. doi : 10.2307/2801640 . JSTOR 2801640 .
- Geankoplis, Christie John (2003). Transportprocesser och separationsprocessprinciper (4:e upplagan). Prentice Hall. ISBN 978-0-13-101367-4.
- Needham, Joseph (1980). Vetenskap och civilisation i Kina . Cambridge University Press. ISBN 0-521-08573-X .
externa länkar
- Alkoholdestillation
- Fallstudie: Petroleumdestillation
- "Binary Vapor-Liquid Equilibrium Data" (sökbar databas) . Chemical Engineering Research Information Center . Hämtad 5 maj 2007 .