Adenosindeaminas - Adenosine deaminase
| Adenosin/AMP deaminas | |||||||||
|---|---|---|---|---|---|---|---|---|---|
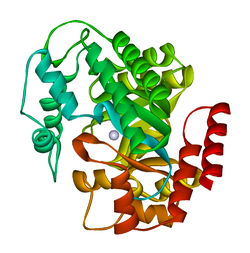
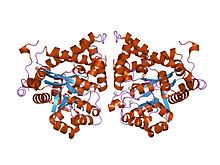 kristallstruktur av plasmodium yoelii adenosindeaminas (py02076)
| |||||||||
| Identifierare | |||||||||
| Symbol | A_deaminase | ||||||||
| Pfam | PF00962 | ||||||||
| Pfam -klan | CL0034 | ||||||||
| InterPro | IPR001365 | ||||||||
| PROSIT | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| CDD | cd01320 | ||||||||
| |||||||||
| Adenosindeaminas (editas) domän | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifierare | |||||||||
| Symbol | A_deamin | ||||||||
| Pfam | PF02137 | ||||||||
| InterPro | IPR002466 | ||||||||
| PROSIT | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| |||||||||
| Adenosin/AMP deaminas N-terminal | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifierare | |||||||||
| Symbol | A_deaminase_N | ||||||||
| Pfam | PF08451 | ||||||||
| InterPro | IPR013659 | ||||||||
| |||||||||
Adenosindeaminas (även känt som adenosinaminhydrolas eller ADA ) är ett enzym ( EC 3.5.4.4 ) som är involverat i purinmetabolismen . Det behövs för nedbrytning av adenosin från mat och för omsättningen av nukleinsyror i vävnader.
Dess främsta funktion hos människor är utveckling och underhåll av immunsystemet. ADA: s fulla fysiologiska roll är dock ännu inte helt klarlagd.
Strukturera
ADA finns i både liten form (som en monomer) och stor form (som ett dimerkomplex). I monomerformen är enzymet en polypeptidkedja, vikt i åtta strängar av parallella α/β -fat, som omger en central djupficka som är den aktiva platsen. Förutom de åtta centrala β-tunnorna och åtta perifera a-helixer innehåller ADA också fem ytterligare spiraler: rester 19-76 gånger i tre spiraler, belägna mellan β1 och α1-veck; och två antiparallella karboxiterminala spiraler är belägna tvärs β-fatets aminoterminal.
Den aktiva platsen för ADA innehåller en zinkjon, som är belägen i den aktivaste platsens djupaste urtag och samordnas av fem atomer från His15, His17, His214, Asp295 och substratet. Zink är den enda kofaktorn som är nödvändig för aktivitet.
Substratet, adenosin, stabiliseras och binds till det aktiva stället med nio vätebindningar. Karboxylgruppen för Glu217, ungefär i samma plan som substratpurinringen, är i position för att bilda en vätebindning med N1 i substratet. Karboxylgruppen i Asp296, som också är planplanerad med substratpurinringen, bildar vätebindning med N7 i substratet. NH -gruppen i Gly184 är i position för att bilda en vätebindning med N3 i substratet. Asp296 bildar bindningar både med Zn 2 + -jonen såväl som med 6-OH av substratet. His238 binder också väte till substrat 6-OH. 3'-OH i substratet ribos bildar en vätebindning med Asp19, medan 5'-OH bildar en vätebindning med His17. Ytterligare två vätebindningar bildas till vattenmolekyler, vid öppnandet av det aktiva stället, av 2'-OH och 3'-OH i substratet.
På grund av att den aktiva platsen inuti enzymet försvinner, utsöndras substratet, när det väl är bundet, nästan helt från lösningsmedel. Ytsexponeringen av substratet för lösningsmedel när det är bundet är 0,5% ytaxponeringen för substratet i fritt tillstånd.
Reaktioner
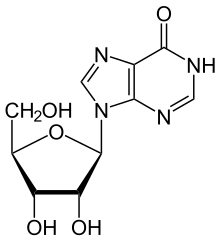
ADA irreversibelt deaminerar adenosin, konvertera den till den relaterade nukleosid inosin genom substitution av den amino -gruppen med en ketogrupp.
Inosin kan sedan deribosyleras (avlägsnas från ribos ) av ett annat enzym som kallas purinnukleosidfosforylas (PNP) och omvandlar det till hypoxantin .
Katalysmekanism
Den föreslagna mekanismen för ADA-katalyserad deaminering är stereospecifik additionseliminering via tetraedrisk intermediär. Med endera mekanismen aktiverar Zn 2+ som en stark elektrofil en vattenmolekyl, som deprotoneras av den grundläggande Asp295 för att bilda den angripande hydroxiden. His238 orienterar vattenmolekylen och stabiliserar laddningen av den angripande hydroxiden. Glu217 protoneras för att donera en proton till N1 i substratet.
Reaktionen är stereospecifik på grund av placeringen av zink-, Asp295- och His238-resterna, som alla vetter mot B-sidan av purinringen i substratet.
Konkurrenskraftig hämning har observerats för ADA, där produkten inosin verkar på den konkurrerande hämmaren för enzymatisk aktivitet.
Fungera
ADA anses vara en av de viktigaste enzymerna för purinmetabolism. Enzymet har hittats i bakterier, växter, ryggradslösa djur, ryggradsdjur och däggdjur, med hög bevarande av aminosyrasekvens . Den höga graden av bevarande av aminosyrasekvens föreslår den avgörande karaktären av ADA i purinbärgningsvägen.
ADA hos människor är främst involverat i utvecklingen och underhållet av immunsystemet. ADA -samband har dock också observerats med differentiering av epitelceller , neurotransmission och underhåll av dräktigheten . Det har också föreslagits att ADA, förutom nedbrytning av adenosin, stimulerar frisättning av excitatoriska aminosyror och är nödvändig för koppling av A1 -adenosinreceptorer och heterotrimära G -proteiner . Adenosindeaminasbrist leder till lungfibros, vilket tyder på att kronisk exponering för höga nivåer av adenosin kan förvärra inflammationssvar snarare än att undertrycka dem. Det har också erkänts att adenosindeaminasprotein och aktivitet uppregleras i mushjärtan som överuttrycker HIF1α , vilket delvis förklarar de försvagade nivåerna av adenosin i HIF-1a som uttrycker hjärtan under ischemisk stress.
Patologi
Vissa mutationer i genen för adenosindeaminas gör att den inte uttrycks. Den resulterande bristen är en orsak till allvarlig kombinerad immunbrist (SCID), särskilt till autosomalt recessivt arv. Bristfälliga nivåer av ADA har också associerats med lunginflammation, tymisk celldöd och defekt T-cellreceptorsignalering.
Omvänt är mutationer som orsakar att detta enzym överuttrycks en orsak till hemolytisk anemi .
Det finns vissa bevis för att en annan allel (ADA2) kan leda till autism .
Förhöjda nivåer av ADA har också associerats med AIDS .
Isoformer
Det finns 2 isoformer av ADA: ADA1 och ADA2.
- ADA1 finns i de flesta kroppsceller, särskilt lymfocyter och makrofager , där det inte bara finns i cytosolen och kärnan utan också som ektoformen på cellmembranet fäst vid dipeptidylpeptidas-4 (aka, CD26). ADA1 är mest involverad i intracellulär aktivitet och finns både i liten form (monomer) och stor form (dimer). Mellankonvertering av små till stora former regleras av en "omvandlingsfaktor" i lungan.
- ADA2 identifierades först i mänsklig mjälte. Det hittades därefter i andra vävnader inklusive makrofagen där det existerar samtidigt med ADA1. De två isoformerna reglerar förhållandet mellan adenosin och deoxyadenosin som förstärker dödandet av parasiter. ADA2 finns huvudsakligen i humanplasma och serum och existerar enbart som en homodimer.
Klinisk signifikans
ADA2 är den dominerande formen som finns i humant blodplasma och ökar vid många sjukdomar, särskilt de som är associerade med immunsystemet: till exempel reumatoid artrit , psoriasis och sarkoidos . Plasma ADA2 -isoformen ökar också i de flesta cancerformer. ADA2 är inte allestädes närvarande men finns samtidigt med ADA1 endast i monocyter-makrofager.
Total plasma ADA kan mätas med högpresterande vätskekromatografi eller enzymatiska eller kolorimetriska tekniker. Det kanske enklaste systemet är mätningen av ammoniaken som frigörs från adenosin när den bryts ner till inosin. Efter inkubation av plasma med en buffrad lösning av adenosin reagerar ammoniaken med ett Berthelot -reagens för att bilda en blå färg som står i proportion till mängden enzymaktivitet. För att mäta ADA2 tillsätts erytro-9- (2-hydroxi-3-nonyl) adenin (EHNA) före inkubation för att hämma den enzymatiska aktiviteten av ADA1. Det är frånvaron av ADA1 som orsakar SCID .
ADA kan också användas vid bearbetning av lymfocytisk pleural effusion eller peritoneal ascites , genom att sådana prover med låga ADA -nivåer väsentligen utesluter tuberkulos från övervägande.
Tuberkulos pleural effusion kan nu diagnostiseras exakt genom ökade nivåer av pleuralvätska adenosindeaminas, över 40 U per liter.
Cladribine och Pentostatin är antineoplastiska medel som används vid behandling av hårcellleukemi ; deras verkningsmekanism är hämning av adenosindeaminas.
Se även
Referenser
Vidare läsning
- da Cunha JG (1992). "[Adenosindeaminas. Ett pluridisciplinärt enzym]". Acta Médica Portuguesa . 4 (6): 315–23. PMID 1807098 .
- Franco R, Casadó V, Ciruela F, Saura C, Mallol J, Canela EI, Lluis C (juli 1997). "Cellyteadenosindeaminas: mycket mer än ett ektoenzym". Framsteg inom neurobiologi . 52 (4): 283–94. doi : 10.1016/S0301-0082 (97) 00013-0 . PMID 9247966 . S2CID 40318396 .
- Valenzuela A, Blanco J, Callebaut C, Jacotot E, Lluis C, Hovanessian AG, Franco R (1997). "HIV-1-hölje gp120 och virala partiklar blockerar adenosindeaminasbindning till humant CD26". Framsteg inom experimentell medicin och biologi . 421 : 185–92. doi : 10.1007/978-1-4757-9613-1_24 . ISBN 978-1-4757-9615-5. PMID 9330696 .
- Moriwaki Y, Yamamoto T, Higashino K (okt 1999). "Enzymer involverade i purinmetabolism-en genomgång av histokemisk lokalisering och funktionella konsekvenser". Histologi och histopatologi . 14 (4): 1321–40. PMID 10506947 .
- Hirschhorn R (1993). "Identifiering av två nya missense-mutationer (R156C och S291L) hos två ADA-SCID-patienter ovanliga för svar på behandling med partiella utbytestransfusioner". Mänsklig mutation . 1 (2): 166–8. doi : 10.1002/humu.1380010214 . PMID 1284479 . S2CID 44617309 .
- Berkvens TM, van Ormondt H, Gerritsen EJ, Khan PM, van der Eb AJ (aug 1990). "Identisk 3250-bp-radering mellan två AluI-upprepningar i ADA-generna hos orelaterade ADA-SCID-patienter". Genomik . 7 (4): 486–90. doi : 10.1016/0888-7543 (90) 90190-6 . PMID 1696926 .
- Aran JM, Colomer D, Matutes E, Vives-Corrons JL, Franco R (aug 1991). "Förekomst av adenosindeaminas på ytan av mononukleära blodkroppar: immunokemisk lokalisering med hjälp av ljus- och elektronmikroskopi" . Journal of Histochemistry and Cytochemistry . 39 (8): 1001–8. doi : 10.1177/39.8.1856451 . PMID 1856451 .
- Bielat K, Tritsch GL (apr 1989). "Ecto-enzymaktivitet av humant erytrocyt adenosindeaminas". Molekylär och cellulär biokemi . 86 (2): 135–42. doi : 10.1007/BF00222613 . PMID 2770711 . S2CID 20850552 .
- Hirschhorn R, Tzall S, Ellenbogen A, Orkin SH (feb 1989). "Identifiering av en punktmutation som resulterar i ett värmelabilt adenosindeaminas (ADA) hos två orelaterade barn med partiell ADA-brist" . Journal of Clinical Investigation . 83 (2): 497–501. doi : 10.1172/JCI113909 . PMC 303706 . PMID 2783588 .
- Murray JL, Perez-Soler R, Bywaters D, Hersh EM (jan 1986). "Minskad adenosindeaminas (ADA) och 5 nukleotidas (5NT) aktivitet i perifera blod -T -celler vid Hodgkins sjukdom". American Journal of Hematology . 21 (1): 57–66. doi : 10.1002/ajh.2830210108 . PMID 3010705 . S2CID 25540139 .
- Wiginton DA, Kaplan DJ, States JC, Akeson AL, Perme CM, Bilyk IJ, Vaughn AJ, Lattier DL, Hutton JJ (dec 1986). "Komplett sekvens och struktur för genen för humant adenosindeaminas". Biokemi . 25 (25): 8234–44. doi : 10.1021/bi00373a017 . PMID 3028473 .
- Akeson AL, Wiginton DA, Dusing MR, States JC, Hutton JJ (nov 1988). "Mutanta humana adenosindeaminasalleler och deras uttryck genom transfektion i fibroblaster" . Journal of Biological Chemistry . 263 (31): 16291–6. doi : 10.1016/S0021-9258 (18) 37591-4 . PMID 3182793 .
- Glader BE, Backer K (feb 1988). "Förhöjd röd cell adenosindeaminasaktivitet: en markör för störd erytropoes vid Diamond-Blackfan-anemi och andra hematologiska sjukdomar". British Journal of Hematology . 68 (2): 165–8. doi : 10.1111/j.1365-2141.1988.tb06184.x . PMID 3348976 . S2CID 44789636 .
- Petersen MB, Tranebjaerg L, Tommerup N, Nygaard P, Edwards H (feb 1987). "Ny tilldelning av adenosindeaminasgenloket till kromosom 20q13 X 11 genom studie av en patient med interstitiell deletion 20q" . Journal of Medical Genetics . 24 (2): 93–6. doi : 10.1136/jmg.24.2.93 . PMC 1049896 . PMID 3560174 .
- Orkin SH, Goff SC, Kelley WN, Daddona PE (apr 1985). "Övergående uttryck av humana adenosindeaminas -cDNA: identifiering av en icke -funktionell klon som härrör från en enda aminosyrasubstitution" . Molekylär och cellulär biologi . 5 (4): 762–7. doi : 10.1128/mcb.5.4.762 . PMC 366780 . PMID 3838797 .
- Valerio D, Duyvesteyn MG, Dekker BM, Weeda G, Berkvens TM, van der Voorn L, van Ormondt H, van der Eb AJ (feb 1985). "Adenosindeaminas: karakterisering och uttryck av en gen med en anmärkningsvärd promotor" . EMBO Journal . 4 (2): 437–43. doi : 10.1002/j.1460-2075.1985.tb03648.x . PMC 554205 . PMID 3839456 .
- Bonthron DT, Markham AF, Ginsburg D, Orkin SH (aug 1985). "Identifiering av en punktmutation i adenosindeaminasgenen som är ansvarig för immunbrist" . Journal of Clinical Investigation . 76 (2): 894–7. doi : 10.1172/JCI112050 . PMC 423929 . PMID 3839802 .
- Daddona PE, Shewach DS, Kelley WN, Argos P, Markham AF, Orkin SH (okt 1984). "Humant adenosindeaminas. CDNA och fullständig primär aminosyrasekvens" . Journal of Biological Chemistry . 259 (19): 12101–6. doi : 10.1016/S0021-9258 (20) 71325-6 . PMID 6090454 .
- Valerio D, Duyvesteyn MG, Meera Khan P, Geurts van Kessel A, de Waard A, van der Eb AJ (nov 1983). "Isolering av cDNA -kloner för humant adenosindeaminas". Gene . 25 (2–3): 231–40. doi : 10.1016/0378-1119 (83) 90227-5 . PMID 6198240 .
externa länkar
- ADA -plats för mänsklig gen i UCSC Genome Browser .
- ADA -information om mänskliga gener i UCSC Genome Browser .
- PDBe-KB ger en översikt över all strukturinformation som finns tillgänglig i PDB för humant adenosindeaminas
- PDBe-KB ger en översikt över all strukturinformation som finns tillgänglig i PDB för mus-adenosindeaminas